Diclorodifenildicloroetileno
Diclorodifenildicloroetileno
| |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||
 | |||||||||||||||||||
| Nomes | |||||||||||||||||||
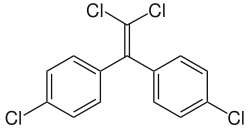
| Nome IUPAC | 1,1-bis-(4-clorofenil)-2,2-dicloroeteno | ||||||||||||||||||
| Outros nomes | Dichlorodiphenyldichloroethylene | ||||||||||||||||||
| |||||||||||||||||||
| |||||||||||||||||||
| Página de dados suplementares | |||||||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||||||
Diclorodifenildicloroetileno (DDE) é um composto químico formado a partir do DDT pela perda de um cloreto de hidrogénio (desidroalogenação) e é um dos produtos de degradação mais comuns do DDT.[1] Devido à elevada frequência de utilização do DDT na sociedade e na agricultura em meados do século XX, o DDT e o DDE ainda podem ser encontrados com muita frequência em amostras de tecido animal, apesar da atual proibição destes produtos. É particularmente perigoso porque é lipossolúvel como os outros organoclorados, pelo que raramente é excretado do organismo e as suas concentrações tendem a aumentar ao longo da vida (bioacumulação). A principal excepção a isto é a excreção de DDE no leite, que transporta uma porção substancial de DDE da mãe para o bebé ou criança.[2] Para além da sua acumulação num organismo ao longo da sua vida, a estabilidade deste composto faz com que se bioacumule no ambiente e na cadeia trófica, o que amplifica os seus efeitos negativos.
Resumo
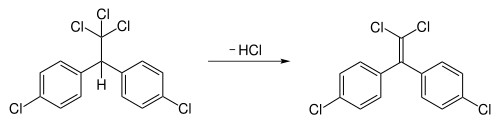
O DDE é gerado pela desidroalogenação do DDT. A perda de HCl no DDT resulta na formação de uma ligação dupla nos átomos centrais de carbono (anteriormente quaternários).
Toxicidade
A toxicidade do DDE foi medida em ratos e verificou-se que era tóxico nestes animais na dose de 79,6 mg/kg.[3] O DDE e a sua molécula-mãe DDT são toxinas reprodutivas para certas espécies de aves. Por exemplo, é uma das principais razões para o declínio da águia-americana (Haliaeetus leucocephalus),[4] o pelicano-pardo (Pelecanus occidentalis)[5] o falcão-peregrino (Falco peregrinus) e a águia-pesqueira (Pandion haliaetus).[6] Estes compostos provocam o adelgaçamento das cascas dos ovos nas espécies susceptíveis, o que faz com que as aves partam os ovos facilmente quando os incubando.[7] aves de rapina, aves aquáticas e pássaros canoros são mais suscetíveis a este adelgaçamento da carapaça do que as galinhas e outros galiformes, e neste efeito o DDE parece ser mais potente que o DDT.[6]
Mecanismo
O mecanismo biológico que causa o adelgaçamento da casca do ovo não está totalmente esclarecido, mas pensa-se que o p,p'-DDE altera a capacidade da glândula da casca de excretar carbonato de cálcio no ovo em desenvolvimento.[6][8][9][10][11] Vários mecanismos podem estar em ação, ou mecanismos diferentes podem operar em espécies diferentes.[6] Alguns estudos indicaram que, embora os níveis de DDE tenham descido drasticamente no ambiente desde a proibição do uso deste composto, as cascas dos ovos permaneceram 10 a 12% mais finas do que antes do uso do DDT.[12]
Alguns estudos indicaram inicialmente que o DDE é um disruptor endócrino[13] e contribui para o cancro da mama, mas estudos mais recentes forneceram fortes evidências de que não existe ligação entre a exposição ao DDE e o cancro da mama.[14] O que é mais claro é que o DDE é um antagonista fraco do receptor de androgénio e pode causar anomalias no trato genital masculino.[15][16]
Estudos feitos em animais indicaram que os pesticidas organoclorados, como o DDE, são neurotóxicos, causam estresse oxidativo, e danificam o sistema dopaminérgico do cérebro.[17]
Ver também
Referências
- ↑ «ATSDR - Public Health Statement: DDT, DDE and DDD». Consultado em 16 de abril de 2016. Cópia arquivada em 28 de junho de 2016
- ↑ Excreção no leite materno Cinética de b-HCH, pp’DDE e pp’DDT. Boletim de Contaminação Ambiental e Toxicologia, Dezembro 2009;83(6):869-73
- ↑ «MSDS do NIST DDE» (PDF). 13 de abril de 2020. Consultado em 16 de abril de 2016. Cópia arquivada (PDF) em 13 de abril de 2020
- ↑ Stokstad, E (2007). «Conservação da espécie. A águia-americana ainda consegue planar após ser retirada da lista?». Science. 316 (5832): 1689–90. PMID 17588911. doi:10.1126/science.316.5832.1689
- ↑ "Vida selvagem e plantas ameaçadas e em perigo de extinção; 12 meses" Petição que conclui e propõe uma regra para remover o pelicano-pardo (Pelecanus occidentalis) da Lista Federal de Vida Selvagem Ameaçada e em Perigo de Extinção; Regra proposta", Serviço de Pesca e Vida Selvagem, Departamento do Interior dos EUA, 20 de Fevereiro de 2008.
- ↑ a b c d «ATSDR - Perfil toxicológico: DDT, DDE, DDD». Consultado em 16 de abril de 2016. Cópia arquivada em 13 de abril de 2020
- ↑ «Primavera selvagem da Califórnia de 1994 - Falcões peregrinos». Consultado em 16 de abril de 2016. Arquivado do original em 16 de junho de 2007
- ↑ Recovery Plan for the California Condor, U.S. Fish and Wildlife Service, April 1996, page 23
- ↑ «DDE concentration and percent eggshell thinning in Double-crested Conmorant eggs(North Channel, Lake Huron, Ont.)». Consultado em 16 de abril de 2016. Arquivado do original em 28 de junho de 2007
- ↑ Guillette, Louis J., Jr. (2006). «Endocrine Disrupting Contaminants» (PDF). Consultado em 2 de fevereiro de 2007. Arquivado do original (PDF) em 18 de novembro de 2010
- ↑ Lundholm, C.E. (1997). «DDE-Induced eggshell thinning in birds». Comp Biochem Physiol C Pharmacol Toxicol Endocrinol. 118 (2): 113–28. PMID 9490182. doi:10.1016/S0742-8413(97)00105-9
- ↑ «Division of Environmental Quality». Consultado em 16 de abril de 2016. Cópia arquivada em 3 de março de 2008
- ↑ «Chemical fact sheet: Organochlorine - The Breast Cancer Fund». Consultado em 16 de abril de 2016. Cópia arquivada em 9 de outubro de 2006
- ↑ Questões sobre os disruptores endócrinos
- ↑ Longnecker, M. P.; Gladen, B. C.; Cupul-Uicab, L. A.; Romano-Riquer, S. P.; Weber, J.-P.; Chapin, R. E.; Hernandez-Avila, M. (2007). «In utero exposure to the antiandrogen 1,1-dichloro-2,2-bis(p-chlorophenyl)ethylene (DDE) in relation to anogenital distance in male newborns from Chiapas, México». American Journal of Epidemiology. 165 (9): 1015–22. PMC 1852527
 . PMID 17272288. doi:10.1093/aje/kwk109
. PMID 17272288. doi:10.1093/aje/kwk109
- ↑ Hejmej, Anna; Kotula-Balak, Magorzata; Bilinsk, Barbara (2011). «Antiandrogenic and Estrogenic Compounds: Effect on Development and Function of Male Reproductive System». doi:10.5772/28538
- ↑ Pesticide Exposure Linked to Parkinson's, Alzheimer's Disease