Descarboxilação do piruvato
A descarboxilação do piruvato, ou descarboxilação oxidativa do piruvato, é a reação enzimática em que o piruvato perde o seu grupo carboxilo sob a forma de CO2, sendo reduzido a um grupo de dois carbonos (acetila), que se liga à coenzima A, formando a acetil-CoA. Esta reação é essencial para que o esqueleto de carbono do piruvato citosólico entre nas reações do ciclo de Krebs e continue a via aeróbia da respiração celular, ligando assim a glicólise ao ciclo de Krebs.[1]
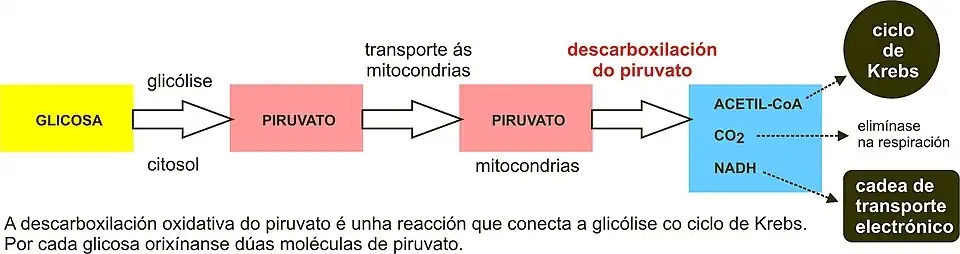
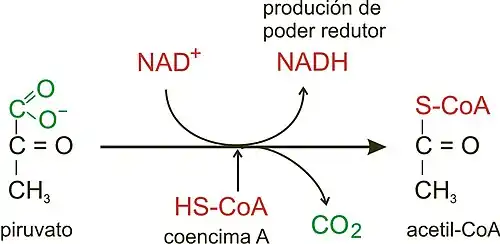
A reacção é uma descarboxilação oxidativa, afastada do equilíbrio (ΔGº' = -8,0 kcal/mol), catalisada pelo complexo enzimático piruvato desidrogenase, que ocorre nas mitocôndrias dos eucariotas e no citoplasma bacteriano [2]. Na reação forma-se NADH, uma molécula com grande capacidade redutora (poder redutor). Por cada glicose (molécula de 6 carbonos) que entra na glicólise, formam-se dois piruvatos (3 carbonos), mas durante a reação de descarboxilação do piruvato, um dos carbonos do piruvato (o grupo carboxilo) é perdido sob a forma de CO2, e os dois carbonos restantes são cedidos à coenzima A (CoA), formando acetil-CoA. A CoA possui um grupo -SH reativo, através do qual se liga à acetila, frequentemente representada nas reações (CoA-SH).
O destino do NADH formado é ceder os seus eletrões à cadeia de transporte de eletrões, de modo a que o ATP seja produzido na fosforilação oxidativa subsequente. O destino da acetil-CoA é ceder a acetila ao ciclo de Krebs, que também vai produzir energia. Esta reação é especialmente importante no fígado, pois impede que o piruvato citosólico seja utilizado na gliconeogénese ou transaminação e obriga-o a entrar nas mitocôndrias e no ciclo de Krebs para produzir ATP ou formar citrato, que pode ser exportado para o citosol para a síntese lipídica.
Nos humanos, em condições anaeróbias, o piruvato pode ser fermentado em lactato no citosol, mas, em condições aeróbias, entra na mitocôndria para ser descarboxilado. Para facilitar a entrada do piruvato na mitocôndria, existe uma série de transportadores específicos na membrana mitocondrial. Na membrana mitocondrial externa, existem porinas através das quais o piruvato passa para o espaço intermembranar e, em seguida, o transportador piruvato translocase da membrana mitocondrial interna transfere o piruvato do espaço intermembranar para a matriz mitocondrial.
Em organismos anaeróbios, a descarboxilação do piruvato difere do processo em organismos aeróbios pelo facto de o aceptor de electrões ser uma proteína ferro-enxofre e não NAD+. A conversão é catalisada por uma enzima dependente de tiamina, que também acila a coenzima A. [3] Os equivalentes de redução são removidos pela produção de H2 pela enzima hidrogenase.
Fases da reacção enzimática
O complexo piruvato desidrogenase é um complexo multienzimático de 96 subunidades nos eucariotas, que formam três enzimas e no qual estão envolvidos cinco coenzimas ou grupos prostéticos. As enzimas são: piruvato desidrogenase (E1), di-hidrolipoil transacetilase (E2) e di-hidrolipoil desidrogenase (E3). As coenzimas são: tiamina pirofosfato (TPP), FAD, CoA, NAD+ e ácido lipoico. Todas estas enzimas e coenzimas estão intimamente relacionadas no complexo, o que facilita a reação.
(Embora o piruvato sofra aqui descarboxilação, note-se que a enzima é chamada piruvato desidrogenase, que não deve ser confundida com a piruvato descarboxilase, que está envolvida na fermentação alcoólica para formar acetaldeído.)
A reacção de descarboxilação do piruvato pode ser dividida em cinco etapas[4]:
Fase 1
O piruvato perde o seu grupo carboxilo ao reagir com o TPP ligado à piruvato desidrogenase (E1) no complexo. O resultado é que o grupo de dois carbonos remanescente do piruvato se liga ao anel tiazol do TPP, formando um grupo hidroxietil ligado ao TPP. Os átomos do grupo carboxilo do piruvato são perdidos como CO2, que é o primeiro produto final desprendido da reação.
piruvato + H+ + E1-TPP → E1-TPP-hidroxietil + CO2
Fase 2
A piruvato desidrogenase do complexo também realiza a fase 2, catalisando a passagem do grupo hidroxietil do TPP para o grupo prostético lipoilo da enzima dihidrolipoil transacetilase (E2), formando um grupo acetil ligado por uma ligação tioéster aos grupos lipoílo reduzidos.
E1-TPP-hidroxietil + E2-lipoil → E1-TPP + E2-lipoil-S-acetil
Fase 3
Agora, intervém a coenzima A (CoA-SH), que reage com a acetila ligada à di-hidrolipoil transacetilase, que perde a sua acetila, que passa para a coenzima A, formando acetil-CoA, e os grupos lipoílo são reduzidos. O segundo produto final da reação, o acetil-CoA, foi, portanto, formado.
E2-lipoil-S-acetil + CoA-SH → E2-lipoil-SH (reduzido) + acetil-S-CoA
Fase 4
Agora, os grupos lipoílo reduzidos de E2 devem ser oxidados. Isto é feito pela terceira enzima do complexo, a di-hidrolipoil desidrogenase, que possui o grupo prostético FAD, que captura dois H dos grupos lipoilo do E2, oxidando-os novamente e formando FADH2.
E2-lipoil-SH (reduzido) + E3-FAD → E2-lipoil (oxidado) + E3-FADH2
Fase 5
Agora, o grupo prostético FADH2 vai reduzir a coenzima NAD+. A di-hidrolipoil desidrogenase (E3) transfere os dois H de FADH2 para NAD+, formando NADH + H+. Isto produz o último produto final da reação, o NADH (poder redutor).
E3-FADH2 + NAD+ → E3-FAD + NADH + H+
Saúde
Uma vez que a reacção de descarboxilação do piruvato envolve coenzimas que possuem grupos derivados de vitaminas em parte da sua estrutura, a deficiência destas vitaminas pode afectar a reacção e provocar vários distúrbios [4]. A tiamina ou vitamina B1 faz parte da TPP, a riboflavina ou vitamina B2 do FAD, o ácido pantoténico ou vitamina B5 da coenzima A e a nicotinamida ou vitamina B3 do NAD. Além disso, o ácido lipóico, que dá origem aos grupos di-hidrolipoil, é um fator de crescimento para muitos microrganismos, embora possa ser sintetizado por animais superiores.
Um exemplo de um distúrbio por deficiência de vitaminas é o beribéri, uma doença causada pela deficiência de tiamina ou vitamina B1. Os animais com esta deficiência nutricional não conseguem descarboxilar o piruvato normalmente, o que afeta especialmente o cérebro, que só consegue obter energia a partir da glicose através do piruvato, desenvolvendo polineurites.
Ver também
- Piruvato desidrogenase (enzima que realiza a descarboxilação oxidativa do piruvato)
- Piruvato descarboxilase (enzima que realiza a descarboxilação do piruvato na fermentação alcoólica)
Referências
- ↑ Alberts et al. Molecular Biology of the Cell. Garland Science, 2001. ISBN 0-8153-4072-9
- ↑ Raven et al. Biologia, 8ª edição. McGraw Hill, 2008. ISBN 978-0-07-110202-5
- ↑ Eric Chabrière, Xavier Vernède, Bruno Guigliarelli, Marie-Hélène Charon, E. Claude Hatchikian, Juan C. Fontecilla-Camps “Crystalline Structure of the Piruvato-Free Radical Intermediate:Ferredoxina Oxidoredutase” Science 2001, Volume 294, página 2559.
- ↑ a b Lehninger. Princípios de Bioquímica. Omega. 1988. páginas 437-441. ISBN 84-282-0738-0