Dímero de proteína
Em bioquímica, um dímero de proteína é um complexo macromolecular ou multímero formado por dois monômeros de proteína, ou proteínas únicas, que geralmente são ligados de forma não covalente. Muitas macromoléculas, como proteínas ou ácidos nucleicos, formam dímeros. A palavra dímero tem raízes que significam "duas partes", di- + -mer. Um dímero de proteína é um tipo de estrutura quaternária de proteína.
Um homodímero de proteína é formado por duas proteínas idênticas, enquanto um heterodímero de proteína é formado por duas proteínas diferentes.
Exemplos
A maioria dos dímeros de proteínas em bioquímica não são conectados por ligações covalentes. Um exemplo de um heterodímero não covalente é a enzima transcriptase reversa, que é composta por duas cadeias de aminoácidos diferentes.[1] Uma exceção são os dímeros que são ligados por pontes dissulfeto, como a proteína homodimérica NEMO.[2]
Algumas proteínas contêm domínios especializados para garantir a dimerização (domínios de dimerização) e a especificidade.[3]
Os receptores canabinoides acoplados à proteína G têm a capacidade de formar homo e heterodímeros com vários tipos de receptores, como os receptores mu-opioides, dopaminérgicos e adenosina A2.[4]
Fosfatase alcalina
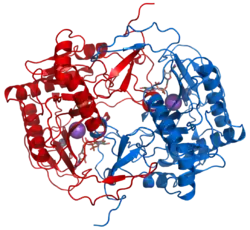
A fosfatase alcalina de E. coli, uma enzima dimérica, exibe complementação intragênica.[5] Ou seja, quando versões mutantes específicas da fosfatase alcalina foram combinadas, as enzimas heterodiméricas formadas como resultado exibiram um nível de atividade mais alto do que seria esperado com base nas atividades relativas das enzimas parentais. Essas descobertas indicaram que a estrutura dimérica da fosfatase alcalina de E. coli permite interações cooperativas entre os monômeros mutantes constituintes que podem gerar uma forma mais funcional da holoenzima. O dímero possui dois locais ativos, cada um contendo dois íons de zinco e um íon de magnésio.[6]
Ver também
Notas
- Este artigo foi inicialmente traduzido, total ou parcialmente, do artigo da Wikipédia em inglês cujo título é «Protein dimer».
Referências
- ↑ Sluis-Cremer N, Hamamouch N, San Félix A, Velazquez S, Balzarini J, Camarasa MJ (agosto de 2006). «Structure-activity relationships of [2',5'-bis-O-(tert-butyldimethylsilyl)-beta-D-ribofuranosyl]- 3'-spiro-5' '-(4' '-amino-1' ',2' '-oxathiole-2' ',2' '-dioxide)thymine derivatives as inhibitors of HIV-1 reverse transcriptase dimerization». J. Med. Chem. 49 (16): 4834–41. PMID 16884295. doi:10.1021/jm0604575
- ↑ Herscovitch M, Comb W, Ennis T, Coleman K, Yong S, Armstead B, Kalaitzidis D, Chandani S, Gilmore TD (fevereiro de 2008). «Intermolecular disulfide bond formation in the NEMO dimer requires Cys54 and Cys347». Biochemical and Biophysical Research Communications. 367 (1): 103–8. PMC 2277332
 . PMID 18164680. doi:10.1016/j.bbrc.2007.12.123
. PMID 18164680. doi:10.1016/j.bbrc.2007.12.123
- ↑ Amoutzias, Grigoris D.; Robertson, David L.; Van de Peer, Yves; Oliver, Stephen G. (1 de maio de 2008). «Choose your partners: dimerization in eukaryotic transcription factors». Trends in Biochemical Sciences. 33 (5): 220–229. ISSN 0968-0004. PMID 18406148. doi:10.1016/j.tibs.2008.02.002
- ↑ Filipiuc, Leontina Elena; Ababei, Daniela Carmen; Alexa-Stratulat, Teodora; Pricope, Cosmin Vasilica; Bild, Veronica; Stefanescu, Raluca; Stanciu, Gabriela Dumitrita; Tamba, Bogdan-Ionel (1 de novembro de 2021). «Major Phytocannabinoids and Their Related Compounds: Should We Only Search for Drugs That Act on Cannabinoid Receptors?». Pharmaceutics. 13 (11). 1823 páginas. ISSN 1999-4923. PMC 8625816
 . PMID 34834237. doi:10.3390/pharmaceutics13111823
. PMID 34834237. doi:10.3390/pharmaceutics13111823
- ↑ Hehir, Michael J.; Murphy, Jennifer E.; Kantrowitz, Evan R. (2000). «Characterization of Heterodimeric Alkaline Phosphatases from Escherichia coli: An Investigation of Intragenic Complementation». Journal of Molecular Biology. 304 (4): 645–656. PMID 11099386. doi:10.1006/jmbi.2000.4230
- ↑ Hjörleifsson, Jens Guðmundur; Ásgeirsson, Bjarni (1 de julho de 2016). «Cold-active alkaline phosphatase is irreversibly transformed into an inactive dimer by low urea concentrations». Biochimica et Biophysica Acta (BBA) - Proteins and Proteomics (7): 755–765. ISSN 1570-9639. doi:10.1016/j.bbapap.2016.03.016. Consultado em 3 de maio de 2025