Coronulidae
Coronulidae
| |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Ocorrência: Placenciano–Recente | |||||||||||||||
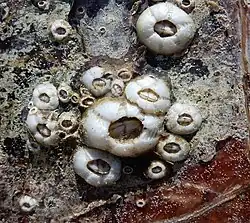
Cryptolepas rhachianecti. | |||||||||||||||
| Classificação científica | |||||||||||||||
| |||||||||||||||
| Gêneros | |||||||||||||||
| |||||||||||||||
As cracas de baleia são espécies de cracas que pertencem à família Coronulidae. Normalmente, elas se prendem às baleias de barbatana e, às vezes, se fixam nas baleias dentadas. As cracas de baleia divergiram há cerca de três milhões de anos.
As cracas de baleia filtram passivamente os alimentos, usando cirros semelhantes a tentáculos, enquanto o hospedeiro nada na água. O arranjo é geralmente considerado comensal, pois é feito sem nenhum custo ou benefício para o hospedeiro. No entanto, algumas baleias podem usar as cracas como armadura protetora ou para infligir mais danos durante a luta, o que tornaria a relação mutualista, em que ambas as partes se beneficiam; como alternativa, algumas espécies podem apenas aumentar o arrasto que o hospedeiro sofre ao nadar, tornando as cracas parasitas.
Após a eclosão, as cracas passam por seis estágios de muda antes de procurar um hospedeiro, sendo levadas a se estabelecer por uma sugestão química da pele do hospedeiro. A craca cria uma carapaça em forma de coroa e, na maioria dos casos, incorpora-se profundamente à pele para obter estabilidade enquanto se desloca em um hospedeiro em movimento rápido. As placas da concha são feitas de carbonato de cálcio e quitina.
As cracas de baleia podem viver por até um ano e geralmente se desprendem ao longo das rotas de migração ou nos locais de parto das baleias. Por esse motivo, os fósseis de cracas de baleia podem ser usados para estudar a distribuição antiga das baleias.
Taxonomia
Evolução
As cracas de baleia podem ter se originado das cracas de tartaruga (Chelonibiidae [en]) - que se prendem a tartarugas, sirênios e caranguejos - como um grupo que mudou sua especialização para baleias de barbatana.[1] As cracas de tartaruga são conhecidas desde antes do início do Terciário, que terminou há 23 milhões de anos (ma), e as cracas de baleia provavelmente divergiram no Plioceno tardio, de 3,5 a 3 ma. Restos de cracas de tartaruga Chelonibia testudinaria do Plioceno da Itália parecem ter sido associados a baleias francas (Eubalaena spp.) e podem representar uma fase de transição; a falta de espécies de cracas concorrentes e a pele mais macia em comparação com a carapaça da tartaruga podem ter levado a uma divergência e dispersão. Como as cracas de baleia são monofiléticas (a família contém um ancestral comum e todos os seus descendentes), essa dispersão só ocorreu com sucesso uma vez.[2] Como as cracas de baleia podem se desprender de seus hospedeiros ao longo das rotas de migração e nos locais de reprodução, seus restos no fundo do mar são usados como indicadores da antiga distribuição das baleias e de seus hábitos migratórios, semelhante à função dos fósseis de vestígios.[1][3][4]
Classificação
As cracas de baleia são uma família de cracas de bolota. A família Coronulidae foi criada pela primeira vez em 1817 pelo biólogo marinho inglês William Elford Leach, e foi colocada na ordem Campylosomata com Balanidae ao lado da ordem Acamptosomata com Cineridea e Pollicipedides, sob a superfamília Coronuloidea.[5] Em 1825, o zoólogo inglês John Edward Gray dividiu Coronulidae em quatro subfamílias: Tubicinella, Polylepas, Platylepas e Astrolepas.[6] Em 1854, Charles Darwin reclassificou as cracas e transferiu todas as cracas sésseis para a família Balanidae, separando-a nas subfamílias Chthamalinae e Balaninae. Ele não tinha certeza se deveria classificar as cracas de baleia na última subfamília ou seguir Leach e Gray e criar a subfamília Coronulinae para incluir as cracas sésseis que se prendem a grandes vertebrados.[7]
Em 1916, o biólogo Henry Augustus Pilsbry diferenciou os cracas de tartaruga das cracas de baleia e os classificou em Chelonibiinae e Coronulinae, respectivamente; ele também reconheceu duas formas de Coronulinae, coronulídeos e platylepádios, com base em diferenças anatômicas e preferências de hospedeiros. Em 1976, a família Coronulidae foi redefinida para incluir Coronulinae, Platylepadinae, Chelonibiinae e Emersoniinae; Coronuloidea foi reorganizado para incluir Coronulidae, Tatraclitidae e Bathylasmatidae. Em 1981, Coronulidae foi reorganizado para incluir as subfamílias Coronulinae, Chelonibiinae e Xenobalaninae.[3] Em 2007, estes foram redefinidos como Coronuloidea, compreendendo três famílias: Coronulidae, Chelonibiidae e Platylepadidae.[8] Em 2021, uma reclassificação das cracas resultou na reintegração dos membros de Platylepadidae à Coronulidae, e Coronulidae deixou de ser agrupada em subfamílias.[9]
De acordo com o World Register of Marine Species (WoRMS), há 35 espécies aceitas de cracas de baleia (da família Coronulidae), 24 das quais existem atualmente. † denota espécies extintas:[10]
Família Coronulidae Leach, 1817
- Gênero Cetolepas Zullo, 1969
- †Cetolepas hertleini Zullo, 1969
- Gênero Cetopirus Ranzani, 1817
- Cetopirus complanatus Mörch, 1852
- †C. fragilis Collareta et al., 2016
- Gênero Chelolepas Ross & Frick, 2007
- Chelolepas cheloniae Monroe & Limpus, 1979
- Gênero Coronula Lamarck, 1802
- Gênero Cryptolepas Dall, 1872
- Cryptolepas rhachianecti Dall, 1872
- †C. murata Zullo, 1961
- Gênero Cylindrolepas Pilsbry, 1916
- Cylindrolepas darwiniana Pilsbry, 1916
- C. sinica Ren, 1980
- Gênero Platylepas Gray, 1825
- Platylepas coriacea Monroe & Limpus, 1979
- P. decorata Darwin, 1854
- P. hexastylos (Fabricius, 1798)
- P. indicus Daniel, 1958
- P. krugeri (Krüger, 1912)
- P. multidecorata Daniel, 1962
- P. ophiophila Lanchester, 1902
- P. wilsoni Ross, 1963
- †P. mediterranea Collareta et al., 2019
- Gênero Stomatolepas Pilsbry, 1910
- Stomatolepas dermochelys Monroe & Limpus, 1979
- S. elegans (Costa, 1838)
- S. muricata Fischer, 1886
- S. pilsbryi Frick, Zardus & Lazo-Wasem, 2010
- S. pulchra Ren, 1980
- S. transversa Nilsson-Cantell, 1930
- Gênero Tubicinella Lamarck, 1802
- Tubicinella cheloniae Monroe & Limpus, 1979
- T. major Lamarck, 1802
- Gênero Xenobalanus Steenstrup, 1852
- Xenobalanus globicipitis Steenstrup, 1852
- Gênero †Emersonius Ross, 1967
- †Emersonius cybosyrinx Ross, 1967
O National Center for Biotechnology Information (NCBI) e o Integrated Taxonomic Information System (ITIS) possuem diferentes classificações para Coronulidae, embora nenhum seja autoritativo como o WoRMS. O NCBI define Coronulidae como contendo Coronula, Cryptolepas, Xenobalanus e os cracas de tartaruga Chelonibia;[11] e o ITIS Coronula, Cryptolepas, Cetopirus, Xenobalanus e Polylepas.[12]
Descrição

Adultos
Todos os cracas de bolota criam uma concha em forma de coroa, com seis a oito placas e um orifício no topo. C. diadema é tipicamente em forma de barril, com a maior parte da concha emergindo da pele, e foi medido no Pacífico norte com 39 a 50 mm de altura. Coronula reginae (que tem tipicamente 13 a 19 mm de altura), Cetopirus (que foi registrado em dois indivíduos com 12 e 28 mm de altura e 53 e 74 mm de diâmetro, respectivamente) e Cryptolepas são achatados e profundamente incrustados na pele.[13] Tubicinella é alto e em forma de tubo com sulcos que podem evitar que a pele rejeite a craca; geralmente excede 50 mm de altura.[8] Xenobalanus tem uma concha em forma de estrela profundamente incrustada na pele e desenvolve um longo pedúnculo (semelhante aos Pedunculata), que pende do hospedeiro;[14][15] Xenobalanus pode ter cerca de 30 mm de tamanho.[16]

O apêndice carnoso que sai do orifício — o "manto apertural" — é mais proeminente do que em outras cracas.[8] Os cirrus, estruturas de alimentação semelhantes a tentáculos que se estendem do orifício, são curtos e grossos, provavelmente permitindo maior estabilidade enquanto estão em um hospedeiro em movimento rápido. As cracas de baleia têm placas operculares reduzidas que apenas parcialmente fecham o orifício no topo, provavelmente porque esses cracas não têm predadores e, portanto, não precisam se defender.[3] As placas, como as das cracas de tartaruga, são feitas de carbonato de cálcio e quitina.[8] Dentro das placas, a craca mole em si é envolto em uma cutícula que é periodicamente substituída.[17] Quando se desprendem do hospedeiro, os cracas de baleia podem deixar marcas redondas,[13] mas Xenobalanus deixa uma cicatriz única em forma de estrela.[1] C. diadema, com base no tamanho das infestações e no número de juvenis presentes ao longo do ano, pode ter uma expectativa de vida de cerca de um ano.[3] Observou-se que C. diadema se desprende em áreas com alto tráfego de baleias, como rotas de migração e áreas de reprodução.[2][4]
Desenvolvimento
Diferentemente de cracas de bolota costeiras, que foram amplamente estudadas, o desenvolvimento de uma craca Coronulidae foi pesquisado pela primeira vez em 2006, com a espécie Coronula diadema coletada da nadadeira de uma baleia-jubarte encalhada. Imediatamente após a eclosão, as larvas náuplio mudaram e, após seis mudas, alcançaram o estágio ciprídeo, o último estágio antes da maturidade. Diferentemente de outras cracas, os estágios II e III do náuplio tinham um par de chifres projetando-se da cabeça, e os olhos no estágio IV eram em forma de crescente. O ciprídeo tinha olhos circulares e, como outras cracas, possuía várias células de óleo na cabeça, que provavelmente atuavam como reservas de alimento, já que os ciprídeos não se alimentam. Os ciprídeos pareciam ser induzidos a se fixar em um substrato por uma pista liberada pela pele da baleia, embora não precisem se fixar na pele. Embora o mecanismo não seja completamente compreendido, as cracas costeiras recebem sinais de fixação de uma certa proteína, então pode ser que as cracas de baleia usem a alfa-2-macroglobulina [en], uma proteína plasmática do sangue comum em vertebrados. Após a fixação, as cracas juvenis formam uma estrutura em forma de anel que se agarra firmemente à pele, crescendo para cima como um cilindro. As placas da parede não se formam inicialmente, embora os juvenis desenvolvam listras. Essa forma cilíndrica é semelhante ao adulto T. major, que se fixa em baleias-francas.[18]
Ecologia

Cirros
Os cirros são usados pelas cracas para capturar partículas de alimento na corrente. As cracas estendem seus cirros em forma de leque, capturam partículas e, em seguida, retraem os cirros de volta à concha para transferir as partículas para a boca. Primeiro, uma membrana — a membrana opercular que protege o craca da água — é aberta e os cirros emergem da concha e se espalham. Na extensão total, três dos seis cirros não se projetam além da membrana. Os cirros então realizam um movimento para a frente, e os cirros longos e a membrana começam a retrair. Eles fazem um movimento para trás e os cirros enrolam-se de volta à concha. Em Cryptolepas, esse processo foi observado como levando de 1,2 a 1,9 segundos; no entanto, os movimentos para a frente e para trás podem ser completamente omitidos, e os cirros podem simplesmente ser estendidos e rapidamente se enrolarem de volta. Cracas jovens têm ciclos mais curtos do que os adultos. Em correntes rápidas, os cirros não se retraem. Cracas terrestres precisam reorientar seus cirros dependendo da direção da corrente; mas, como a corrente flui apenas em uma direção para as cracas de baleia — da cabeça à cauda do hospedeiro — os adultos perderam essa habilidade. No entanto, os cirros têm uma função especial durante a cópula.[19] Nesse momento, a craca que atua como macho (as cracas são hermafroditas) estende completamente seus cirros, e o pênis começa um movimento de busca ao redor de sua circunferência. Após encontrar outra craca, o par inicia uma série de movimentos cirrais intensos que, em Cryptolepas, foi observado como durando cerca de 32 segundos.[19]
Simbiose

Cracas de baleia tipicamente se fixam em baleias-de-barbatana e podem ter uma relação de comensalismo — a craca se beneficia e a baleia não é ajudada nem prejudicada;[1] no entanto, conforme descrito nos parágrafos seguintes, há possíveis vantagens e desvantagens para a baleia. Uma única baleia-jubarte pode carregar até 450 kg de cracas.[20]
Em baleias-francas (Eubalaena spp), uma espécie endêmica de craca, Tubicinella, está incrustada em manchas de pele endurecida e calcificada chamadas calosidades. A distribuição das calosidades e os ciamídeos [en] de cor clara que ocupam as calosidades formam um padrão único para baleias individuais, sendo usado como marcador de identidade por pesquisadores.[21]
Como as cracas requerem que a água flua independentemente sobre eles para filtrar alimentos, as colônias podem seguir a direção das correntes de água produzidas pelo animal em áreas com fluxo moderado.[22] No entanto, Xenobalanus habita exclusivamente os ambientes mais turbulentos para cracas em nadadeiras, barbatanas caudais e nadadeiras dorsais. As larvas de craca podem chegar a esses locais passivamente, sendo depositadas naturalmente por vórtices criados pelo animal, ou podem rastejar para locais mais adequados.[14] Xenobalanus estimula o crescimento de pele calcificada ao seu redor, o que impede que a pele se desprenda e desaloje a craca.[16] Em baleias-de-barbatana, as cracas são frequentemente encontradas em conjunto com piolho-de-baleia.[22] A craca Conchoderma auritum frequentemente se fixa à concha de C. diadema.[13]
Embora as cracas de baleia sejam geralmente consideradas comensais, as calosidades podem ser uma adaptação para evitar que as cracas aumentem o arrasto, concentrando as infestações,[21] e uma infestação pesada pode levar a eczema.[22] Xenobalanus pode crescer mais facilmente em pele doente com um sistema imunológico enfraquecido, e indivíduos mais jovens tendem a ter infestações maiores, presumivelmente porque são menos resistentes;[15] além disso, dado que possui um pedúnculo, aumenta o arrasto sentido pelo hospedeiro e pode ser considerado parasitário nesse sentido.[16] Uma infecção por Cryptolepas em baleia-belugas (Delphinapterus leucas) em cativeiro provocou uma resposta imune pela pele, e as cracas foram ejetadas após algumas semanas.[23] Baleias-cinzentass foram observadas esfregando-se contra o fundo marinho de cascalho para desalojar cracas.[24]

Por outro lado, algumas baleias podem usar cracas como armas ou armaduras protetoras para adicionar força a um golpe em batalhas de acasalamento ou como um dissuasor contra mordidas de orcas (Orcinus orca). Isso tornaria a relação entre cracas de baleia e certas baleias mutualística, na qual ambas as partes se beneficiam. Pode ser que algumas baleias-de-barbatana, no contexto da resposta de luta ou fuga, estejam adaptadas para uma resposta de luta, nomeadamente as baleias-jubarte e baleias-cinzentas (Eschrichtius robustus). Como tal, elas podem ter evoluído para atrair cracas, sacrificando velocidade por dano e defesa. Outras, as Balaenoptera, estão adaptadas para uma resposta de fuga, provavelmente desenvolvendo um mecanismo antincrustação em sua pele para deter infestações, evitando peso desnecessário que dificultaria a velocidade. No entanto, a baleia-da-Groenlândia (Balaena mysticetus), a baleia-franca-do-Atlântico-Norte (Eubalaena glacialis) e a baleia-franca-do-Pacífico (E. japonica), que favorecem respostas de luta, geralmente estão livres de cracas.[20] Pode ser que uma redução na população causada pela caça às baleias tenha restringido sua distribuição e contato com outras baleias, dificultando a capacidade das cracas de infestar outras baleias.[13]
Hospedeiros
C. diadema é comum a abundante na baleia-jubarte (Megaptera novaeangliae), e incomum a rara em outras espécies de baleia. Cryptolepas é abundante na baleia-cinzenta, mas foi registrado na orca, na baleia-beluga e no estômago do peixe-prata Atherinops affinis.[25] Peixes-prata são conhecidos por remover a pele morta e piolhos de baleia frequentemente encontrados em associação com cracas.[24] Tubicinella major foi registrado apenas na baleia-franca-austral.[25][15]
Cetopirus complanatus habita exclusivamente a baleia-franca-austral E. australis. Xenobalanus foi registrado em: baleia-piloto (Globicephala spp.), golfinho-nariz-de-garrafa (Tursiops truncatus), roaz-do-índico (T. aduncus), golfinho-pintado-pantropical (Stenella attenuata), golfinho-riscado, golfinho-rotador (S. longirostris), baleia-bicuda-de-Cuvier (Ziphius cavirostris), franciscana (Pontoporia blainvillei), orca, falsa-orca (Pseudorca crassidens), tucuxi (Sotalia fluviatilis), golfinho-de-dentes-rugosos (Steno bredanensis), golfinho-de-risso (Grampus griseus), orca-pigmeia (Feresa attenuata), golfinho-comum (Delphinus spp.), golfinho-cinzento (Lagenorhynchus obscurus), golfinho-cabeça-de-melão (Peponocephala electra), baleia-cachalote, Neophocaena phocaenoides, toninha-comum (Phocoena phocoena), vaquita (P. sinus), toninha-de-Burmeister (P. spinipinnis), baleia-bicuda-de-True (Mesoplodon mirus), baleia-de-bryde (B. edeni), baleia-azul, baleia-jubarte e algumas outras.[25]
Ver também
Referências
- ↑ a b c d Collareta, A.; Insacco, G.; Reitano, A.; Catanzariti, R.; Bosselaers, M.; Montes, M.; Bianucci, G. (2018). «Fossil whale barnacles from the lower Pleistocene of Sicily shed light on the coeval Mediterranean cetacean fauna». Carnets de Géologie. 18 (2): 9–22. doi:10.4267/2042/65747
 . hdl:11568/957060
. hdl:11568/957060
- ↑ a b Collareta, A.; Bosselaers, M.; Bianucci, G. (2016). «Jumping from turtles to whales: a Pliocene fossil record depicts an ancient dispersal of Chelonibia on mysticetes». Rivista Italiana di Paleontologia e Stratigrafia. 122 (2): 35–44. doi:10.13130/2039-4942/7229
- ↑ a b c d Hayashi, R. (2012). «Atlas of the barnacles on marine vertebrates in Japanese waters including taxonomic review of superfamily Coronuloidea (Cirripedia: Thoracica)». Journal of the Marine Biological Association of the United Kingdom. 92 (1): 107–127. doi:10.1017/S0025315411000737
- ↑ a b Bianucci, G.; Landini, W.; Buckeridge, J. S. J. S. (2006). «Whale barnacles and Neogene cetacean migration routes». New Zealand Journal of Geology and Geophysics. 49 (1): 115–120. doi:10.1080/00288306.2006.9515152

- ↑ Leach, W. E. (1817). «Distribution systématique de la classe des Cirripèdes» [Systemic distribution of the class Cirripedia]. Journal de Physique, de Chimie, d'Histoire Naturelle Avec des Planches en Taille-douce (em francês): 67–69
- ↑ Gray, J. E. (1825). «A synopsis of the genera of Cirripedes arranged in natural families, with a description of some new species». Annals of Philosophy. 10: 105
- ↑ Darwin, C. (1854). A monograph on the sub-class Cirripedia, with figures of all the species. [S.l.]: The Ray Society. pp. 153–154
- ↑ a b c d Ross, A.; Frick, M. (2007). «From Hendrickson (1958) to Monroe & Limpus (1979) and beyond: an evaluation of the turtle barnacle Tubicinella cheloniae». Marine Turtle Newsletter. 118: 2–5. Consultado em 2 de setembro de 2025
- ↑ Chan, Benny K. K.; Dreyer, Niklas; Gale, Andy S.; Glenner, Henrik; et al. (2021). «The evolutionary diversity of barnacles, with an updated classification of fossil and living forms». Zoological Journal of the Linnean Society. 193 (3): 789–846. doi:10.1093/zoolinnean/zlaa160
 . hdl:11250/2990967
. hdl:11250/2990967
- ↑ Coronulidae. In: WoRMS 2013. World Register of Marine Species.
- ↑ «Coronulidae» (em inglês). NCBI. Consultado em 2 de setembro de 2025
- ↑ «Coronulidae» (em inglês). ITIS (www.itis.gov). Consultado em 2 de setembro de 2025
- ↑ a b c d Scarff, J. E. (1986). «Occurrence of the barnacles Coronula diadema, C. reginae and Cetopirus complanatus (Cirripedia) on right whales» (PDF). The Scientific Reports of the Whales Research Institute: 131–134. Consultado em 2 de setembro de 2025
- ↑ a b Carrillo, J. M.; Overstreet, R. M.; Raga, J. A.; Aznar, F. J. (2015). «Living on the edge: settlement patterns by the symbiotic barnacle Xenobalanus globicipitis on small cetaceans» 6 ed. PLOS ONE. 10: e0127367. Bibcode:2015PLoSO..1027367C. PMC 4470508
 . PMID 26083019. doi:10.1371/journal.pone.0127367
. PMID 26083019. doi:10.1371/journal.pone.0127367
- ↑ a b c Fertl, D.; Newman, W. A. (2018). «Barnacles». In: Würsig, B.; Thewissen, J. G. M.; Kovacs, Kit. Encyclopedia of Marine Mammals 3 ed. [S.l.]: Academic Press. pp. 75–78. ISBN 978-0-12-804381-3. doi:10.1016/B978-0-12-804327-1.00060-1
- ↑ a b c Pugliese, M. C.; Böttger, S. A.; Fish, F. E. (2012). «Barnacle bonding: morphology of attachment of Xenobalanus globicipitis to its host Tursiops truncatus» 4 ed. Journal of Morphology. 273: 453–459. PMID 22253021. doi:10.1002/jmor.20006
- ↑ Ruppert, Edward E.; Fox, Richard, S.; Barnes, Robert D. (2004). Invertebrate Zoology, 7th edition. [S.l.]: Cengage Learning. 683 páginas. ISBN 978-81-315-0104-7
- ↑ Nogata, Yasuyuki; Matsumura, Kiyotaka (2006). «Larval development and settlement of a whale barnacle» 1 ed. Biology Letters. 2: 92–93. PMC 1617185
 . PMID 17148335. doi:10.1098/rsbl.2005.0409
. PMID 17148335. doi:10.1098/rsbl.2005.0409
- ↑ a b Achituv, Y. (1998). «Cirral activity in the whale barnacle Cryptolepas Rhachianechi» 4 ed. Journal of the Marine Biological Association of the United Kingdom. 78: 1203–1213. doi:10.1017/s0025315400044428
- ↑ a b Ford, J. K. B.; Reeves, R. R. (2008). «Fight or flight: antipredator strategies of baleen whales» 1 ed. Mammalian Review. 38: 50–86. CiteSeerX 10.1.1.573.6671
 . doi:10.1111/j.1365-2907.2008.00118.x
. doi:10.1111/j.1365-2907.2008.00118.x
- ↑ a b Goddard, J.; Thompson, P. (2010). Mammal anatomy: an illustrated guide. [S.l.]: Marshall Cavendish Corporation. p. 86. ISBN 978-0-7614-7882-9. Consultado em 2 de setembro de 2025
- ↑ a b c Hermosilla, C.; Silva, L. M. R.; Prieto, R.; Kleinertz, S.; Taubert, A.; Silva, M. A. (2015). «Endo- and ectoparasites of large whales (Cetartiodactyla: Balaenopteridae, Physeteridae): Overcoming difficulties in obtaining appropriate samples by non- and minimally-invasive methods» 3 ed. International Journal for Parasitology: Parasites and Wildlife. 4: 414–420. PMC 4699982
 . PMID 26835249. doi:10.1016/j.ijppaw.2015.11.002
. PMID 26835249. doi:10.1016/j.ijppaw.2015.11.002
- ↑ Ridgeway, S. H.; Lindner, E.; Mahoney, K. A.; Newman, W. A. (1997). «Gray whale barnacles (Cryptolepas rhachianecti) infested white whales that were being held in San Diego Bay.» 2 ed. Bulletin of Marine Science. 61: 377–385. Consultado em 2 de setembro de 2025
- ↑ a b Busch, R. (1998). Gray whales: wandering giants. [S.l.]: Heritage House Publishing Co. pp. 61–62. ISBN 978-1-55143-114-7. Consultado em 2 de setembro de 2025
- ↑ a b c Hayashi, R. (2013). «A checklist of turtle and whale barnacles (Cirripedia: Thoracica: Coronuloidea)» 1 ed. Journal of the Marine Biological Association of the United Kingdom. 93: 149–155. doi:10.1017/S0025315412000847