Produção primária marinha

A produção primária marinha é a síntese química no oceano de compostos orgânicos a partir de dióxido de carbono atmosférico ou dissolvido. Esse processo ocorre principalmente por meio da fotossíntese, que utiliza a luz solar como fonte de energia, mas também por quimiossíntese, que utiliza a oxidação ou redução de compostos químicos inorgânicos como fonte de energia. Quase toda a vida na Terra depende direta ou indiretamente da produção primária. Os organismos responsáveis pela produção primária são chamados de produtores primários ou autotróficos.
A maior parte da produção primária marinha é gerada por uma coleção diversa de micro-organismos marinhos [en] chamados algas e cianobactérias. Juntos, esses formam os principais produtores primários na base da cadeia alimentar oceânica e produzem metade do oxigênio do mundo. Os produtores primários marinhos sustentam quase toda a vida animal marinha, gerando praticamente todo o oxigênio e alimento que os animais marinhos necessitam para sobreviver. Alguns produtores primários marinhos também são engenheiros de ecossistemas [en], que modificam o ambiente e fornecem habitats para outras formas de vida marinha.
A produção primária no oceano pode ser contrastada com a produção primária em terra. Globalmente, o oceano e a terra produzem aproximadamente a mesma quantidade de produção primária, mas no oceano ela vem principalmente de cianobactérias e algas, enquanto em terra provém principalmente de plantas vasculares.
As algas marinhas incluem as microalgas, amplamente invisíveis e frequentemente unicelulares, que, junto com as cianobactérias, formam o fitoplâncton oceânico, além das macroalgas, mais visíveis e complexas, comumente chamadas de algas marinhas. As algas marinhas são encontradas em áreas costeiras, vivendo no fundo das plataformas continentais e sendo arrastadas para as zonas entremarés. Algumas algas marinhas derivam com o plâncton nas águas superficiais iluminadas pelo sol (zona epipelágica) do oceano aberto. No período Siluriano, alguns fitoplanctons evoluíram para algas vermelhas, algas castanhas e algas verdes. Essas algas então invadiram a terra e começaram a evoluir para as plantas terrestres que conhecemos hoje. Mais tarde, no Cretáceo, algumas dessas plantas terrestres retornaram ao mar como manguezais e ervas marinhas. Estas são encontradas ao longo das costas em regiões entremarés e nas águas salobras de estuários. Além disso, algumas ervas marinhas, como as algas marinhas, podem ser encontradas a profundidades de até 50 m em fundos moles e duros da plataforma continental.
Produtores primários marinhos
Os produtores primários são organismos autotróficos que produzem seu próprio alimento em vez de consumir outros organismos. Isso significa que os produtores primários são o ponto de partida na cadeia alimentar para organismos heterotróficos que consomem outros organismos. Alguns produtores primários marinhos são bactérias e arqueas especializadas que são quimiotróficas, produzindo seu próprio alimento ao se reunir em torno de fontes hidrotermais e emanações frias e utilizando quimiossíntese. No entanto, a maior parte da produção primária marinha vem de organismos que utilizam a fotossíntese com o dióxido de carbono dissolvido na água. Esse processo usa energia da luz solar para converter água e dióxido de carbono[4]:186–187 em açúcares que podem ser usados tanto como fonte de energia química quanto como moléculas orgânicas utilizadas nos componentes estruturais das células.[4]:1242 Os produtores primários marinhos são importantes porque sustentam quase toda a vida animal marinha, gerando a maior parte do oxigênio e do alimento que fornecem aos outros organismos a energia química necessária para sua existência.
Os principais produtores primários marinhos são cianobactérias, algas e plantas marinhas. O oxigênio liberado como subproduto da fotossíntese é necessário para quase todos os seres vivos realizarem a respiração celular. Além disso, os produtores primários influenciam os ciclos globais do carbono e da água. Eles estabilizam áreas costeiras e podem fornecer habitats para animais marinhos. O termo divisão tem sido tradicionalmente usado em vez de filo ao discutir produtores primários, embora o Código Internacional de Nomenclatura para Algas, Fungos e Plantas agora aceite os termos como equivalentes.[5]
Em uma inversão do padrão em terra, nos oceanos, quase toda a fotossíntese é realizada por algas e cianobactérias, com uma pequena fração contribuída por plantas vasculares terrestres e outros grupos. As algas abrangem uma gama diversificada de organismos, desde células flutuantes individuais até algas marinhas fixas. Elas incluem organismos fotoautotróficos de vários grupos. Eubactérias são importantes fotossintetizantes em ecossistemas oceânicos e terrestres, e enquanto algumas arqueias são fototróficas, nenhuma é conhecida por utilizar fotossíntese que libera oxigênio.[6] Vários eucariotos são contribuintes significativos para a produção primária no oceano, incluindo algas verdes, algas castanhas e algas vermelhas, além de um grupo diversificado de seres unicelulares. Plantas vasculares também estão representadas no oceano por grupos como as ervas marinhas.
Diferentemente dos ecossistemas terrestres, a maioria da produção primária no oceano é realizada por organismos microscópicos de vida livre chamados fitoplâncton. Estima-se que metade do oxigênio do mundo seja produzida pelo fitoplâncton.[7][8] Autotróficos maiores, como ervas marinhas e macroalgas, são geralmente confinados a zonas litorâneas e águas rasas adjacentes, onde podem se fixar ao substrato subjacente, mas ainda estar dentro da zona fótica. Há exceções, como as algas castanhas do gênero Sargassum, mas a grande maioria da produção de flutuação livre ocorre em organismos microscópicos.
Os fatores que limitam a produção primária no oceano também são muito diferentes daqueles em terra. A disponibilidade de água, obviamente, não é um problema (embora sua salinidade possa ser). Da mesma forma, a temperatura, embora afete as taxas metabólicas, varia menos amplamente no oceano do que em terra, porque a capacidade térmica da água do mar amortece as mudanças de temperatura, e a formação de gelo marinho a isola em temperaturas mais baixas. No entanto, a disponibilidade de luz, a fonte de energia para a fotossíntese, e nutrientes minerais, os blocos de construção para o crescimento, desempenham papéis cruciais na regulação da produção primária no oceano.[9] Modelos de sistemas terrestres disponíveis sugerem que mudanças biogeoquímicas contínuas no oceano podem desencadear reduções na produção primária líquida (PPL) oceânica entre 3% e 10% dos valores atuais, dependendo do cenário de emissões.[10]
Em 2020, pesquisadores relataram que medições das últimas duas décadas da produção primária no Oceano Ártico mostram um aumento de quase 60% devido a maiores concentrações de fitoplâncton. Eles hipotetizam que novos nutrientes estão fluindo de outros oceanos e sugerem que isso significa que o Oceano Ártico pode ser capaz de suportar uma produção em níveis tróficos mais altos e uma fixação de carbono adicional no futuro.[11][12]
Cianobactérias
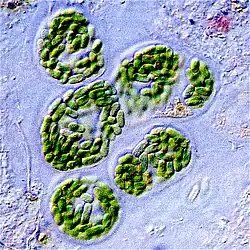
As cianobactérias são um filo (divisão) de bactérias, variando de unicelulares a filamentosas e incluindo espécies coloniais, que fixam carbono inorgânico em compostos orgânicos de carbono. Elas são encontradas em quase todos os lugares na Terra: em solos úmidos, em ambientes de água doce e marinhos, e até em rochas antárticas.[19] Em particular, algumas espécies ocorrem como células flutuantes no oceano e, como tal, estavam entre os primeiros fitoplanctons. Essas bactérias funcionam como algas, pois podem processar nitrogênio da atmosfera quando não há nitrogênio no oceano.
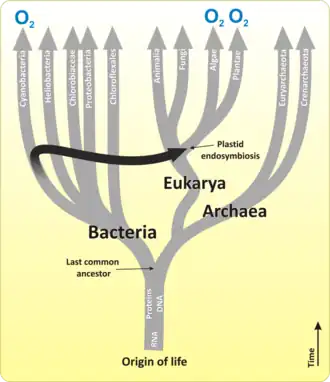
Os primeiros produtores primários que usaram a fotossíntese foram cianobactérias oceânicas há cerca de 2,3 bilhões de anos.[20][21] A liberação de oxigênio molecular pelas cianobactérias como subproduto da fotossíntese induziu mudanças globais no ambiente da Terra. Como o oxigênio era tóxico para a maioria da vida na Terra na época, isso levou à quase extinção de organismos intolerantes ao oxigênio, uma mudança dramática que redirecionou a evolução das principais espécies de animais e plantas.[22]
.jpg)
A pequena cianobactéria marinha Prochlorococcus, descoberta em 1986, forma hoje parte da base da cadeia alimentar oceânica e é responsável por mais da metade da fotossíntese do oceano aberto[23] e por cerca de 20% do oxigênio na atmosfera terrestre.[24] É possivelmente o gênero mais abundante na Terra: um único mililitro de água superficial do mar pode conter 100.000 células ou mais.[25]
Originalmente, os biólogos pensavam que as cianobactérias eram algas e as chamavam de "algas verde-azuladas". A visão mais recente é que as cianobactérias são bactérias e, portanto, não pertencem ao mesmo reino biológico que as algas. A maioria das autoridades exclui todos os procariotos, e portanto as cianobactérias, da definição de algas.[26][27]
Pigmentos biológicos
Pigmentos biológicos são qualquer material colorido em células de plantas ou animais. Todos os pigmentos biológicos absorvem seletivamente certos comprimentos de onda da luz enquanto refletem outros.[28][29] A função primária dos pigmentos nas plantas é a fotossíntese, que utiliza o pigmento verde clorofila e vários pigmentos coloridos que absorvem o máximo possível de energia luminosa. A clorofila é o pigmento primário nas plantas; é uma clorina [en] que absorve comprimentos de onda amarelos e azuis da luz enquanto reflete o verde. É a presença e a abundância da clorofila que dá às plantas sua cor verde. As algas verdes e as plantas possuem duas formas desse pigmento: clorofila a e clorofila b. As grandes algas da ordem Laminariales, diatomáceas e outros heterocontos fotossintéticos contêm clorofila c em vez de b, enquanto as algas vermelhas possuem apenas clorofila a. Todas as clorofilas servem como o principal meio para as plantas interceptarem a luz para "alimentar" a fotossíntese.
Cloroplastos
.jpg)

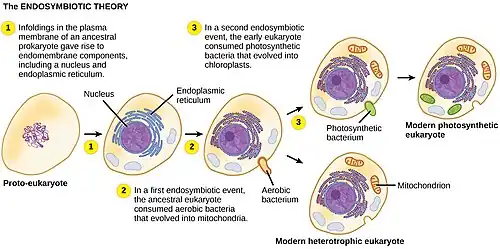
Os cloroplastos (do grego chloros, verde, e plastes, "o que forma"[31]) são organelas que realizam a fotossíntese, onde o pigmento fotossintético clorofila captura a energia da luz solar, converte-a e armazena-a em moléculas de armazenamento de energia, enquanto libera oxigênio da água em células de plantas e algas. Eles então utilizam a energia armazenada para produzir moléculas orgânicas a partir de dióxido de carbono em um processo conhecido como ciclo de Calvin.
Um cloroplasto é um tipo de organela conhecido como plastídeo, caracterizado por suas duas membranas e uma alta concentração de clorofila. Eles são altamente dinâmicos — circulam e são movidos dentro das células vegetais, e ocasionalmente se dividem em dois para se reproduzir. Seu comportamento é fortemente influenciado por fatores ambientais, como a cor e a intensidade da luz. Cloroplastos, assim como mitocôndrias, contêm seu próprio DNA, que se acredita ser herdado de seu ancestral — uma cianobactéria fotossintética que foi "engolida" por uma célula eucariótica inicial.[32] Cloroplastos não podem ser produzidos pela célula vegetal e devem ser herdados por cada célula filha durante a divisão celular.
A maioria dos cloroplastos provavelmente pode ser rastreada até um único evento endossimbiótico, quando uma cianobactéria foi engolida por um eucarioto. Apesar disso, cloroplastos podem ser encontrados em um conjunto extremamente amplo de organismos, alguns nem mesmo diretamente relacionados entre si — uma consequência de muitos eventos endossimbióticos secundários e até terciários.
Rodopsina microbiana
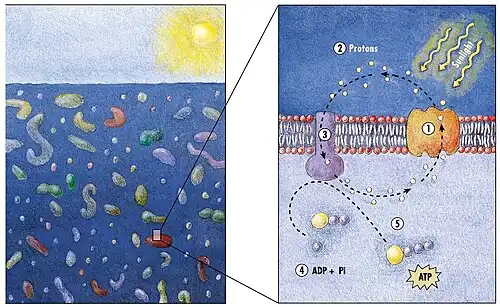

O metabolismo fototrófico depende de um dos três pigmentos conversores de energia: clorofila, bacterioclorofila e retinal. O retinal é o cromóforo encontrado em rodopsinas. A importância da clorofila na conversão de energia luminosa é conhecida há décadas, mas a fototrofia baseada em pigmentos de retinal está apenas começando a ser estudada.[35]
.jpg)
Em 2000, uma equipe de microbiologistas liderada por Edward DeLong fez uma descoberta crucial para a compreensão dos ciclos marinhos de carbono e energia. Eles descobriram um gene em várias espécies de bactérias[37][38] responsável pela produção da proteína rodopsina, até então desconhecida em bactérias. Essas proteínas, encontradas nas membranas celulares, são capazes de converter energia luminosa em energia bioquímica devido a uma mudança na configuração da molécula de rodopsina quando atingida pela luz solar, causando o bombeamento de um próton de dentro para fora e um fluxo subsequente que gera energia.[39] As rodopsinas semelhantes às de arqueias foram posteriormente encontradas em diferentes táxons, incluindo protistas, bactérias e arqueias, embora sejam raras em organismos multicelulares complexos.[37][40][41]
Pesquisas em 2019 mostram que essas "bactérias captadoras de sol" são mais disseminadas do que se pensava anteriormente e podem alterar como os oceanos são afetados pelo aquecimento global. "As descobertas rompem com a interpretação tradicional da ecologia marinha encontrada em livros didáticos, que afirma que quase toda a luz solar no oceano é capturada pela clorofila nas algas. Em vez disso, bactérias equipadas com rodopsina funcionam como carros híbridos, alimentadas por matéria orgânica quando disponível — como a maioria das bactérias — e pela luz solar quando os nutrientes são escassos."[42][35]
Há uma conjectura astrobiológica chamada "hipótese da Terra roxa", que supõe que as formas de vida originais na Terra eram baseadas em retinal em vez de clorofila, o que teria feito a Terra parecer roxa em vez de verde.[43][44]
Algas marinhas
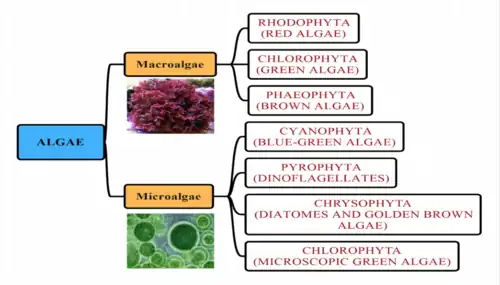
Algas é um termo informal para uma coleção ampla e diversa de organismos eucarióticos fotossintéticos que não são necessariamente próximos em termos evolutivos e, portanto, são polifiléticos. Diferentemente das plantas superiores, as algas não possuem raízes, caules ou folhas.
Grupos de algas
As algas marinhas têm sido tradicionalmente classificadas em grupos como: algas verdes, algas vermelhas, algas castanhas, diatomáceas, cocolitoforídeos e dinoflagelados.
Algas verdes
As algas verdes vivem a maior parte de suas vidas como células únicas ou são filamentosas, enquanto outras formam colônias compostas por longas cadeias de células ou são algas marinhas macroscópicas altamente diferenciadas. Elas formam um grupo informal contendo cerca de 8.000 espécies reconhecidas.[46]
Algas vermelhas
-
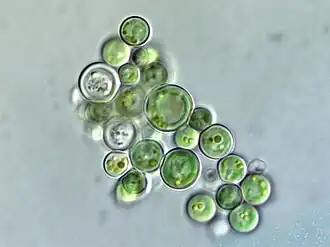 Colônia de Cyanidiophyceae, uma classe de algas vermelhas unicelulares.
Colônia de Cyanidiophyceae, uma classe de algas vermelhas unicelulares. -
A alga marinha Porphyra umbilicalis.
As algas vermelhas modernas são majoritariamente multicelulares com células diferenciadas e incluem muitas macroalgas notáveis.[47][48] Como algas coralinas, elas desempenham um papel importante na ecologia dos recifes de coral. Elas formam um filo contendo cerca de 7.000 espécies reconhecidas.[47]
Algas castanhas
As algas castanhas são majoritariamente multicelulares e também incluem muitas macroalgas, incluindo florestas de algas Laminariales. Elas formam uma classe contendo cerca de 2.000 espécies reconhecidas.[49]

Diatomáceas
No total, cerca de 45% da produção primária nos oceanos é feita por diatomáceas.[50]
Cocolitoforídeos
Os cocolitoforídeos são quase exclusivamente marinhos e encontrados em grande número na zona iluminada do oceano. Eles possuem placas de carbonato de cálcio de função incerta chamadas "cocolitos", que são importantes micrófósseis.
-
_Various_diatoms.jpg) Diatomáceas são um dos tipos mais comuns de fitoplâncton.
Diatomáceas são um dos tipos mais comuns de fitoplâncton. -
![Elas são um grupo importante de algas, gerando cerca de 20% da produção de oxigênio mundial.[51]](./_assets_/0c70a452f799bfe840676ee341124611/Diatoms_through_the_microscope.jpg) Elas são um grupo importante de algas, gerando cerca de 20% da produção de oxigênio mundial.[51]
Elas são um grupo importante de algas, gerando cerca de 20% da produção de oxigênio mundial.[51] -
![Diatomáceas possuem paredes celulares de vidro chamadas frústulas, feitas de sílica.[52]](./_assets_/0c70a452f799bfe840676ee341124611/Diatom_algae_Amphora_sp.jpg)
-
![Diatomáceas ligadas em uma cadeia colonial.[53]](./_assets_/0c70a452f799bfe840676ee341124611/Phytoplankton_in_the_form_of_a_diatom_chain.jpg) Diatomáceas ligadas em uma cadeia colonial.[53]
Diatomáceas ligadas em uma cadeia colonial.[53]
Os cocolitoforídeos são de interesse para estudos sobre mudanças climáticas globais, pois, com o aumento da acidez oceânica, seus cocolitos podem se tornar ainda mais importantes como sumidouro de carbono.[54]
-
 A abundante espécie Emiliania huxleyi.
A abundante espécie Emiliania huxleyi. -
 Floração de E. huxleyi no sul da Inglaterra.
Floração de E. huxleyi no sul da Inglaterra.
A espécie mais abundante de cocolitoforídeo, Emiliania huxleyi, é um componente ubíquo da base planctônica nas teias alimentares marinhas.[55] Estratégias de manejo estão sendo empregadas para prevenir florações de cocolitoforídeos relacionadas à eutrofização, pois essas florações levam a uma diminuição do fluxo de nutrientes para níveis mais profundos do oceano.[56]
Dinoflagelados
-
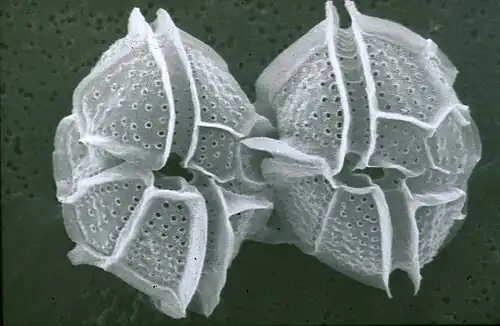 Dinoflagelados.
Dinoflagelados. -
![Karenia brevis produz marés vermelhas altamente tóxicas para humanos.[57]](./_assets_/0c70a452f799bfe840676ee341124611/Karenia_brevis.jpg) Karenia brevis produz marés vermelhas altamente tóxicas para humanos.[57]
Karenia brevis produz marés vermelhas altamente tóxicas para humanos.[57] -
_by_Noctiluca_in_Nagasaki.jpg)
Algas mixotróficas
-
 Diplonemídeos podem ser abundantes nos oceanos mundiais.
Diplonemídeos podem ser abundantes nos oceanos mundiais.
Tradicionalmente, a filogenia de micro-organismos, como os grupos de algas discutidos acima, era inferida e sua taxonomia estabelecida com base em estudos de morfologia. No entanto, avanços na filogenética molecular permitiram estabelecer as relações evolutivas das espécies por meio da análise de suas sequências de DNA e proteínas.[58] Muitos táxons, incluindo os grupos de algas discutidos acima, estão em processo de reclassificação ou redefinição usando filogenética molecular. Desenvolvimentos recentes em sequenciamento molecular permitiram a recuperação de genomas diretamente de amostras ambientais, evitando a necessidade de cultivo. Isso levou, por exemplo, a uma rápida expansão no conhecimento da abundância e diversidade de micro-organismos marinhos. Técnicas moleculares, como metagenômica resolvida por genoma e genômica de célula única, estão sendo usadas em combinação com técnicas de alto rendimento.
Entre 2009 e 2013, a expedição "Tara Oceans" percorreu os oceanos do mundo coletando plâncton e analisando-o com técnicas moleculares contemporâneas. Eles encontraram uma vasta gama de algas fotossintéticas e mixotróficas previamente desconhecidas.[59] Entre suas descobertas estavam os diplonemídeos [en]. Esses organismos são geralmente incolores e de forma oblonga, com cerca de 20 μm de comprimento e dois flagelos.[60] Evidências de código de barras de DNA sugerem que os diplonemídeos podem estar entre os grupos de eucariotos marinhos mais abundantes e ricos em espécies.[61][62]
Por tamanho
As algas podem ser classificadas por tamanho como microalgas ou macroalgas.
Microalgas
As microalgas são os tipos microscópicos de algas, invisíveis a olho nu. Elas são majoritariamente espécies unicelulares que existem individualmente ou em cadeias ou grupos, embora algumas sejam multicelulares. As microalgas são componentes importantes dos protistas marinhos, bem como do fitoplâncton marinho. Elas são muito diversas. Estima-se que existam entre 200.000 e 800.000 espécies, das quais cerca de 50.000 foram descritas.[63] Dependendo da espécie, seus tamanhos variam de alguns micrômetros (μm) a algumas centenas de micrômetros. Elas são especialmente adaptadas a um ambiente dominado por forças viscosas.
- Algumas microalgas
-
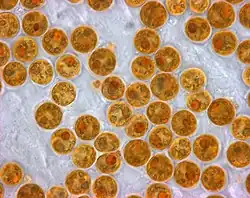 Zooxantelas são algas fotossintéticas que vivem dentro de hospedeiros como corais.
Zooxantelas são algas fotossintéticas que vivem dentro de hospedeiros como corais. -
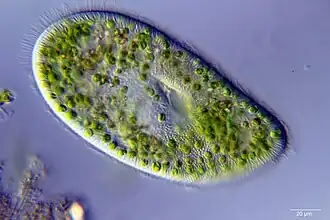
-
_(cropped).jpg) Euglena mutabilis, um flagelado fotossintético.
Euglena mutabilis, um flagelado fotossintético.
Macroalgas

As macroalgas são os tipos maiores, multicelulares e mais visíveis de algas, comumente chamadas de algas marinhas. Essas algas geralmente crescem em águas costeiras rasas, onde estão ancoradas ao fundo do mar por uma estrutura parecida com raízes. Algas marinhas que se soltam podem ser levadas para as praias. As algas do grupo Laminariales, conhecidas no inglês como "Kelp", são grandes algas castanhas que formam florestas subaquáticas, cobrindo cerca de 25% das costas mundiais.[64] Elas estão entre os ecossistemas mais produtivos e dinâmicos da Terra.[65] Algumas algas do gênero Sargassum são planctônicas (flutuantes livres) e formam derivações flutuantes.[66] Assim como as microalgas, as macroalgas (algas marinhas) são tecnicamente protistas marinhos, pois não são plantas verdadeiras.

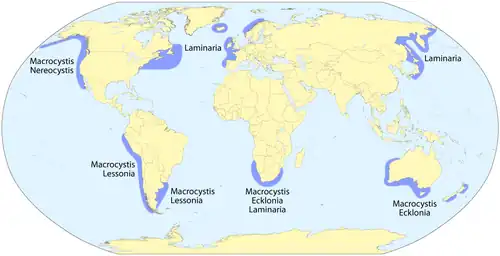
- Algumas macroalgas
-
 Macrocystis,uma alga gigante, é tecnicamente um protista, pois não é uma planta verdadeira, mas é multicelular e pode crescer até 50 m.
Macrocystis,uma alga gigante, é tecnicamente um protista, pois não é uma planta verdadeira, mas é multicelular e pode crescer até 50 m. -
Sargassum é uma alga castanha com bexigas de ar que ajudam na flutuação.
-
 Peixes-sargaço são camuflados para viver entre algas Sargassum flutuantes.
Peixes-sargaço são camuflados para viver entre algas Sargassum flutuantes. -
Alga unicelular Valonia ventricosa vive em zonas entremarés e pode ter 4 cm de diâmetro.[67]
Evolução das plantas terrestres
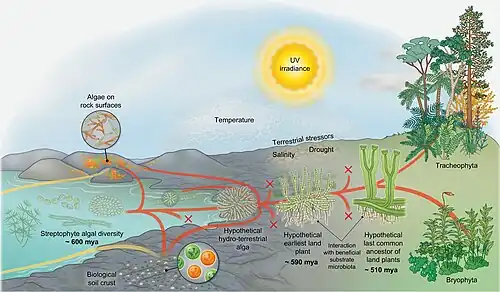
O diagrama à direita mostra um cenário evolutivo para a conquista da terra por estreptófitas.[68] As algas estreptófitas incluem todas as algas verdes e são os únicos eucariotos fotossintéticos dos quais a flora terrestre macroscópica evoluiu (linhas vermelhas do diagrama). Apesar disso, ao longo da evolução, algas de várias outras linhagens colonizaram a terra (linhas amarelas) — mas também as algas estreptófitas fizeram a transição do ambiente úmido para o seco de forma contínua e independente (convergência de vermelho e amarelo). Ao longo da história, numerosas linhagens tornaram-se extintas (marcados por X).
Algas terrestres de diversas afiliações taxonômicas habitam superfícies rochosas e formam a crosta biológica do solo. No entanto, da diversidade das algas estreptófitas parafiléticas, surgiu um organismo cujos descendentes eventualmente conquistaram a terra em escala global: provavelmente uma alga filamentosa ramificada — ou até mesmo parenquimática — que formava estruturas rizoicas e enfrentava dessecação ocasionalmente. Dessa "alga hipotética hidroterrestre", surgiram as linhagens de Zygnematophyceae e embriófitas (plantas terrestres).[68] No início desse processo, a trajetória que levou às embriófitas foi representada pelas — agora extintas — primeiras plantas terrestres.[70]
As primeiras plantas terrestres provavelmente interagiram com substratos benéficos de microbiota que as ajudaram a obter nutrientes do substrato. Além disso, as primeiras plantas terrestres tiveram que superar uma série de estressores terrestres (incluindo luz ultravioleta e irradiância fotossinteticamente ativa, seca, mudanças drásticas de temperatura, etc.). Elas tiveram sucesso porque possuíam o conjunto certo de características — uma mistura de adaptações selecionadas em seus ancestrais de algas hidroterrestres, exaptações e o potencial para co-opção de um conjunto fortuito de genes e vias.[68]
Durante o curso da evolução, alguns membros das populações das primeiras plantas terrestres adquiriram características adaptativas em ambientes terrestres (como alguma forma de condução de água, estruturas semelhantes a estômatos, embriões, etc.); eventualmente, o "ancestral comum mais recente hipotético das plantas terrestres" surgiu. Deste ancestral, evoluíram as briófitas e traqueófitas existentes. Embora o repertório exato de características do ancestral comum mais recente hipotético das plantas terrestres seja incerto, ele certamente incluiu propriedades de plantas vasculares e não vasculares. Também é certo que o ancestral comum mais recente das plantas terrestres possuía características de ancestralidade algal.[68]
Plantas marinhas
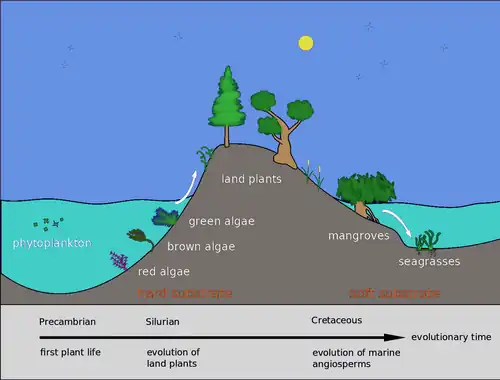
No período Siluriano, alguns fitoplanctons evoluíram para algas vermelhas, castanhas e verdes. As algas verdes então invadiram a terra e começaram a evoluir para as plantas terrestres que conhecemos hoje. Mais tarde, no Cretáceo, algumas dessas plantas terrestres retornaram ao mar como manguezais e ervas marinhas.[71]
A vida vegetal pode prosperar nas águas salobras de estuários, onde manguezais e capins Ammophila ou Spartina podem crescer. Plantas com flores crescem em águas rasas arenosas na forma de pradarias de ervas marinhas,[72] os manguezais alinham a costa em regiões tropicais e subtropicais[73] e plantas tolerantes ao sal prosperam em sapais regularmente inundados.[74] Todos esses habitats são capazes de sequestrar grandes quantidades de carbono e suportar uma gama biodiversa de vida animal maior e menor.[75] As plantas marinhas podem ser encontradas em zonas entremarés e águas rasas, como ervas marinhas, Zostera e Thalassia. Essas plantas adaptaram-se à alta salinidade do ambiente oceânico.
A luz só consegue penetrar os primeiros 200 m da superfície do mar, sendo esta a única parte onde as plantas podem crescer.[76] As camadas superficiais frequentemente carecem de compostos nitrogenados biologicamente ativos. O ciclo do nitrogênio marinho consiste em transformações microbianas complexas que incluem a fixação de nitrogênio, sua assimilação, nitrificação, anammox e desnitrificação.[77] Alguns desses processos ocorrem em águas profundas, de modo que onde há ressurgência de águas frias, e também perto de estuários onde nutrientes de origem terrestre estão presentes, o crescimento vegetal é maior. Isso significa que as áreas mais produtivas, ricas em plâncton e, portanto, também em peixes, são principalmente costeiras.[78]
Manguezais
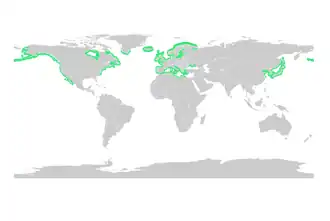
Os manguezais fornecem habitats de berçário importantes para a vida marinha, atuando como locais de esconderijo e forrageamento para formas larvais e juvenis de peixes maiores e invertebrados. Com base em dados de satélite, a área total mundial de florestas de mangue foi estimada em 2010 como 134.257 km².[79][80]
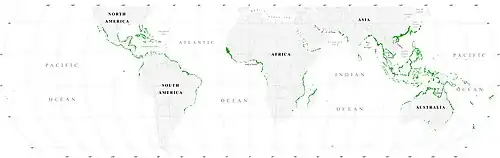
Ervas marinhas
]
Assim como os manguezais, as ervas marinhas fornecem habitats de berçário importantes para formas larvais e juvenis de peixes maiores e invertebrados. A área total mundial de pradarias de ervas marinhas é mais difícil de determinar do que as
florestas de manguezal, mas foi estimada conservadoramente em 2003 como 177.000 km².[81]
-

-
![Dragões-marinhos camuflados para parecerem algas marinhas flutuantes vivem em florestas de algas e pradarias de ervas marinhas.[82]](./_assets_/0c70a452f799bfe840676ee341124611/Leafy_Sea_Dragon_SA.jpg) Dragões-marinhos camuflados para parecerem algas marinhas flutuantes vivem em florestas de algas e pradarias de ervas marinhas.[82]
Dragões-marinhos camuflados para parecerem algas marinhas flutuantes vivem em florestas de algas e pradarias de ervas marinhas.[82]
Estequiometria
| Como a multicelularidade evoluiu? – Jordana ao Microcosmos (em inglês) | |
A estequiometria (medição de reagentes químicos e produtos) da produção primária no oceano superficial desempenha um papel crucial na ciclagem de elementos no oceano [en] global. A proporção entre os elementos carbono (C), nitrogênio (N) e fósforo (P) na matéria orgânica exportada, expressa em termos da razão C:N:P, ajuda a determinar quanto carbono atmosférico é sequestrado no oceano profundo em relação à disponibilidade de nutrientes limitantes.[83]
Em escala de tempo geológico, a razão N:P reflete a disponibilidade relativa de nitrato em relação ao fosfato, ambos fornecidos externamente da atmosfera por fixação de nitrogênio e/ou dos continentes por suprimento fluvial, e perdidos por desnitrificação e soterramento.[84][85][86][87] Em escalas de tempo mais curtas, a estequiometria média da matéria orgânica particulada [en] exportada reflete a estequiometria elementar do fitoplâncton,[88][89][90] com influências adicionais da diversidade biológica e do processamento secundário de matéria orgânica por zooplâncton e bactérias heterótrofas. Diante das mudanças globais, entender e quantificar os mecanismos que levam à variabilidade nas razões C:N:P é crucial para uma projeção precisa das futuras mudanças climáticas.[83]

Uma questão fundamental não resolvida é o que determina o C:N:P de fitoplanctons individuais. O fitoplâncton cresce na camada superior iluminada do oceano, onde a quantidade de nutrientes inorgânicos, luz e temperatura varia espacial e temporalmente.[83] Estudos de laboratório mostram que essas flutuações desencadeiam respostas no nível celular, nas quais as células modificam a alocação de recursos para se adaptar de forma ideal ao seu ambiente.[91] Por exemplo, o fitoplâncton pode alterar a alocação de recursos entre o aparato biossintético rico em P, o aparato de captação de luz rico em N e as reservas de armazenamento de energia ricas em C.[92]
Sob um cenário típico de aquecimento futuro, espera-se que o oceano global passe por mudanças na disponibilidade de nutrientes, temperatura e irradiância.[93] Essas mudanças provavelmente terão efeitos profundos na fisiologia do fitoplâncton,[94][95] e observações mostram que espécies de fitoplâncton competitivas podem se aclimatar e adaptar a mudanças em temperatura, irradiância e nutrientes em escalas decenais.[96]
Numerosos experimentos de laboratório e de campo foram conduzidos para estudar a relação entre a razão C:N:P do fitoplâncton e os fatores ambientais. No entanto, é desafiador sintetizar esses estudos e generalizar a resposta do C:N:P do fitoplâncton às mudanças nos fatores ambientais.[83] Estudos individuais utilizam diferentes conjuntos de análises estatísticas para caracterizar os efeitos do(s) fator(es) ambiental(is) nas razões elementares, variando de um simples teste t a modelos mistos mais complexos, o que torna as comparações entre estudos desafiadoras. Além disso, como as mudanças de características induzidas pelo ambiente são impulsionadas por uma combinação de plasticidade (aclimatação), adaptação e história de vida,[97][98] as respostas estequiométricas do fitoplâncton podem ser variáveis mesmo entre espécies intimamente relacionadas.[83]
A meta-análise/revisão sistemática é uma estrutura estatística poderosa para sintetizar e integrar resultados de pesquisas obtidos de estudos independentes e para descobrir tendências gerais.[99] A síntese seminal de Geider e La Roche em 2002,[100] bem como o trabalho mais recente de Persson et al. em 2010,[101] mostraram que C:P e N:P podem variar até um fator de 20 entre células repletas de nutrientes e células limitadas por nutrientes. Esses estudos também mostraram que a razão C:N pode ser moderadamente plástica devido à limitação de nutrientes. Um estudo de meta-análise de Hillebrand et al. em 2013 destacou a importância da taxa de crescimento na determinação da estequiometria elementar e mostrou que as razões C:P e N:P diminuem com o aumento da taxa de crescimento.[102] Em 2015, Yvon-Durocher et al. investigaram o papel da temperatura na modulação de C:N:P.[103] Embora seu conjunto de dados fosse limitado a estudos realizados antes de 1996, eles mostraram uma relação estatisticamente significativa entre C:P e aumento de temperatura. MacIntyre et al. (2002)[104] e Thrane et al. (2016)[105] mostraram que a irradiância desempenha um papel importante no controle das razões celulares ótimas de C:N e N:P. Mais recentemente, Moreno e Martiny (2018) forneceram um resumo abrangente de como as condições ambientais regulam a estequiometria celular a partir de uma perspectiva fisiológica.[92][83]
A estequiometria elementar do fitoplâncton marinho desempenha um papel crítico nos ciclos biogeoquímicos globais por meio de seu impacto na ciclagem de nutrientes, produção secundária e exportação de carbono. Embora extensos experimentos de laboratório tenham sido realizados ao longo dos anos para avaliar a influência de diferentes fatores ambientais na composição elementar do fitoplâncton, uma avaliação quantitativa abrangente dos processos ainda está faltando. Aqui, as respostas das razões P:C e N:C do fitoplâncton marinho foram sintetizadas para cinco principais fatores (fósforo inorgânico, nitrogênio inorgânico, ferro inorgânico, irradiância e temperatura) por uma meta-análise de dados experimentais em 366 experimentos de 104 artigos de revistas. Esses resultados mostram que a resposta dessas razões às mudanças em macronutrientes é consistente em todos os estudos, onde o aumento na disponibilidade de nutrientes está positivamente relacionado às mudanças nas razões P:C e N:C. Os resultados mostram que o fitoplâncton eucariótico é mais sensível às mudanças em macronutrientes em comparação com os procariotos, possivelmente devido ao seu maior tamanho celular e suas capacidades de regular rapidamente seus padrões de expressão gênica. O efeito da irradiância foi significativo e constante em todos os estudos, onde um aumento na irradiância diminuiu tanto P:C quanto N:C. A razão P:C diminuiu significativamente com o aquecimento, mas a resposta às mudanças de temperatura foi mista, dependendo do modo de crescimento da cultura e da fase de crescimento no momento da colheita. Junto com outras condições oceanográficas dos giros subtropicais (por exemplo, baixa disponibilidade de macronutrientes), a temperatura elevada pode explicar por que P:C é consistentemente baixo nos oceanos subtropicais. A adição de ferro não alterou sistematicamente nem P:C nem N:C.[83]
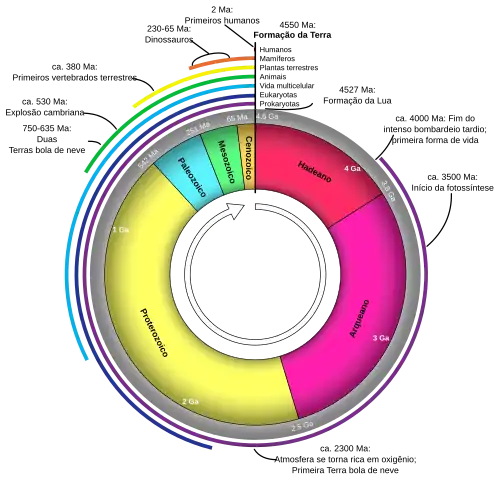
Linha do tempo evolutiva
.png)
Veja também
- Algas
- Plantas aquáticas
- Bomba biológica (oceanografia)
- História evolutiva das plantas
- Ciclo do carbono nos oceanos
Referências
- ↑ «Chlorophyll». NASA Earth Observatory. Consultado em 9 de junho de 2025
- ↑ «Modeled Phytoplankton Communities in the Global Ocean». NASA Hyperwall. 30 de setembro de 2015. Consultado em 9 de junho de 2025
- ↑ «Darwin Project». Massachusetts Institute of Technology. Consultado em 9 de junho de 2025
- ↑ a b Campbell, Neil A.; Reece, Jane B.; Urry, Lisa Andrea; Cain, Michael L.; Wasserman, Steven Alexander; Minorsky, Peter V.; Jackson, Robert Bradley (2008). Biology 8 ed. San Francisco: Pearson – Benjamin Cummings. ISBN 978-0-321-54325-7
- ↑ McNeill, J.; et al., eds. (2012). International Code of Nomenclature for algae, fungi, and plants (Melbourne Code), Adopted by the Eighteenth International Botanical Congress Melbourne, Australia, July 2011 electronic ed. [S.l.]: International Association for Plant Taxonomy. Consultado em 9 de junho de 2025
- ↑ Schäfer G, Engelhard M, Müller V (1999). «Bioenergetics of the Archaea». Microbiol. Mol. Biol. Rev. 63 (3): 570–620. PMC 103747
 . PMID 10477309. doi:10.1128/MMBR.63.3.570-620.1999
. PMID 10477309. doi:10.1128/MMBR.63.3.570-620.1999
- ↑ Roach, John (2004). «Source of Half Earth's Oxygen Gets Little Credit». National Geographic News. Consultado em 9 de junho de 2025. Arquivado do original em 8 de junho de 2004
- ↑ Lin, I.; Liu, W. Timothy; Wu, Chun-Chieh; Wong, George T. F.; Hu, Chuanmin; Chen, Zhiqiang; Wen-Der, Liang; Yang, Yih; Liu, Kon-Kee (2003). «New evidence for enhanced ocean primary production triggered by tropical cyclone». Geophysical Research Letters. 30 (13): 1718. Bibcode:2003GeoRL..30.1718L. doi:10.1029/2003GL017141. Consultado em 9 de junho de 2025
- ↑ Sigman, D.M.; Hain, M.P. (2012). «The Biological Productivity of the Ocean» (PDF). Nature Education Knowledge. 3 (6): 1–16. Consultado em 9 de junho de 2025
- ↑ Mora, C.; et al. (2013). «Biotic and Human Vulnerability to Projected Changes in Ocean Biogeochemistry over the 21st Century». PLOS Biology. 11 (10): e1001682. PMC 3797030
 . PMID 24143135. doi:10.1371/journal.pbio.1001682
. PMID 24143135. doi:10.1371/journal.pbio.1001682
- ↑ «A 'regime shift' is happening in the Arctic Ocean, scientists say». phys.org (em inglês). Consultado em 9 de junho de 2025
- ↑ Lewis, K. M.; Dijken, G. L. van; Arrigo, K. R. (2020). «Changes in phytoplankton concentration now drive increased Arctic Ocean primary production». Science (em inglês). 369 (6500): 198–202. ISSN 0036-8075. PMID 32647002. doi:10.1126/science.aay8380. Consultado em 9 de junho de 2025
- ↑ Olson, J. M.; Blankenship, R. E. (2005). «Thinking about the evolution of photosynthesis». Discoveries in Photosynthesis. [S.l.]: Springer. pp. 1073–1086. ISBN 9781402033247. doi:10.1007/1-4020-3324-9_95
- ↑ Blankenship, R. E.; Sadekar, S.; Raymond, J. (2007). «The evolutionary transition from anoxygenic to oxygenic photosynthesis». In: Falkowski, P. G.; Knoll, A. N. Evolution of Aquatic Photoautotrophs. [S.l.]: Academic Press. pp. 21–35. doi:10.1016/B978-012370518-1/50004-7
- ↑ Hohmann-Marriott, M.F.; Blankenship, R.E. (2011). «Evolution of photosynthesis». Annual Review of Plant Biology. 62: 515–548. doi:10.1146/annurev-arplant-042110-103811
- ↑ Kim, E.; Harrison, J.W.; Sudek, S.; Jones, M.D.; Wilcox, H.M.; Richards, T.A.; Worden, A.Z.; Archibald, J.M. (2011). «Newly identified and diverse plastid-bearing branch on the eukaryotic tree of life». Proceedings of the National Academy of Sciences. 108 (4): 1496–1500. doi:10.1073/pnas.1013337108
- ↑ Garcia-Mendoza, E.; Ocampo-Alvarez, H. (2011). «Photoprotection in the brown alga Macrocystis pyrifera: evolutionary implications». Journal of Photochemistry and Photobiology B: Biology. 104 (1-2): 377–385. doi:10.1016/j.jphotobiol.2011.04.004
- ↑ Shevela, D. (2011). «Adventures with cyanobacteria: a personal perspective». Frontiers in Plant Science. 2. 28 páginas. doi:10.3389/fpls.2011.00028

- ↑ Walsh PJ, Smith S, Fleming L, Solo-Gabriele H, Gerwick WH, eds. (2011). «Cyanobacteria and cyanobacterial toxins». Oceans and Human Health: Risks and Remedies from the Seas. [S.l.]: Academic Press. pp. 271–296. ISBN 978-0-08-087782-2. Consultado em 9 de junho de 2025
- ↑ «The Rise of Oxygen». Astrobiology Magazine (em inglês). 2003. Consultado em 9 de junho de 2025. Arquivado do original em 3 de abril de 2015
- ↑ Flannery, D. T.; R.M. Walter (2012). «Archean tufted microbial mats and the Great Oxidation Event: new insights into an ancient problem». Australian Journal of Earth Sciences. 59 (1): 1–11. Bibcode:2012AuJES..59....1F. doi:10.1080/08120099.2011.607849
- ↑ Rothschild, Lynn (2003). «Understand the evolutionary mechanisms and environmental limits of life». NASA. Consultado em 9 de junho de 2025. Arquivado do original em 29 de março de 2012
- ↑ Nadis S (2003). «The cells that rule the seas» (PDF). Scientific American. 289 (6): 52–3. Bibcode:2003SciAm.289f..52N. PMID 14631732. doi:10.1038/scientificamerican1203-52. Consultado em 9 de junho de 2025. Arquivado do original (PDF) em 19 de abril de 2014
- ↑ «The Most Important Microbe You've Never Heard Of». npr.org. Consultado em 9 de junho de 2025
- ↑ Flombaum, P.; Gallegos, J. L.; Gordillo, R. A.; Rincon, J.; Zabala, L. L.; Jiao, N.; Karl, D. M.; Li, W. K. W.; Lomas, M. W.; Veneziano, D.; Vera, C. S.; Vrugt, J. A.; Martiny, A. C. (2013). «Present and future global distributions of the marine Cyanobacteria Prochlorococcus and Synechococcus». Proceedings of the National Academy of Sciences. 110 (24): 9824–9829. Bibcode:2013PNAS..110.9824F. PMC 3683724
 . PMID 23703908. doi:10.1073/pnas.1307701110
. PMID 23703908. doi:10.1073/pnas.1307701110
- ↑ Nabors, Murray W. (2004). Introduction to Botany. San Francisco, CA: Pearson Education, Inc. ISBN 978-0-8053-4416-5
- ↑ Allaby, M., ed. (1992). «Algae». The Concise Dictionary of Botany. Oxford: Oxford University Press
- ↑ Grotewold, E. (2006). «The Genetics and Biochemistry of Floral Pigments». Annual Review of Plant Biology. 57: 761–780. PMID 16669781. doi:10.1146/annurev.arplant.57.032905.105248
- ↑ Lee, Dw (2007). Nature's Palette - the Science of Plant Color. [S.l.]: University of Chicago Press
- ↑ «Concepts of Biology: Eukaryotic Origins». OpenStax CNX. Consultado em 16 de julho de 2020 Texto modificado foi copiado desta fonte, que está disponível sob uma Licença Creative Commons Atribuição 4.0 Internacional.
- ↑ «cloroplasto». Online Etymology Dictionary. Consultado em 9 de junho de 2025
- ↑ Basic Biology (2016). «Bactérias». Consultado em 9 de junho de 2025
- ↑ DeLong, E.F.; Beja, O. (2010). «The light-driven proton pump proteorhodopsin enhances bacterial survival during tough times». PLOS Biology. 8 (4): e1000359. PMC 2860490
 . PMID 20436957. doi:10.1371/journal.pbio.1000359
. PMID 20436957. doi:10.1371/journal.pbio.1000359 . e1000359
. e1000359
- ↑ Patrick J. Keeling (2004). «Diversity and evolutionary history of plastids and their hosts». American Journal of Botany. 91 (10): 1481–1493. PMID 21652304. doi:10.3732/ajb.91.10.1481

- ↑ a b Gómez-Consarnau, L.; Raven, J.A.; Levine, N.M.; Cutter, L.S.; Wang, D.; Seegers, B.; Arístegui, J.; Fuhrman, J.A.; Gasol, J.M.; Sañudo-Wilhelmy, S.A. (2019). «Microbial rhodopsins are major contributors to the solar energy captured in the sea». Science Advances. 5 (8): eaaw8855. Bibcode:2019SciA....5.8855G. PMC 6685716
 . PMID 31457093. doi:10.1126/sciadv.aaw8855
. PMID 31457093. doi:10.1126/sciadv.aaw8855
- ↑ Oren, Aharon (2002). «Molecular ecology of extremely halophilic Archaea and Bacteria». FEMS Microbiology Ecology. 39 (1): 1–7. Bibcode:2002FEMME..39....1O. ISSN 0168-6496. PMID 19709178. doi:10.1111/j.1574-6941.2002.tb00900.x

- ↑ a b Béja, O.; Aravind, L.; Koonin, E.V.; Suzuki, M.T.; Hadd, A.; Nguyen, L.P.; Jovanovich, S.B.; Gates, C.M.; Feldman, R.A.; Spudich, J.L.; Spudich, E.N. (2000). «Bacterial rhodopsin: evidence for a new type of phototrophy in the sea». Science. 289 (5486): 1902–1906. Bibcode:2000Sci...289.1902B. PMID 10988064. doi:10.1126/science.289.5486.1902
- ↑ «Interviews with Fellows: Ed Delong». American Academy of Microbiology. Consultado em 9 de junho de 2025. Arquivado do original em 7 de agosto de 2016
- ↑ Bacteria with Batteries, Popular Science, January 2001, Page 55.
- ↑ Boeuf, Dominique; Audic, Stéphane; Brillet-Guéguen, Loraine; Caron, Christophe; Jeanthon, Christian (2015). «MicRhoDE: a curated database for the analysis of microbial rhodopsin diversity and evolution». Database. 2015: bav080. ISSN 1758-0463. PMC 4539915
 . PMID 26286928. doi:10.1093/database/bav080
. PMID 26286928. doi:10.1093/database/bav080
- ↑ Yawo, Hiromu; Kandori, Hideki; Koizumi, Amane (5 de junho de 2015). Optogenetics: Light-Sensing Proteins and Their Applications. [S.l.]: Springer. pp. 3–4. ISBN 978-4-431-55516-2. Consultado em 9 de junho de 2025
- ↑ «A tiny marine microbe could play a big role in climate change». University of Southern California, Press Room. 2019. Consultado em 9 de junho de 2025
- ↑ DasSarma, Shiladitya; Schwieterman, Edward W. (2018). «Early evolution of purple retinal pigments on Earth and implications for exoplanet biosignatures». International Journal of Astrobiology. 20 (3): 241–250. Bibcode:2018arXiv181005150D. ISSN 1473-5504. arXiv:1810.05150
 . doi:10.1017/S1473550418000423. Consultado em 9 de junho de 2025
. doi:10.1017/S1473550418000423. Consultado em 9 de junho de 2025
- ↑ Sparks, William B.; DasSarma, S.; Reid, I. N. (2006). «Evolutionary Competition Between Primitive Photosynthetic Systems: Existence of an early purple Earth?». American Astronomical Society Meeting Abstracts. 38: 901. Bibcode:2006AAS...209.0605S
- ↑ Javed, M.R., Bilal, M.J., Ashraf, M.U.F., Waqar, A., Mehmood, M.A., Saeed, M. and Nashat, N. (2019) "Microalgae as a Feedstock for Biofuel Production: Current Status and Future Prospects" In: Top 5 Contributions in Energy Research and Development, third edition, chapter 2, Avid Science. ISBN 978-93-88170-77-2.
 Modified text was copied from this source, which is available under a Creative Commons Attribution 4.0 International License.
Modified text was copied from this source, which is available under a Creative Commons Attribution 4.0 International License.
- ↑ Guiry MD (2012). «How many species of algae are there?». Journal of Phycology. 48 (5): 1057–1063. Bibcode:2012JPcgy..48.1057G. PMID 27011267. doi:10.1111/j.1529-8817.2012.01222.x
- ↑ a b Guiry, M.D.; Guiry, G.M. (2016). «Algaebase». www.algaebase.org. Consultado em 20 de novembro de 2016
- ↑ Thomas, D. (2002). Seaweeds. [S.l.]: Life Series. Natural History Museum, London. ISBN 978-0-565-09175-0
- ↑ Hoek, Christiaan; den Hoeck, Hoeck Van; Mann, David; Jahns, H.M. (1995). Algae: an introduction to phycology. [S.l.]: Cambridge University Press. p. 166. ISBN 9780521316873. OCLC 443576944. Consultado em 9 de junho de 2025
- ↑ Yool, A.; Tyrrell, T. (2003). «Role of diatoms in regulating the ocean's silicon cycle». Global Biogeochemical Cycles. 17 (4): n/a. Bibcode:2003GBioC..17.1103Y. CiteSeerX 10.1.1.394.3912
 . doi:10.1029/2002GB002018
. doi:10.1029/2002GB002018
- ↑ «The Air You're Breathing? A Diatom Made That». Live Science. Consultado em 11 de julho de 2019
- ↑ «More on Diatoms». University of California Museum of Paleontology. Consultado em 11 de julho de 2019. Arquivado do original em 4 de outubro de 2012
- ↑ «This twilight zone is dark, watery, and yes, also full of intrigue». NASA Blog. 2018. Consultado em 9 de junho de 2025
- ↑ Smith, H.E.K.; et al. (2012). «Predominance of heavily calcified coccolithophores at low CaCO3 saturation during winter in the Bay of Biscay». Proceedings of the National Academy of Sciences. 109 (23): 8845–8849. Bibcode:2012PNAS..109.8845S. PMC 3384182
 . PMID 22615387. doi:10.1073/pnas.1117508109
. PMID 22615387. doi:10.1073/pnas.1117508109
- ↑ «Biogeography and dispersal of micro-organisms: a review emphasizing protists». Acta Protozoologica. 45 (2): 111–136. 2005
- ↑ Yunev, O.A.; et al. (2007). «Nutrient and phytoplankton trends on the western Black Sea shelf in response to cultural eutrofication and climate changes». Estuarine, Coastal and Shelf Science. 74 (1–2): 63–67. Bibcode:2007ECSS...74...63Y. doi:10.1016/j.ecss.2007.03.030
- ↑ Brand, Larry E.; Campbell, Lisa; Bresnan, Eileen (2012). «Karenia: The biology and ecology of a toxic genus». Harmful Algae. 14: 156–178. Bibcode:2012HAlga..14..156B. PMC 9891709
 . PMID 36733478. doi:10.1016/j.hal.2011.10.020
. PMID 36733478. doi:10.1016/j.hal.2011.10.020
- ↑ Olsen GJ, Woese CR, Overbeek R (1994). «The winds of (evolutionary) change: breathing new life into microbiology». Journal of Bacteriology. 176 (1): 1–6. PMC 205007
 . PMID 8282683. doi:10.2172/205047
. PMID 8282683. doi:10.2172/205047
- ↑ Bork, P.; Bowler, C.; De Vargas, C.; Gorsky, G.; Karsenti, E.; Wincker, P. (2015). «Tara Oceans studies plankton at planetary scale». Science. doi:10.1126/science.aac5605
- ↑ Gawryluk, Ryan M.R.; Del Campo, Javier; Okamoto, Noriko; Strassert, Jürgen F.H.; Lukeš, Julius; Richards, Thomas A.; Worden, Alexandra Z.; Santoro, Alyson E.; Keeling, Patrick J. (2016). «Morphological Identification and Single-Cell Genomics of Marine Diplonemids». Current Biology. 26 (22): 3053–3059. Bibcode:2016CBio...26.3053G. PMID 27875688. doi:10.1016/j.cub.2016.09.013

- ↑ Faktorová, D.; Dobáková, E.; Peña-Diaz, P.; Lukeš, J. (2016). «From simple to supercomplex: mitochondrial genomes of euglenozoan protists». F1000Research. 5. doi:10.12688/f1000research.8040.1
 Texto modificado foi copiado desta fonte, que está disponível sob uma Licença Creative Commons Atribuição 4.0 Internacional.
Texto modificado foi copiado desta fonte, que está disponível sob uma Licença Creative Commons Atribuição 4.0 Internacional.
- ↑ De Vargas, C.; Audic, S.; Henry, N.; Decelle, J.; Mahé, F.; Logares, R.; Lara, E.; Berney, C.; Le Bescot, N.; Probert, I.; Carmichael, M. (2015). «Eukaryotic plankton diversity in the sunlit ocean». Science. 348 (6237). 1261605 páginas. doi:10.1126/science.1261605
- ↑ Starckx, Senne (2012). «A place in the sun - Algae is the crop of the future, according to researchers in Geel». Flanders Today. Consultado em 8 de dezembro de 2012. Cópia arquivada em 4 de março de 2016
- ↑ Wernberg, T.; Krumhansl, K.; Filbee-Dexter, K.; Pedersen, M.F. (2019). Status and trends for the world’s kelp forests. [S.l.]: Academic Press. pp. 57–78. doi:10.1016/B978-0-12-805052-1.00003-6
- ↑ Mann, K.H. (1973). «Seaweeds: their productivity and strategy for growth». Science. 182 (4116): 975–981
- ↑ Kindersley, Dorling (2011). Illustrated Encyclopedia of the Ocean. [S.l.]: Dorling Kindersley. pp. 246–255. ISBN 978-1-4053-3308-5
- ↑ Tunnell, John Wesley; Chávez, Ernesto A.; Withers, Kim (2007). Coral reefs of the southern Gulf of Mexico. [S.l.]: Texas A&M University Press. p. 91. ISBN 978-1-58544-617-9. Consultado em 9 de junho de 2025
- ↑ a b c d e De Vries, Jan; De Vries, Sophie; Fürst-Jansen, Janine M R. (2020). «Evo-physio: On stress responses and the earliest land plants». Journal of Experimental Botany. 71 (11): 3254–3269. PMC 7289718
 . PMID 31922568. doi:10.1093/jxb/eraa007 Texto modificado foi copiado desta fonte, que está disponível sob uma Licença Creative Commons Atribuição 4.0 Internacional.
. PMID 31922568. doi:10.1093/jxb/eraa007 Texto modificado foi copiado desta fonte, que está disponível sob uma Licença Creative Commons Atribuição 4.0 Internacional.
- ↑ Morris, Jennifer L.; Puttick, Mark N.; Clark, James W.; Edwards, Dianne; Kenrick, Paul; Pressel, Silvia; Wellman, Charles H.; Yang, Ziheng; Schneider, Harald; Donoghue, Philip C. J. (2018). «The timescale of early land plant evolution». Proceedings of the National Academy of Sciences. 115 (10): E2274–E2283. Bibcode:2018PNAS..115E2274M. PMC 5877938
 . PMID 29463716. doi:10.1073/pnas.1719588115
. PMID 29463716. doi:10.1073/pnas.1719588115
- ↑ Delaux, Pierre-Marc; Hetherington, Alexander J.; Coudert, Yoan; Delwiche, Charles; Dunand, Christophe; Gould, Sven; Kenrick, Paul; Li, Fay-Wei; Philippe, Hervé; Rensing, Stefan A.; Rich, Mélanie; Strullu-Derrien, Christine; De Vries, Jan (2019). «Reconstructing trait evolution in plant evo–devo studies». Current Biology. 29 (21): R1110–R1118. Bibcode:2019CBio...29R1110D. PMID 31689391. doi:10.1016/j.cub.2019.09.044

- ↑ Orth, R.J.; Carruthers, T.J.; Dennison, W.C.; Duarte, C.M.; Fourqurean, J.W.; Heck, K.L.; Hughes, A.R.; Kendrick, G.A.; Kenworthy, W.J.; Olyarnik, S.; Short, F.T. (2006). «A global crisis for seagrass ecosystems». BioScience. 56 (12): 987–996. doi:10.1641/0006-3568(2006)56[987:AGCFSE]2.0.CO;2
- ↑ van der Heide, T.; van Nes, E.H.; van Katwijk, M.M.; Olff, H.; Smolders, A.J.P. (2011). Romanuk, Tamara, ed. «Positive feedbacks in seagrass ecosystems: evidence from large-scale empirical data». PLOS ONE. 6 (1): e16504. Bibcode:2011PLoSO...616504V. PMC 3025983
 . PMID 21283684. doi:10.1371/journal.pone.0016504
. PMID 21283684. doi:10.1371/journal.pone.0016504
- ↑ «Mangal (Mangrove)». Mildred E. Mathias Botanical Garden. Consultado em 11 de julho de 2013
- ↑ «Coastal Salt Marsh». Mildred E. Mathias Botanical Garden. Consultado em 11 de julho de 2013
- ↑ «Facts and figures on marine biodiversity». Marine biodiversity. UNESCO. 2012. Consultado em 11 de julho de 2013
- ↑ Russell, F. S.; Yonge, C. M. (1928). The Seas. [S.l.]: Frederick Warne. pp. 225–227
- ↑ Voss, Maren; Bange, Hermann W.; Dippner, Joachim W.; Middelburg, Jack J.; Montoya, Joseph P.; Ward, Bess (2013). «The marine nitrogen cycle: recent discoveries, uncertainties and the potential relevance of climate change». Philosophical Transactions of the Royal Society B. 368 (1621). 20130121 páginas. PMC 3682741
 . PMID 23713119. doi:10.1098/rstb.2013.0121
. PMID 23713119. doi:10.1098/rstb.2013.0121
- ↑ Stow, Dorrik (2004). Encyclopedia of the Oceans. [S.l.]: Oxford University Press. pp. 160–163. ISBN 978-0-19-860687-1
- ↑ Giri, C.; Ochieng, E.; Tieszen, L.L.; Zhu, Z.; Singh, A.; Loveland, T. (2011). «Status and distribution of mangrove forests of the world using earth observation satellite data». Global Ecology and Biogeography. 20 (1): 154–159. doi:10.1111/j.1466-8238.2010.00584.x
- ↑ Thomas, N.; Lucas, R.; Bunting, P.; Hardy, A.; Rosenqvist, A.; Simard, M. (2017). «Distribution and drivers of global mangrove forest change, 1996–2010». PLOS ONE. 12 (6): e0179302. doi:10.1371/journal.pone.0179302

- ↑ Short, F.T.; Frederick, T. (2003). World atlas of seagrasses. [S.l.]: University of California Press. p. 24. ISBN 9780520240476. Consultado em 9 de junho de 2025. Cópia arquivada em 10 de julho de 2019
- ↑ Froese, Rainer; Pauly, Daniel (eds.) (2009). "Phycodurus eques" em FishBase. Versão July 2009.
- ↑ a b c d e f g h Tanioka, Tatsuro; Matsumoto, Katsumi (2020). «A meta-analysis on environmental drivers of marine phytoplankton C:N:P». Biogeosciences. 17 (11): 2939–2954. Bibcode:2020BGeo...17.2939T. doi:10.5194/bg-17-2939-2020
 Texto modificado foi copiado desta fonte, que está disponível sob uma Licença Creative Commons Atribuição 4.0 Internacional.
Texto modificado foi copiado desta fonte, que está disponível sob uma Licença Creative Commons Atribuição 4.0 Internacional.
- ↑ Broecker, Wallace S. (1982). «Ocean chemistry during glacial time». Geochimica et Cosmochimica Acta. 46 (10): 1689–1705. Bibcode:1982GeCoA..46.1689B. doi:10.1016/0016-7037(82)90110-7
- ↑ Lenton, Timothy M.; Watson, Andrew J. (2000). «Redfield revisited: 1. Regulation of nitrate, phosphate, and oxygen in the ocean». Global Biogeochemical Cycles. 14 (1): 225–248. Bibcode:2000GBioC..14..225L. doi:10.1029/1999GB900065

- ↑ Redfield, A. C. (1958). «The biological control of chemical factors in the environment». American Scientist. 46 (3): 230A–221. Consultado em 9 de junho de 2025
- ↑ Tyrrell, Toby (1999). «The relative influences of nitrogen and phosphorus on oceanic primary production». Nature. 400 (6744): 525–531. Bibcode:1999Natur.400..525T. doi:10.1038/22941
- ↑ Bonachela, Juan A.; Klausmeier, Christopher A.; Edwards, Kyle F.; Litchman, Elena; Levin, Simon A. (2016). «The role of phytoplankton diversity in the emergent oceanic stoichiometry». Journal of Plankton Research. 38 (4): 1021–1035. doi:10.1093/plankt/fbv087

- ↑ Garcia, Catherine A.; Baer, Steven E.; Garcia, Nathan S.; Rauschenberg, Sara; Twining, Benjamin S.; Lomas, Michael W.; Martiny, Adam C. (2018). «Nutrient supply controls particulate elemental concentrations and ratios in the low latitude eastern Indian Ocean». Nature Communications. 9 (1): 4868. Bibcode:2018NatCo...9.4868G. PMC 6242840
 . PMID 30451846. doi:10.1038/s41467-018-06892-w
. PMID 30451846. doi:10.1038/s41467-018-06892-w
- ↑ Martiny, Adam C.; Pham, Chau T. A.; Primeau, Francois W.; Vrugt, Jasper A.; Moore, J. Keith; Levin, Simon A.; Lomas, Michael W. (2013). «Strong latitudinal patterns in the elemental ratios of marine plankton and organic matter». Nature Geoscience. 6 (4): 279–283. Bibcode:2013NatGe...6..279M. doi:10.1038/ngeo1757. Consultado em 9 de junho de 2025
- ↑ Geider, Richard; La Roche, Julie (2002). «Redfield revisited: Variability of C:N:P in marine microalgae and its biochemical basis» (PDF). European Journal of Phycology. 37 (1): 1–17. Bibcode:2002EJPhy..37....1G. doi:10.1017/S0967026201003456. Consultado em 9 de junho de 2025
- ↑ a b Moreno, Allison R.; Martiny, Adam C. (2018). «Ecological Stoichiometry of Ocean Plankton». Annual Review of Marine Science. 10: 43–69. Bibcode:2018ARMS...10...43M. PMID 28853998. doi:10.1146/annurev-marine-121916-063126
- ↑ Boyd, Philip W.; Strzepek, Robert; Fu, Feixue; Hutchins, David A. (2010). «Environmental control of open-ocean phytoplankton groups: Now and in the future». Limnology and Oceanography. 55 (3): 1353–1376. Bibcode:2010LimOc..55.1353B. doi:10.4319/lo.2010.55.3.1353
- ↑ Finkel, Z. V.; Beardall, J.; Flynn, K. J.; Quigg, A.; Rees, T. A. V.; Raven, J. A. (2010). «Phytoplankton in a changing world: Cell size and elemental stoichiometry». Journal of Plankton Research. 32: 119–137. doi:10.1093/plankt/fbp098
- ↑ Van De Waal, Dedmer B.; Verschoor, Antonie M.; Verspagen, Jolanda MH; Van Donk, Ellen; Huisman, Jef (2010). «Climate-driven changes in the ecological stoichiometry of aquatic ecosystems». Frontiers in Ecology and the Environment. 8 (3): 145–152. Bibcode:2010FrEE....8..145V. doi:10.1890/080178. hdl:20.500.11755/c74d7e45-762a-4e66-aa31-844e96e69fa2
 . Consultado em 9 de junho de 2025
. Consultado em 9 de junho de 2025
- ↑ Irwin, Andrew J.; Finkel, Zoe V.; Müller-Karger, Frank E.; Troccoli Ghinaglia, Luis (2015). «Phytoplankton adapt to changing ocean environments». Proceedings of the National Academy of Sciences. 112 (18): 5762–5766. Bibcode:2015PNAS..112.5762I. PMC 4426419
 . PMID 25902497. doi:10.1073/pnas.1414752112
. PMID 25902497. doi:10.1073/pnas.1414752112
- ↑ Collins, Sinéad; Boyd, Philip W.; Doblin, Martina A. (2020). «Evolution, Microbes, and Changing Ocean Conditions». Annual Review of Marine Science. 12: 181–208. Bibcode:2020ARMS...12..181C. PMID 31451085. doi:10.1146/annurev-marine-010318-095311
- ↑ Ward, B. A.; Collins, S.; Dutkiewicz, S.; Gibbs, S.; Bown, P.; Ridgwell, A.; Sauterey, B.; Wilson, J. D.; Oschlies, A. (2019). «Considering the Role of Adaptive Evolution in Models of the Ocean and Climate System». Journal of Advances in Modeling Earth Systems. 11 (11): 3343–3361. Bibcode:2019JAMES..11.3343W. PMC 6988444
 . PMID 32025278. doi:10.1029/2018MS001452
. PMID 32025278. doi:10.1029/2018MS001452
- ↑ Gurevitch, Jessica; Koricheva, Julia; Nakagawa, Shinichi; Stewart, Gavin (2018). «Meta-analysis and the science of research synthesis». Nature. 555 (7695): 175–182. Bibcode:2018Natur.555..175G. PMID 29517004. doi:10.1038/nature25753. Consultado em 9 de junho de 2025
- ↑ Geider, Richard; La Roche, Julie (2002). «Redfield revisited: Variability of C:N:P in marine microalgae and its biochemical basis» (PDF). European Journal of Phycology. 37 (1): 1–17. Bibcode:2002EJPhy..37....1G. doi:10.1017/S0967026201003456. Consultado em 9 de junho de 2025
- ↑ Persson, Jonas; Fink, Patrick; Goto, Akira; Hood, James M.; Jonas, Jayne; Kato, Satoshi (2010). «To be or not to be what you eat: Regulation of stoichiometric homeostasis among autotrophs and heterotrophs». Oikos. 119 (5): 741–751. Bibcode:2010Oikos.119..741P. doi:10.1111/j.1600-0706.2009.18545.x
- ↑ Hillebrand, Helmut; Steinert, Georg; Boersma, Maarten; Malzahn, Arne; Meunier, Cédric Léo; Plum, Christoph; Ptacnik, Robert (2013). «Goldman revisited: Faster-growing phytoplankton has lower N:P and lower stoichiometric flexibility». Limnology and Oceanography. 58 (6): 2076–2088. Bibcode:2013LimOc..58.2076H. doi:10.4319/lo.2013.58.6.2076

- ↑ Yvon-Durocher, Gabriel; Dossena, Matteo; Trimmer, Mark; Woodward, Guy; Allen, Andrew P. (2015). «Temperature and the biogeography of algal stoichiometry». Global Ecology and Biogeography. 24 (5): 562–570. Bibcode:2015GloEB..24..562Y. doi:10.1111/geb.12280
- ↑ MacIntyre, Hugh L.; Kana, Todd M.; Anning, Tracy; Geider, Richard J. (2002). «Photoacclimation of Photosynthesis Irradiance Response Curves and Photosynthetic Pigments in Microalgae and Cyanobacteria1». Journal of Phycology. 38 (1): 17–38. Bibcode:2002JPcgy..38...17M. doi:10.1046/j.1529-8817.2002.00094.x
- ↑ Thrane, Jan-Erik; Hessen, Dag O.; Andersen, Tom (2016). «The impact of irradiance on optimal and cellular nitrogen to phosphorus ratios in phytoplankton». Ecology Letters. 19 (8): 880–888. Bibcode:2016EcolL..19..880T. PMID 27250733. doi:10.1111/ele.12623

- ↑ Hassani, M.A., Durán, P. and Hacquard, S. (2018) "Microbial interactions within the plant holobiont". Microbiome, 6(1): 58. doi:10.1186/s40168-018-0445-0.
 Modified text was copied from this source, which is available under a Creative Commons Attribution 4.0 International License.
Modified text was copied from this source, which is available under a Creative Commons Attribution 4.0 International License.
- ↑ Lucking, R., Huhndorf, S., Pfister, D.H., Plata, E.R. and Lumbsch, H.T. (2009) "Fungi evolved right on track". Mycologia, 101(6): 810–822. doi:10.3852/09-016.
- ↑ Heckman, D.S., Geiser, D.M., Eidell, B.R., Stauffer, R.L., Kardos, N.L. and Hedges, S.B. (2001) "Molecular evidence for the early colonization of land by fungi and plants". Science, 293(5532): 1129–1133. doi:10.1126/science.1061457.
Ligações externas
- Falkowski, Paul (Ed.) (2013) Primary Productivity in the Sea Springer. ISBN 9781468438901.
- Falkowski, Paul and Raven, John A. (2013) Aquatic Photosynthesis Second edition revised, Princeton University Press. ISBN 9781400849727.
- Falkowski P and Knoll AH (2011) Evolution of Primary Producers in the Sea Academic Press. ISBN 9780080550510.
- Kirk, John T. O. (2010) Light and Photosynthesis in Aquatic Ecosystems Third edition revised, Cambridge University Press. ISBN 9781139493918.
- Evolução das plantas
- Linha do tempo da evolução das plantas
- Evolução da fotossíntese
