Coprinellus micaceus
Coprinellus micaceus
| |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Classificação científica | |||||||||||||||||
| |||||||||||||||||
| Nome binomial | |||||||||||||||||
| Coprinellus micaceus (Bull.:Fr.) Vilgalys, Hopple & Jacq.Johnson (2001) | |||||||||||||||||
| Sinónimos[1] | |||||||||||||||||
| |||||||||||||||||
Coprinellus micaceus é uma espécie comum de fungo formador de cogumelos da família Psathyrellaceae.
Anteriormente conhecida como Coprinus micaceus, a espécie foi transferida para Coprinellus [en] em 2001, quando análises filogenéticas levaram à reorganização das muitas espécies anteriormente agrupadas no gênero Coprinus. Com base na aparência externa, C. micaceus é praticamente indistinguível de C. truncorum, e tem sido sugerido que muitas coletas reportadas da primeira podem ser, na verdade, da segunda.
Dependendo do estágio de desenvolvimento, os píleos dos cogumelos marrom-alaranjados podem variar de forma oval a campanulada ou convexa, atingindo diâmetros de até 3 cm. Os píleos, marcados por finos sulcos radiais ou lineares que se estendem quase até o centro, repousam sobre estipes esbranquiçados de até 10 cm de comprimento. Em exemplares jovens, toda a superfície do píleo é coberta por uma fina camada de células reflexivas semelhantes à mica. Embora pequenos e com carne fina, os cogumelos geralmente são abundantes, pois crescem tipicamente em aglomerados densos. Algumas horas após a coleta, as lamelas começarão a se dissolver lentamente em um líquido preto, viscoso e carregado de esporos — um processo enzimático chamado autodigestão ou deliquescência.
Com distribuição cosmopolita, o cogumelo saprófito produz tipicamente aglomerados em ou perto de tocos de árvores de madeira dura em decomposição ou raízes subterrâneas de árvores. Os basidiomas são comestíveis antes que as lamelas escureçam e se dissolvam; o cozimento interrompe o processo de autodigestão. Análises químicas dos basidiomas revelaram a presença de compostos antibacterianos e inibidores de enzimas.
Taxonomia

Coprinellus micaceus foi ilustrada em uma xilogravura pelo botânico do século XVI Carolus Clusius no que é considerado a primeira monografia publicada sobre fungos, a Rariorum plantarum historia de 1601 (História de plantas raras), em um apêndice.[2][3] Clusius acreditava erroneamente que a espécie era tóxica e a classificou como um gênero de Fungi perniciales (fungos nocivos). A espécie foi descrita cientificamente pela primeira vez pelo botânico francês Jean Baptiste François Pierre Bulliard em 1786 como Agaricus micaceus em sua obra Herbier de la France.[4] Em 1801, Christian Hendrik Persoon agrupou todos os fungos laminados que se autodigerem (deliquescem) durante a liberação de esporos na seção Coprinus do gênero Agaricus.[5] Elias Magnus Fries elevou mais tarde a seção Coprinus de Persoon ao status de gênero em sua Epicrisis Systematis Mycologici, e a espécie passou a ser conhecida como Coprinus micaceus.[6] Era a espécie-tipo da subseção Exannulati na seção Micacei do gênero Coprinus, um agrupamento de táxons relacionados com véus parciais formados exclusivamente por esferocistos (células redondas inchadas geralmente formadas em aglomerados) ou com hifas filamentosas finas misturadas.[7] Estudos moleculares publicados na década de 1990[8][9] demonstraram que muitos dos cogumelos coprinoides (semelhantes a Coprinus) não eram, na verdade, relacionados entre si. Isso culminou em uma revisão de 2001 do gênero Coprinus, que foi dividido em quatro gêneros; C. micaceus foi transferido para Coprinellus.[10]
Em parte devido à sua fácil disponibilidade e à simplicidade de cultivo em laboratório, C. micaceus e outros cogumelos coprinoides foram comuns em estudos citológicos nos séculos XIX e XX. O botânico alemão Johann Heinrich Friedrich Link relatou suas observações sobre a estrutura do himênio (a superfície fértil portadora de esporos) em 1809,[11] mas interpretou erroneamente o que viu. Link pensava que as estruturas microscópicas conhecidas hoje como basídios eram técas, comparáveis em forma aos ascos dos ascomicetos, e que cada téca continha quatro séries de esporos. Seus desenhos imprecisos do himênio de C. micaceus foram copiados em publicações micológicas subsequentes por outros autores, e só foi com o avanço da microscopia que os micólogos puderam determinar a verdadeira natureza dos basídios, quase três décadas depois, em 1837, quando Joseph-Henri Léveillé e August Corda publicaram independentemente descrições corretas da estrutura do himênio.[3] Em 1924, A. H. Reginald Buller publicou uma descrição e análise abrangentes dos processos de produção e liberação de esporos no terceiro volume de sua Researches on Fungi.[12]
Etimologia
O epíteto específico micaceus deriva da palavra em latim mica, que significa "migalha, grão de sal", e do sufixo -aceus, "semelhante a";[13] a aplicação moderna de "mica" a uma substância muito diferente vem da influência de micare, "brilhar".[14]
Descrição


O píleo tem inicialmente 1 a 2,5 cm de diâmetro, oval a cilíndrico, mas expande-se para se tornar campanulado (em forma de sino), às vezes com um umbo (protrusão central semelhante a um mamilo); finalmente, achata-se um pouco, tornando-se convexo. Quando expandido, o diâmetro do píleo atinge 0,8 a 5 cm, com a margem rasgada em raios e ligeiramente curvada para cima. A cor é amarelo-marrom ou bege, frequentemente com centro mais escuro, depois amarelo pálido ou bege da margem para dentro.[15] A margem do píleo é prominentemente sulcada quase até o centro; os sulcos marcam as posições das lamelas mais longas na parte inferior do píleo. Quando jovem, a superfície do píleo é coberta por partículas brancas ou esbranquiçadas brilhantes, remanescentes do véu universal que cobre exemplares imaturos.[16] As partículas estão frouxamente aderidas e são facilmente lavadas, de modo que exemplares mais velhos são frequentemente lisos.[17] Coprinellus micaceus é higrófana, assumindo cores diferentes dependendo de seu estado de hidratação.[18]
As lamelas estão densamente agrupadas e têm uma fixação adnexa (estreita) ao estipe.[19] Inicialmente brancas, mudam para marrom escuro e eventualmente preto à medida que os esporos amadurecem. A expansão do píleo faz com que as lamelas se abram ao longo de seus planos medianos, rasgando a margem do píleo em raios. O processo de liberação de esporos e autodigestão começa na base das lamelas antes que as partes superiores tenham se tornado completamente pretas.[20] O estipe frágil é oco e mede 3–10 cm de comprimento por 2–5 mm de espessura, e tem diâmetro aproximadamente uniforme ao longo do comprimento. É geralmente branco, mas pode descolorar para creme sujo pálido da base para cima.[15] A superfície do estipe é inicialmente aveludada com um pó esbranquiçado muito fino, mas isso eventualmente se desgasta, deixando-o mais ou menos liso. Os estipes podem ter um anel rudimentar na base, outro remanescente do véu universal.[21] A esporada é marrom escura ou preta.[22] A carne é fina, frágil, branca no estipe e marrom no píleo;[23] seu odor e sabor não são distintos.[24] Os basidiomas individuais levam em média cinco a sete dias para amadurecer completamente.[25]
Características microscópicas
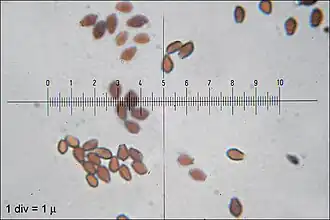
Os esporos de C. micaceus são vermelho-acastanhados ou pretos,[15] com dimensões de 7–10 por 4,5–6 μm. Geralmente, são lentiformes (em forma de lente bicôncava), mas vistos de lado parecem mais em forma de amêndoa ou fusiformes, enquanto em vista frontal parecem ovais ou mitriformes (aproximadamente na forma de uma mitra — um píleo pontudo). Os esporos têm um poro de germinação, uma área achatada no centro da superfície do esporo por onde um tubo germinativo pode emergir.[22] As células portadoras de esporos (os basídios) têm quatro esporos, forma de taco, e medem 10–15 por 4–7 μm.[26] Estudos mostraram que os basídios se desenvolvem em quatro gerações discretas. Os basídios da primeira geração são os mais proeminentes e se estendem a maior distância da superfície do himênio. As gerações subsequentes de basídios têm corpos mais curtos e menos proeminentes. Quando uma lamela viva é vista ao microscópio, os quatro conjuntos de basídios podem ser distinguidos claramente. Arthur Buller cunhou o termo inaequihymeniiferous para descrever esse modo de desenvolvimento himenial. O propósito dos tamanhos escalonados de basídios é facilitar a liberação de esporos do himênio. Há quatro zonas de liberação de esporos que correspondem aos quatro conjuntos de basídios, e basídios que liberaram todos os seus esporos começam rapidamente a se autodigerir. O arranjo escalonado minimiza a chance de colisão de esporos com basídios vizinhos durante a liberação.[27]
Os cistídios localizados na borda do píleo (queilocistídios) são esféricos e medem 30–120 por 20–74 μm. Os cistídios faciais (pleurocistídios) são em forma de taco ou elipses alongadas, com até 130–155 μm de comprimento. Os pleurocistídios protrudem da face da lamela e atuam como guardas, impedindo que lamelas adjacentes se toquem e também garantindo espaço suficiente para o desenvolvimento de basídios e esporos.[28] C. micaceus pode também ter caulocistídios espalhados (cistídios no estipe) de 60–100 por 5–10 μm, mas sua presença é variável e não pode ser usada de forma confiável para identificação.[26] Tanto De Bary quanto Buller, em suas investigações sobre a estrutura das cistídios, concluíram que há uma massa central de citoplasma formada onde numerosas placas finas de citoplasma se encontram no centro da célula. De Bary acreditava que as placas eram processos filamentosos ramificados,[29] mas Buller pensava que eram formadas em um processo semelhante às paredes de bolhas de espuma e que a massa central podia mudar lentamente de forma e posição alterando os volumes relativos dos vacúolos envolvidos pelas numerosas paredes citoplasmáticas finas. Em células mais velhas, o citoplasma pode se limitar à periferia da célula, com um grande vacúolo ocupando o centro.[30]
As células globulares que formam as escamas semelhantes à mica no píleo são incolores, de parede lisa e variam de cerca de 25–65 μm, embora a maioria esteja entre 40 e 50 μm.[20] Buller explicou o "brilho" dessas células da seguinte forma: "O brilho das células farináceas, assim como das cistídios nas bordas e faces das lamelas, deve-se simplesmente à luz que as atinge de fora e é refratada e refletida para o olho da mesma maneira que das mínimas gotas de água que se vêem frequentemente nas pontas das folhas de grama em gramados ingleses no início da manhã após uma noite de orvalho."[31]
Em 1914, Michael Levine foi o primeiro a relatar com sucesso o cultivo de C. micaceus a partir de esporos em laboratório. Em seus experimentos, os basidiomas apareceram cerca de 40 a 60 dias após a inoculação inicial do meio de crescimento (ágar suplementado com solo, esterco de cavalo ou fubá) com esporos.[32] Como outras espécies coprinoides, C. micaceus sofre meiose síncrona. Os cromossomos são facilmente discerníveis com microscopia de luz e todos os estágios meióticos são bem definidos. Essas características tornaram a espécie uma ferramenta útil em investigações laboratoriais de citogenética de basidiomicetos.[33][34] O número cromossômico de C. micaceus é n=12.[35]
As características microscópicas e a citogenética de C. micaceus são bem conhecidas e a espécie tem sido frequentemente usada como organismo modelo para estudar divisão celular e meiose em basidiomicetos.[33][34]
Espécies semelhantes
Coprinopsis variegata tem píleo marrom-acinzentado com escamas brancas opacas a amarronzada; seu odor é desagradável. Coprinellus disseminatus (comestível) tem píleos menores, amarelo-marrons a marrom-acinzentado e lamelas brancas que escurecem para preto, mas não se dissolvem; cresce sempre em grandes aglomerados sobre madeira podre (às vezes madeira enterrada).[36] Coprinopsis atramentaria é uma espécie maior,[37] cinzenta, que cresce em aglomerados densos sobre tocos ou no solo a partir de madeira enterrada, carece de partículas reluzentes no píleo, e o píleo e as lamelas se dissolvem na maturidade. Coprinellus radians desenvolve-se isolada ou em aglomerados sobre madeira, a partir de um tapete tufado de micélio amarelo-alaranjado grosso.[38] Coprinellus truncorum também é coberta por grânulos reluzentes e é considerada quase indistinguível de C. micaceus no campo; a microscopia é necessária para diferenciar, uma vez que C. truncorum tem esporos elipsoides com poro de germinação arredondado, em comparação aos esporos mitriformes com poros de germinação truncados de C. micaceus.[39] Um estudo sugere que, em comparação a C. truncorum, C. micaceus é mais marrom no centro do píleo (em vez de cinzento) e tem maior tendência a crescer em aglomerados; mas mais evidências moleculares são necessárias para determinar se os dois táxons são geneticamente idênticos.[26] C. flocculosus é outra espécie semelhante.[15]
Ecologia, habitat e distribuição
Coprinellus micaceus é uma espécie saprófita, obtendo nutrientes de matéria orgânica morta e em decomposição, e cresce em e ao redor de tocos ou troncos de árvores de folha larga ou aderido a madeira enterrada. Prefere se alimentar de casca, particularmente o floema secundário, em vez da madeira.[40] No esquema da sucessão ecológica de espécies fúngicas envolvidas na decomposição de madeira, C. micaceus é um colonizador de estágio tardio, e prefere se alimentar de madeira que já se decompôs suficientemente para atingir "uma consistência friável e amolecida".[41] Um estudo de 2010 sugere que o fungo também pode viver como endófito, habitando o tecido lenhoso de árvores saudáveis sem causar sintomas de doença.[42] O fungo também está associado a solos perturbados ou desenvolvidos, como margens de estradas e trilhas, jardins, canteiros de obras e bordas de estacionamentos;[21] também foi observado crescendo em ambientes internos sobre madeira podre em condições úmidas.[21] Em um caso, foi descoberto a cerca de 120 m de profundidade em uma mina de carvão abandonada, crescendo sobre passarelas e suportes de madeira usados para sustentar o teto.[43]

Os basidiomas são comumente encontrados crescendo em aglomerados densos, mas também podem ser encontrados isolados ou em pequenos grupos, especialmente em áreas florestadas.[18] Na América do Norte, C. micaceus é um dos primeiros cogumelos comestíveis a aparecer na primavera[24] e frutifica de abril a setembro. Na Europa, frutifica de maio a dezembro.[44] Embora possa crescer em qualquer época do ano, é mais prevalente na primavera e outono, coincidindo com a maior umidade resultante das chuvas primaveris e outonais.[38] Um estudo de qualidade do ar realizado na cidade de Santiago de Compostela, na Península Ibérica, concluiu que a maioria dos esporos de "Coprinus" presentes na atmosfera pertenciam a C. micaceus, e que o número de esporos aumentava com a maior umidade relativa e precipitação, mas diminuía com temperaturas mais altas.[45] A espécie é conhecida por reaparecer com frutificações sucessivas no mesmo local. Em um caso, um total de 17 kg de cogumelos frescos foram coletados de um toco de ulmeiro em 10 colheitas sucessivas ao longo de uma primavera e verão.[46][47]
Coprinellus micaceus tem distribuição cosmopolita,[23] e foi coletada no norte da África,[48] África do Sul,[49] Europa (incluindo Turquia),[50] América do Norte (até o Alasca),[51] ilhas do Havaí,[26][39] América do Sul,[26] Índia,[52][53] Austrália,[44] Nova Zelândia,[54] e Japão.[55] Análise filogenética de sequências de rDNA de exemplares coletados no sudeste da Ásia e Havaí mostra que as populações havaianas formam um clado distinto com pouca diversidade genética em comparação às populações asiáticas; isso sugere que as populações havaianas foram introduzidas relativamente recentemente e não tiveram muito tempo para desenvolver variação genética.[56] Um estudo sugere que na África do Sul, onde C. micaceus é rara, tem sido frequentemente confundida com a semelhante C. truncorum, uma espécie mais comum naquela região. Uma inferência semelhante foi levantada sobre espécies norte-americanas.[51][57]
Comestibilidade
Coprinellus micaceus é uma espécie comestível,[19][58] e o cozimento inativa as enzimas que causam autodigestão ou deliquescência — um processo que pode começar tão cedo quanto uma hora após a coleta.[59] É considerado bom para omeletes[23] e como tempero para molhos,[60] embora seja "uma espécie muito delicada, facilmente estragada por cozimento excessivo".[44] O sabor é tão delicado que é fácil sobrecarregá-lo e escondê-lo com quase qualquer coisa. O cogumelo também atrai moscas do gênero Drosophila, que frequentemente usam os basidiomas como hospedeiros para produção de larvas.[61][62]
Um estudo dos conteúdos minerais de vários cogumelos comestíveis descobriu que C. micaceus continha a maior concentração de potássio entre as 34 espécies testadas, próxima a 0,5 grama de potássio por quilograma de cogumelo.[63] Como a espécie pode bioacumular metais pesados prejudiciais como chumbo e cádmio, recomenda-se restringir o consumo de cogumelos coletados à beira de estradas ou outros locais de coleta que possam estar expostos a ou conter poluentes.[64]
Compostos bioativos
Pesquisas sobre a química de produtos naturais de Coprinellus micaceus revelaram a presença de vários compostos químicos únicos da espécie. O micaceol é um esterol com atividade antibacteriana "modesta" contra os patógenos Corynebacterium xerosis e Staphylococcus aureus. O composto (Z,Z)-4-oxo-2,5-heptadienodioico tem atividade inibitória contra a glutationa S-transferase, uma enzima implicada na resistência de células cancerígenas a agentes quimioterápicos, especialmente drogas alquilantes.[65][66] Um estudo de 2003 não encontrou atividade antibacteriana nesta espécie.[67] Uma publicação de 1962 relatou a presença do composto indol biologicamente ativo triptamina em C. micaceus, embora a concentração não tenha sido determinada.[68] Os basidiomas também produzem uma variedade de compostos pigmentados conhecidos como melaninas — polímeros químicos complexos que contribuem para a formação de húmus do solo após a desintegração dos basidiomas.[69] C. micaceus foi encontrada desprovida da toxina coprina, o químico mimetizador de dissulfiram encontrado em C. atramentaria que causa mal-estar quando consumido simultaneamente com álcool.[70]
Ver também
- Coprinopsis atramentaria
- Coprinopsis variegata
- Parasola auricoma
- Psathyrella corrugis
- Tulosesus impatiens
Referências
- ↑ «Species synonymy – Coprinellus micaceus». Index Fungorum. CAB International. 2008. Consultado em 22 de outubro de 2025
- ↑ Fungorum in Pannoniis observatorum brevis historia (Breve história de fungos observados na Panônia [Hungria]), gênero XVI, p. cclxxxii.
- ↑ a b Buller, 1924, p. 331.
- ↑ Bulliard JBF (1786). Herbier de la France [Guide to the Herbs of France] (em francês). 6. [S.l.: s.n.] pp. 241–88, plate 246.
- ↑ Persoon CH (1801). Synopsis Methodica Fungorum (Göttingen) (em latim). 1. [S.l.: s.n.] p. 403
- ↑ Fries EM (1838). Epicrisis Systematis Mycologici (em latim). Uppsala, Sweden: W.G. Farlow. p. 247
- ↑ Singer R. (1986). The Agaricales in Modern Taxonomy 4th ed. Königstein im Taunus, Germany: Koeltz Scientific Books. p. 522. ISBN 3-87429-254-1
- ↑ Hopple JS, Vilgalys R (1994). «Phylogenetic relationships among coprinoid taxa and allies based on data from restriction site mapping of nuclear rDNA» (PDF). Mycologia. 86 (1): 96–107. JSTOR 3760723. doi:10.2307/3760723. Consultado em 22 de outubro de 2025
- ↑ Park DS, Go SJ, Kim YS, Seok SJ, Song JK, Yeo YS, Ryu JC, Sung JM (1999). «Genetic relationships of Coprinus spp. on the basis of sequences in ITS II region». Korean Journal of Mycology (em coreano). 27 (1): 27–31. ISSN 0253-651X
- ↑ Redhead SA, Vilgalys R, Moncalvo J-M, Johnson J, Hopple JS Jr (2001). «Coprinus Pers. and the disposition of Coprinus species sensu lato». Taxon. 50 (1): 203–41. Bibcode:2001Taxon..50..203R. JSTOR 1224525. doi:10.2307/1224525
- ↑ Link HF (1809). «Nova plantarum genera e classe Lichenum, Algarum, Fungorum». Schrader's Neues Journal für die Botanik. 3: 10–15
- ↑ Buller, 1924, pp. 328–56.
- ↑ Stearn WT (1973). Botanical Latin 2nd annot. and rev. ed. Newton Abbot: David & Charles. pp. 379, 463
- ↑ Oxford English Dictionary Online. Oxford: Oxford University Press. 2010. Consultado em 22 de outubro de 2025. Cópia arquivada em 25 de junho de 2006 ss. vv. "mica", "micaceous".
- ↑ a b c d Davis, R. Michael; Sommer, Robert; Menge, John A. (2012). Field Guide to Mushrooms of Western North America. Berkeley: University of California Press. pp. 205–206. ISBN 978-0-520-95360-4. OCLC 797915861
- ↑ Evenson VS (1997). Mushrooms of Colorado and the Southern Rocky Mountains. [S.l.]: Westcliffe Publishers. p. 131. ISBN 978-1-56579-192-3
- ↑ Buller, 1924, p. 335.
- ↑ a b McKnight VB, McKnight KH (1987). A Field Guide to Mushrooms, North America. Boston: Houghton Mifflin. p. 34. ISBN 0-395-91090-0
- ↑ a b Orr DB, Orr RT (1979). Mushrooms of Western North America. Berkeley, California: University of California Press. p. 176. ISBN 0-520-03656-5
- ↑ a b Buller, 1924, p. 337.
- ↑ a b c Arora, David (1986). Mushrooms Demystified: A Comprehensive Guide to the Fleshy Fungi 2nd ed. Berkeley, CA: Ten Speed Press. pp. 348–49. ISBN 978-0-89815-170-1
- ↑ a b Orton PD, Watling R (1979). Coprinaceae: Coprinus. Edinburgh, Scotland: Royal Botanic Garden. pp. 54–55. ISBN 0-11-491565-2
- ↑ a b c Schalkwijk-Barendsen HME. (1991). Mushrooms of Western Canada. Edmonton, Canada: Lone Pine Publishing. p. 334. ISBN 0-919433-47-2
- ↑ a b Roody WC (2003). Mushrooms of West Virginia and the Central Appalachians. Lexington, Kentucky: University Press of Kentucky. p. 156. ISBN 0-8131-9039-8
- ↑ Pady SM (1941). «Notes on Coprinus micaceus growing in an unusual habitat». Mycologia. 33 (4): 411–14. JSTOR 3754895. doi:10.2307/3754895
- ↑ a b c d e Keirle MR, Hemmes DE, Desjardin DE (2004). «Agaricales of the Hawaiian Islands. 8. Agaricaceae: Coprinus and Podaxis; Psathyrellaceae: Coprinopsis, Coprinellus and Parasola» (PDF). Fungal Diversity. 15 (4): 33–124
- ↑ Buller, 1924, pp. 351–53.
- ↑ Buller, 1924, pp. 329, 342.
- ↑ De Bary A. (1873). «On cystidia». Grevillea. 1: 181–83
- ↑ Buller, 1924, pp. 248–50.
- ↑ Buller, 1924, p. 340.
- ↑ Levine M. (1914). «The origin and development of the lamellae of Coprinus micaceus». American Journal of Botany. 1 (7): 343–56. JSTOR 2435139. doi:10.2307/2435139
- ↑ a b Bos CJ (1996). Fungal Genetics: Principles and Practice. New York: Marcel Dekker. pp. 152–53. ISBN 0-8247-9544-X
- ↑ a b Moore D, Chiu S-W (1996). Patterns in Fungal Development. Cambridge, UK: Cambridge University Press. p. 127. ISBN 0-521-56047-0
- ↑ Lu BC, Raju NB (1970). «Meiosis in Coprinus. II. Chromosome pairing and the lampbrush diplotene stage of meiotic prophase». Chromosoma (Berlin). 29 (3): 305–16. PMID 5445348. doi:10.1007/BF00325945
- ↑ Sundberg W, Bessette A (1987). Mushrooms: A Quick Reference Guide to Mushrooms of North America (Macmillan Field Guides). New York: Collier Books. p. 134. ISBN 0-02-063690-3
- ↑ Trudell, Steve; Ammirati, Joe (2009). Mushrooms of the Pacific Northwest. Col: Timber Press Field Guides. Portland, OR: Timber Press. 196 páginas. ISBN 978-0-88192-935-5
- ↑ a b Healy RA, Huffman DR, Tiffany LH, Knaphaus G (2008). Mushrooms and Other Fungi of the Midcontinental United States (Bur Oak Guide). Iowa City, Iowa: University of Iowa Press. p. 63. ISBN 978-1-58729-627-7
- ↑ a b Hemmes DE, Desjardin D (2002). Mushrooms of Hawai'i: An Identification Guide. Berkeley, California: Ten Speed Press. p. 127. ISBN 1-58008-339-0
- ↑ Buller, 1924, p. 333.
- ↑ Peiris D, Dunn WB, Brown M, Kell DB, Roy I, Hedger JN (2008). «Metabolite profiles of interacting mycelial fronts differ for pairings of the wood decay basidiomycete fungus, Stereum hirsutum with its competitors Coprinus micaceus and Coprinus disseminatus». Metabolomics. 4 (1): 52–62. doi:10.1007/s11306-007-0100-4
- ↑ de Errasti A, Carmarán CC, Novas MV (2010). «Diversity and significance of fungal endophytes from living stems of naturalized trees from Argentina». Fungal Diversity. 40 (1): 29–40. doi:10.1007/s13225-009-0012-x
- ↑ Atkinson GF (1898). «Society for Plant Morphology and Physiology. 2. Studies on some mycelium and fungi from a coal mine». Botanical Gazette. 25 (2): 106–18. JSTOR 2464466. doi:10.1086/327641
- ↑ a b c Dickinson C, Lucas J (1982). VNR Color Dictionary of Mushrooms. New York: Van Nostrand Reinhold. p. 78. ISBN 978-0-442-21998-7
- ↑ Aira MJ, Rodriguez-Rajo FJ, Castro M, Jato V (2009). «Characterization of Coprinus spores in the NW of the Iberian Peninsula. Identification and count in aerobiological samples». Cryptogamie, Mycologie. 30 (1): 57–66
- ↑ Christensen CM (1981). Edible Mushrooms. Minnesota, Minneapolis: University of Minnesota Press. p. 80. ISBN 978-0-8166-1049-5
- ↑ Stewart FC (1926). «The mica ink-cap or glistening Coprinus». New York (Geneva) Agricultural Experiment Station Bulletin. 535: 1–30
- ↑ Melchers LE (1931). «A check list of plant diseases and fungi occurring in Egypt». Transactions of the Kansas Academy of Science. 34: 41–106. JSTOR 3624470. doi:10.2307/3624470
- ↑ Reid DA, Eicker A (1999). «South African fungi 10: New species, new records and some new observations». Mycotaxon. 73: 169–97
- ↑ Gezer K, Ekici FT, Turkoglu A (2008). «Macrofungi of Karci Mountain (Denizli, Turkey)». Turkish Journal of Botany. 32 (1): 91–6. ISSN 1300-008X
- ↑ a b Watling R, Miller OK (1971). «8 species of Coprinus of Yukon Territory and adjacent Alaska». Canadian Journal of Botany. 49 (9): 1687–90. doi:10.1139/b71-237
- ↑ Kaul TN, Kachroo JL (1974). «Common edible mushrooms of Jammu and Kashmir India». Journal of the Bombay Natural History Society. 71 (1): 26–31
- ↑ Manjula R, Surjit S, Dutta BB, Krishnendu A (2005). «Some additions to the Coprinaceae of Sikkim Himalaya». Journal of Mycopathological Research. 43 (1): 101–03. ISSN 0971-3719
- ↑ Crowe A. (1983). A Field Guide to the Native Edible Plants of New Zealand : including Those Plants Eaten by the Maori. [S.l.]: Collins. p. 135. ISBN 0-00-216983-5
- ↑ Uljé, K. «Coprinus micaceus». Kees Uljé Coprinus site. Consultado em 22 de outubro de 2025
- ↑ Ko KS. (2001). «Phylogeographic divergences of nuclear ITS sequences in Coprinus species sensu lato». Mycological Research. 105 (12): 1519–26. doi:10.1017/S0953756201005184
- ↑ Kuo M. (fevereiro de 2008). «Coprinellus micaceus». MushroomExpert.Com. Consultado em 22 de outubro de 2025
- ↑ Russell B. (2006). Field Guide to Wild Mushrooms of Pennsylvania and the Mid-Atlantic. University Park, Pennsylvania: Pennsylvania State University Press. p. 29. ISBN 978-0-271-02891-0
- ↑ Smith AH (1975). A Field Guide to Western Mushrooms. Ann Arbor, Michigan: University of Michigan Press. p. 229. ISBN 0-472-85599-9
- ↑ Ammirati JF, McKenny M, Stuntz DE (1987). The New Savory Wild Mushroom. Seattle, Washington: University of Washington Press. p. 156. ISBN 0-295-96480-4
- ↑ Kimura MT (1980). «Evolution of food preferences in fungus-feeding Drosophila: an ecological study» (PDF). Evolution. 34 (5): 1009–18. JSTOR 2408009. PMID 28581130. doi:10.2307/2408009
- ↑ Toda MJ, Kimura MT, Tuno N (1999). «Coexistence mechanisms of mycophagous drosophilids on multispecies fungal hosts: aggregation and resource partitioning» (PDF). Journal of Animal Ecology. 68 (4): 794–803. Bibcode:1999JAnEc..68..794T. JSTOR 2647329. doi:10.1046/j.1365-2656.1999.00328.x

- ↑ Dursun N, Ozcan MM, Ozturk C (2006). «Mineral contents of 34 species of edible mushrooms growing wild in Turkey». Journal of the Science of Food and Agriculture. 86 (7): 1087–94. Bibcode:2006JSFA...86.1087D. doi:10.1002/jsfa.2462
- ↑ Das N. (2007). «Heavy metal levels in wild edible mushroom samples from Nayagram Block of Midnapore District, West Bengal». Indian Forester. 133 (2): 171–78
- ↑ Zahid S, Udenigwe CC, Ata A, Eze MO, Segstro EP, Holloway P (2006). «New bioactive natural products from Coprinus micaceus». Natural Product Research. 20 (14): 1283–89. PMID 17393652. doi:10.1080/14786410601101829
- ↑ Ata A. (2009). «Novel bioactive natural products from marine and terrestrial sources». In: Şener B. Innovations in Chemical Biology. Dordrecht, The Netherlands: Springer Netherlands. pp. 51–60. ISBN 978-1-4020-6954-3. doi:10.1007/978-1-4020-6955-0
- ↑ Efremenkova OV, Ershova EY, Tolstych IV, Zenkova VA, Dudnik YV (2003). «Antimicrobial activity of medicinal mushrooms from the genus Coprinus (Fr.) S. F. Gray (Agaricomycetideae)». International Journal of Medicinal Mushrooms. 5 (1): 37–41. doi:10.1615/InterJMedicMush.v5.i1
- ↑ Worthen LR, Stessel GJ, Youngken HW (1962). «The occurrence of indole compounds in Coprinus species». Economic Botany. 16 (4): 315–18. Bibcode:1962EcBot..16..315W. doi:10.1007/BF02860190
- ↑ Saiz-Jimenez C. (1983). «The chemical nature of the melanins from Coprinus spp.». Soil Science. 136 (2): 65–74. Bibcode:1983SoilS.136...65S. doi:10.1097/00010694-198308000-00001. hdl:10261/76183

- ↑ Brossi A. (1991). The Alkaloids: Chemistry and Pharmacology. 40. Amsterdam, the Netherlands: Elsevier. p. 298. ISBN 0-12-469540-X
Bibliografia
- Buller AH (1924). «Chapter XI: The micaceus sub-type illustrated by Coprinus micaceus». Researches on Fungi. III. London: Longmans, Green, and Co. pp. 328–56

