Cafileria
Cafileria
| |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
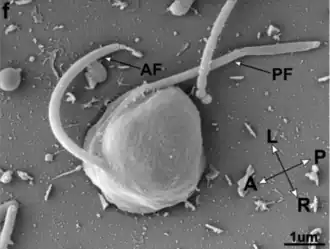 Imagem de Cafileria marina obtida por microscópio eletrônico de varredura. AF: flagelo anterior; PF: flagelo posterior; L: esquerda; R: direita; A: anterior; P: posterior. | |||||||||||||||||
| Classificação científica | |||||||||||||||||
| |||||||||||||||||
| Nome binomial | |||||||||||||||||
| Cafileria marina Jirsová, Füssy, Richtová, Gruber & Oborník 2019[1] | |||||||||||||||||
Cafileria é um gênero de protistas marinhos microscópicos. É monotípico, compreendendo apenas a espécie Cafileria marina, descrita em 2019 a partir de amostras coletadas na Noruega. Pertence a um clado de flagelados heterotróficos que consomem bactérias, conhecido como Bicosoecida, uma linhagem basal de Stramenopiles. Devido ao seu pequeno tamanho, é classificado como um nanoflagelado. É o único organismo no qual foram observadas conexões diretas entre mitocôndrias e o núcleo celular. Outra peculiaridade de C. marina é a mudança na forma do complexo de Golgi durante o ciclo celular.[1]
Descoberta
As células de Cafileria marina foram coletadas de uma comunidade de tapete de algas em uma superfície rochosa no fiorde Kvernesfjorden [en], Noruega. Sua morfologia, ultraestrutura, aparelho flagelar e genoma mitocondrial foram analisados. Os resultados, juntamente com a descrição taxonômica formal de Cafileria marina, foram publicados em 2019 por pesquisadores tchecos Dagmar Jirsová, Zoltán Füssy, Jitka Richtová, Ansgar Gruber e Miroslav Oborník.[1]
O hapantótipo de C. marina foi depositado sob o nome IP CAS Pro 59 na coleção de lâminas do Centro Biológico da Academia Tcheca de Ciências [en] em České Budějovice, República Tcheca.[1]
Etimologia
O nome Cafileria deriva de kafilerie, termo em tcheco para uma fábrica de graxaria onde biomassa de origem animal é transformada em lipídios, adesivos e fertilizantes. De maneira semelhante, Cafileria consome bactérias e recicla materiais orgânicos presentes em seu habitat de biofilme. O epíteto específico marina refere-se à origem marinha da espécie.[1]
Estrutura celular
Aparência externa
As células de C. marina têm a forma de um "D", com o lado direito arredondado e o esquerdo achatado. O corpo celular mede 3–4 μm de largura e 5–6 μm de comprimento, classificando-a como um nanoflagelado devido ao tamanho. A superfície celular é lisa, sem características visíveis (como lorica ou parede celular) sob microscopia óptica ou microscopia eletrônica de varredura. Como outros membros da ordem Bicosoecida, possui dois flagelos lisos (anterior e posterior), com comprimento de aproximadamente 1,5 a 2 vezes o tamanho do corpo celular. Os flagelos estão em posição subapical e emergem de uma depressão na face ventral.[1]
Organelas
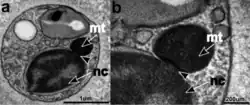
As células de C. marina posicionam o núcleo celular e as mitocôndrias com cristas tubulares (comuns em Stramenopiles) na parte anterior da célula. Um fenômeno peculiar em C. marina é que, em culturas microbiológicas jovens (com até 2 semanas), o núcleo e as mitocôndrias estão intimamente conectados por junções. Embora o agrupamento de mitocôndrias próximo ao núcleo seja observado em tecidos de mamíferos,[2][3] esta é a primeira vez que uma conexão completa entre esses compartimentos celulares [en] foi descrita. Foram hipotetizadas várias funções para essa conexão peculiar:
- (i) permitir a troca de ATP/ADP entre as duas organelas, fornecendo a energia necessária ao núcleo,
- (ii) facilitar o transporte de tRNA nuclear necessário, que as mitocôndrias não produzem,
- (iii) transportar mRNA para ser traduzido nas mitocôndrias,
- (iv) segregar igualmente as mitocôndrias para as células-filhas após a mitose,
- (v) ou simplesmente otimizar o uso do espaço limitado em uma célula pequena.[1]
O complexo de Golgi está na parte anterior da célula, com suas 4–5 cisternas alinhadas paralelamente ao envoltório nuclear. Durante o ciclo celular, a forma das cisternas do complexo de Golgi muda de empilhadas planas para arredondadas: as cisternas planas curvam-se para dentro, formando estruturas arredondadas e ocas. Um fenômeno semelhante ocorre em células de mamíferos, associado a mudanças no metabolismo de esfingomielina,[4] mas no caso de Cafileria, o mecanismo responsável é desconhecido.[1]
Várias vesículas pequenas estão espalhadas pelo citosol, enquanto vacúolos alimentares são significativamente maiores e localizados na parte posterior da célula, ocupando quase um terço de seu volume. Alguns vacúolos alimentares podem conter bactérias intactas ou parcialmente digeridas.[1]
Aparelho flagelar
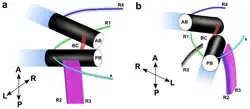
C. marina possui dois flagelos fixados a quatro raízes de microtúbulos. Existem dois corpos basais na parte anterior da célula, posicionados em um ângulo de 45° entre si, conectados por uma fibra estriada. Cada flagelo possui uma estrutura de axonema com dois microtúbulos centrais e um círculo de nove microtúbulos ao redor. As quatro raízes (denominadas R1, R2, R3 e R4) possuem 8, 3, 1 e 1 microtúbulos, respectivamente, uma configuração única para C. marina.[1]
Ecologia e comportamento celular
Cafileria marina vive em associação próxima com uma espécie não identificada de alga da classe Pelagophyceae. Ela se desloca por deslizamento através da mucilagem secretada pela alga. Durante o movimento, exibe uma rotação, com o flagelo anterior movendo-se livremente enquanto o posterior atua como âncora, fixado à superfície. Alimenta-se continuamente por fagotrofia, com um citostoma permanente; não foram observados estágios de repouso ou esporos.[1]
Características genéticas
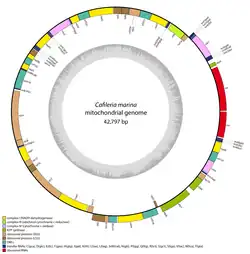
O genoma mitocondrial de C. marina tem 42.797 pares de bases, com um conteúdo GC de 21,3% (guanina-citosina), significativamente menor que outros genomas mitocondriais de Stramenopiles heterotróficos.[1]
O código genético do genoma mitocondrial é um incomum código tipo 4, encontrado em diferentes grupos procariontes e eucariontes, no qual o códon UGA codifica o aminoácido triptofano e os códons UAA/UAG são códons de terminação. O genoma mitocondrial também é incomum por não conter íntrons do grupo I ou do grupo II, comuns em outras mitocôndrias.[1]
O genoma mitocondrial contém genes para todos os tRNAs, exceto para treonina, alanina e glicina — que são transportados por tRNAs nucleares —, genes de unidade grande e unidade pequena de RNA ribossômico organizados em tandem, e genes codificadores de proteínas para subunidades de vários complexos: complexos respiratórios (I, III e IV), ATP sintase, e a porção proteica das subunidades grande e pequena de ribossomos. Apesar de ter um conteúdo genético semelhante a outros Stramenopiles heterotróficos, a ordem dos genes em C. marina é altamente reorganizada. Por exemplo, é a única espécie de Stramenopiles conhecida por codificar o gene nad11 (uma subunidade de NADH-ubiquinona oxidorredutase) com domínios 4Fe–4S no módulo N-terminal do tipo ferredoxina, em vez do módulo C-terminal do tipo molibdopterina, embora as consequências dessa mudança sejam incertas.[1]
Relações evolutivas
Cafileria pertence à linhagem Bicosoecida, um clado basal de Stramenopiles, mas sua posição dentro desse grupo ainda não está clara. De acordo com o estudo que descreveu Cafileria marina em 2019, análises filogenéticas e morfológicas agrupam a família Cafeteriidae como o parente mais próximo de Cafileria marina, com Caecitellus como o grupo-irmão de C. marina, embora os autores afirmem que "mais investigações são [...] necessárias para confirmar essa afirmação".[1] Uma análise posterior de 2022 posicionou Cafileria fora da ordem Anoecida [en]; como os autores destacaram, "a resolução filogenética de Bicosoecida ainda é uma questão em andamento".[5]
| Filogenia em 2019[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
| Filogenia em 2022[5] | |||||||||||||||||||||||||||||||||||||||
|
Referências
- ↑ a b c d e f g h i j k l m n o p Jirsová D, Füssy Z, Richtová J, Gruber A, Oborník M (2019). «Morphology, Ultrastructure, and Mitochondrial Genome of the Marine Non-Photosynthetic Bicosoecid Cafileria marina Gen. et sp. nov.». Microorganisms. 7 (8). 240 páginas. PMC 6723347
 . PMID 31387253. doi:10.3390/microorganisms7080240
. PMID 31387253. doi:10.3390/microorganisms7080240
- ↑ Dzeja PP, Bortolon R, Perez-Terzic C, Holmuhamedov EL, Terzic A (Julho de 2002). «Energetic communication between mitochondria and nucleus directed by catalyzed phosphotransfer». Proc. Natl. Acad. Sci. USA. 99 (15): 10156–10161. Bibcode:2002PNAS...9910156D. PMC 126640
 . PMID 12119406. doi:10.1073/pnas.152259999
. PMID 12119406. doi:10.1073/pnas.152259999
- ↑ Al-Mehdi AB, Pastukh VM, Swiger BM, Reed DJ, Patel MR, Bardwell GC, Pastukh VV, Alexeyev MF, Gillespie MN (Julho de 2012). «Perinuclear mitochondrial clustering creates an oxidant-rich nuclear domain required for hypoxia-induced transcription». Science Signaling. 5 (231): ra47. PMC 3565837
 . PMID 22763339. doi:10.1126/scisignal.2002712
. PMID 22763339. doi:10.1126/scisignal.2002712
- ↑ Campelo F, van Galen J, Turacchio G, Parashuraman S, Kozlov MM, Garcia-Parajo MF, Malhotra V (Maio de 2017). «Sphingomyelin metabolism controls the shape and function of the Golgi cisternae». eLife. 6: e24603. PMC 5462544
 . PMID 28500756. doi:10.7554/eLife.24603
. PMID 28500756. doi:10.7554/eLife.24603
- ↑ a b Schoenle A, Hohlfeld M, Rybarski A, Sachs M, Freches E, Wiechmann K, Nitsche F, Arndt H (2022). «Cafeteria in extreme environments: Investigations on C. burkhardae and three new species from the Atacama Desert and the deep ocean». European Journal of Protistology. 85. 125905 páginas. PMID 35868212. doi:10.1016/j.ejop.2022.125905