Acetil-CoA carboxilase
| Acetyl-CoA carboxylase | |
|---|---|
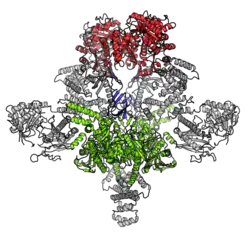 |
A acetil-CoA carboxilase (ACC) é uma enzima dependente de biotina (EC 6.4.1.2) que catalisa a carboxilação irreversível da acetil-CoA para produzir malonil-CoA através das suas duas atividades catalíticas: biotina carboxilase (BC) e carboxiltransferase (CT). A ACC é uma enzima multissubunidade encontrada na maioria dos procariontes e nos cloroplastos da maioria das plantas e algas, enquanto é uma grande enzima multidomínio encontrada no citoplasma da maioria dos eucariontes. A função mais importante da ACC é fornecer o substrato enzimático malonil-CoA para a biossíntese de ácidos gordos.[1] A atividade da ACC pode ser controlada a nível transcricional, bem como por moduladores de pequenas moléculas e modificação covalente. O genoma humano contém genes para duas ACC diferentes,[2] denominados ACACA[3] e ACACB.[4]
Estrutura
As procariontes e as plantas possuem ACCs multissubunitárias compostas por vários polipeptídeos. A atividade da biotina carboxilase (BC), a proteína transportadora de carboxila da biotina (BCCP) e a atividade da carboxiltransferase (CT) estão contidas em diferentes subunidades. A estequiometria destas subunidades na holoenzima ACC difere entre organismos.[1] Nos humanos e na maioria dos eucariontes, uma ACC evoluiu com domínios catalíticos proteínas CT e BC e BCCP localizados num único polipeptídeo. A maioria das plantas também possui esta forma homomérica no citosol.[5] As regiões funcionais da ACC, começando na extremidade N-terminal e terminando na extremidade C-terminal, são: biotina carboxilase (BC), ligação à biotina (BB), carboxiltransferase (CT) e motivo de ligação ao ATP (AB). A região AB está localizada dentro da BC. A biotina está ligada covalentemente, através de uma ligação amida, à longa cadeia lateral de um resíduo de lisina na BB. Como a BB está entre as regiões BC e CT, a biotina pode translocar-se facilmente para ambos os sítios ativos quando necessário.
Nos mamíferos, onde são expressas duas isoformas da ACC, a principal diferença estrutural entre elas é a extensão da extremidade N-terminal da ACC2, que contém uma sequência de direccionamento mitocondrial.[1]
- Estruturas cristalográficas da acetil-CoA carboxilase de E. coli
-
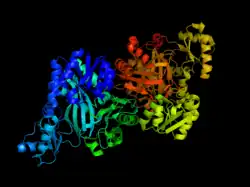 Subunidade biotina carboxilase da acetil-CoA carboxilase de E. coli.
Subunidade biotina carboxilase da acetil-CoA carboxilase de E. coli. -
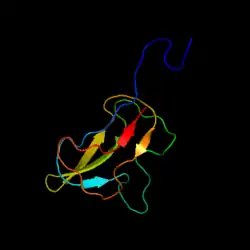 Subunidade da proteína transportadora de biotina carboxilo a acetil-CoA carboxilase de E. coli.
Subunidade da proteína transportadora de biotina carboxilo a acetil-CoA carboxilase de E. coli. -
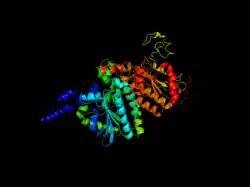 Subunidade carboxil transferase da acetil-CoA carboxilase de E. coli.
Subunidade carboxil transferase da acetil-CoA carboxilase de E. coli.
Genes
Os polipeptídeos que constituem a ACCS multissubunidade dos procariontes e das plantas são codificados por genes diferentes. Em Escherichia coli, o gene accA codifica a subunidade alfa da acetil-CoA carboxilase,[6] e o accD a sua subunidade beta.[7]
Mecanismo
A reação global ACAC(A,B) ocorre através de um mecanismo de duas etapas.[8] A primeira reação é realizada pela BC e envolve a carboxilação ATP-dependente da biotina com o bicarbonato a funcionar como fonte de CO2. O grupo carboxilo é transferido da biotina para o acetil-CoA para formar malonil-CoA na segunda reação, que é catalisada pela CT.
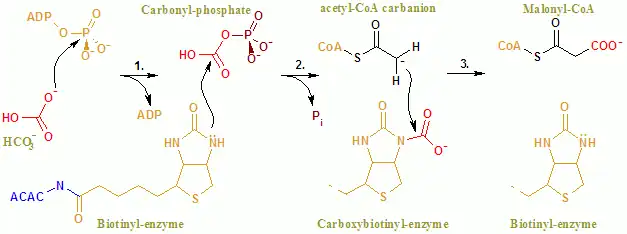
No sítio ativo, a reação prossegue com uma extensa interação dos resíduos Glu296 e dos resíduos Arg338 e Arg292, carregados positivamente, com os substratos.[9] Dois iões Mg²⁺ estão coordenados pelos grupos fosfato da adenosina trifosfato (ATP) e são necessários para a ligação do ATP à enzima. O bicarbonato é desprotonado pelo Glu296, embora em solução esta transferência de protões seja improvável, dado que o pKa do bicarbonato é de 10,3. Aparentemente, a enzima manipula o pKa para facilitar a desprotonação do bicarbonato. O pKa do bicarbonato é diminuído pela sua interação com as cadeias laterais carregadas positivamente da Arg338 e da Arg292. Além disso, o Glu296 interage com a cadeia lateral do Glu211, uma interação que provoca um aumento aparente do pKa. Após a desprotonação do bicarbonato, o oxigénio do bicarbonato atua como nucleófilo e ataca o fosfato gama do ATP. O intermediário carboxifosfato decompõe-se rapidamente em CO₂ e PO₄³⁻. O PO₄³⁻ desprotona a biotina, criando um enolato, estabilizado pela Arg338, que ataca então o CO₂, resultando na produção de carboxibiotina. A carboxibiotina é translocada para o sítio ativo da carboxiltransferase (CT), onde o grupo carboxilo é transferido para a acetil-CoA. Ao contrário do domínio BC, pouco se sabe sobre o mecanismo de reação da CT. Um mecanismo proposto é a libertação de CO₂ da biotina, que depois extrai um protão do grupo metilo da acetil-CoA carboxilase. O enolato resultante ataca o CO₂ para formar malonil-CoA. Num mecanismo competitivo, a extração de protões é coordenada com o ataque da acetil-CoA.
Função
A função da ACC é regular o metabolismo dos ácidos gordos. Quando a enzima está ativa, forma-se o produto malonil-CoA, que é um bloco de construção para a síntese de novos ácidos gordos e pode inibir a transferência do grupo acil gordo da acil-CoA para a carnitina pela carnitina aciltransferase, o que inibe a beta-oxidação dos ácidos gordos nas mitocôndrias.
Nos mamíferos, são expressas duas isoformas principais da ACC: ACC1 e ACC2, que diferem na distribuição tecidular e na função. A ACC1 encontra-se no citoplasma de todas as células, mas é mais abundante nos tecidos lipogénicos, como o tecido adiposo e a glândula mamária lactante, onde a síntese de ácidos gordos é importante.[10] Nos tecidos oxidativos, como o músculo esquelético e o coração, a proporção de ACC2 expressa é maior. Tanto a ACC1 como a ACC2 são altamente expressas no fígado, onde a oxidação e a síntese de ácidos gordos são importantes.[11] As diferenças na distribuição tecidular indicam que a ACC1 mantém a regulação da síntese de ácidos gordos, enquanto a ACC2 regula principalmente a oxidação dos ácidos gordos (beta-oxidação).
Uma isoforma mitocondrial da ACC1 (mtACC1) desempenha um papel parcialmente redundante na síntese de ácido lipoico e, portanto, na lipoilação de proteínas, fornecendo malonil-CoA para a síntese mitocondrial de ácidos gordos em conjunto com a ACSF3.[12][13]
Regulação

A regulação da ACC em mamíferos é complexa, controlando duas populações distintas de moléculas de malonil-CoA que direcionam a inibição da beta-oxidação ou a ativação da biossíntese lipídica.
A ACC1 e a ACC2 nos mamíferos são reguladas transcricionalmente por múltiplos promotores que determinam a abundância de ACC em resposta ao estado nutricional da célula. A ativação da expressão génica por diferentes promotores resulta no splicing alternativo do mRNA. No entanto, o significado fisiológico das isoenzimas ACC específicas não é claro.[11] A sensibilidade ao estado nutricional surge do controlo destes promotores por fatores de transcrição como a proteína 1 de ligação ao elemento regulador de esteróis, que é controlada transcricionalmente pela insulina, e a ChREBP, que é regulada positivamente por dietas ricas em carboidratos.[14][15]
Através de um circuito de feedback, o citrato ativa o ACC.[16] O citrato pode aumentar a polimerização da ACC, aumentando assim a atividade enzimática; contudo, não está claro se a polimerização é o principal mecanismo pelo qual o citrato aumenta a atividade da ACC ou se é um artefacto das experiências in vitro. Outros ativadores alostéricos são o glutamato e outros ácidos dicarboxílicos.[17] Os acil-CoA gordos de cadeia curta e longa são inibidores do ACC através de feedback negativo.[18] Um desses moduladores alostéricos negativos é o palmitoil-CoA.[19]
A fosforilação pode ocorrer quando as hormonas glucagon[20] ou epinefrina[21] A fosforilação ocorre principalmente devido ao aumento dos níveis de AMP quando o estado energético da célula é baixo, levando à ativação da proteína quinase ativada por AMP (AMPK). A AMPK é o principal regulador do tipo quinase da ACC, com a capacidade de fosforilar vários resíduos de serina em ambas as isoformas da ACC.[22] Na ACC1, a AMPK fosforila a Ser79, Ser1200 e Ser1215. A proteína quinase A tem também a capacidade de fosforilar a ACC, mas com uma capacidade muito maior de fosforilar a ACC2 do que a ACC1. Os resíduos Ser80 e Ser1263 da ACC1 podem também servir como locais de fosforilação como mecanismo regulador.[23] No entanto, a importância fisiológica da proteína quinase A (PKA) na regulação da ACC é atualmente desconhecida. Coloca-se a hipótese de existirem outras quinases da ACC importantes para esta regulação, dado que existem muitos outros possíveis locais de fosforilação na ACC.[24]
Quando a insulina se liga aos seus recetores na membrana plasmática, ativa uma enzima fosfatase chamada proteína fosfatase 2A (PP2A) para desfosforilar a enzima, eliminando assim o efeito inibitório. Além disso, a insulina induz uma fosfodiesterase que diminui o nível de AMP cíclico (AMPc) na célula, inibindo assim a PKA, e também inibe diretamente a AMPK.
Esta proteína pode utilizar o modelo de regulação alostérica da morfeína.[25]
Referências
- ↑ a b c Tong L (agosto de 2005). «Acetyl-coenzyme A carboxylase: crucial metabolic enzyme and attractive target for drug discovery». Cellular and Molecular Life Sciences. 62 (16): 1784–1803. PMC 11139103
 . PMID 15968460. doi:10.1007/s00018-005-5121-4
. PMID 15968460. doi:10.1007/s00018-005-5121-4
- ↑ Brownsey RW, Zhande R, Boone AN (novembro de 1997). «Isoforms of acetyl-CoA carboxylase: structures, regulatory properties and metabolic functions». Biochemical Society Transactions. 25 (4): 1232–1238. PMID 9449982. doi:10.1042/bst0251232
- ↑ Abu-Elheiga L, Jayakumar A, Baldini A, Chirala SS, Wakil SJ (abril de 1995). «Human acetyl-CoA carboxylase: characterization, molecular cloning, and evidence for two isoforms». Proceedings of the National Academy of Sciences of the United States of America. 92 (9): 4011–4015. Bibcode:1995PNAS...92.4011A. PMC 42092
 . PMID 7732023. doi:10.1073/pnas.92.9.4011
. PMID 7732023. doi:10.1073/pnas.92.9.4011
- ↑ Widmer J, Fassihi KS, Schlichter SC, Wheeler KS, Crute BE, King N, Nutile-McMenemy N, Noll WW, Daniel S, Ha J, Kim KH, Witters LA (junho de 1996). «Identification of a second human acetyl-CoA carboxylase gene». The Biochemical Journal. 316 (Pt 3): 915–922. PMC 1217437
 . PMID 8670171. doi:10.1042/bj3160915
. PMID 8670171. doi:10.1042/bj3160915
- ↑ Sasaki Y, Nagano Y (junho de 2004). «Plant acetyl-CoA carboxylase: structure, biosynthesis, regulation, and gene manipulation for plant breeding». Bioscience, Biotechnology, and Biochemistry. 68 (6): 1175–1184. PMID 15215578. doi:10.1271/bbb.68.1175
- ↑ «accA, acetyl-CoA carboxylase alpha subunit (Escherichia coli str. K-12 substr. MG1655)». NCBI gene. National Center for Biotechnology Information, U.S. National Library of Medicine
- ↑ «accD, acetyl-CoA carboxylase beta subunit (Escherichia coli str. K-12 substr. MG1655)». NCBI gene. National Center for Biotechnology Information, U.S. National Library of Medicine
- ↑ Lee CK, Cheong HK, Ryu KS, Lee JI, Lee W, Jeon YH, Cheong C (agosto de 2008). «Biotinoyl domain of human acetyl-CoA carboxylase: Structural insights into the carboxyl transfer mechanism». Proteins. 72 (2): 613–624. PMID 18247344. doi:10.1002/prot.21952
- ↑ Chou CY, Yu LP, Tong L (abril de 2009). «Crystal structure of biotin carboxylase in complex with substrates and implications for its catalytic mechanism». The Journal of Biological Chemistry. 284 (17): 11690–11697. PMC 2670172
 . PMID 19213731. doi:10.1074/jbc.M805783200
. PMID 19213731. doi:10.1074/jbc.M805783200
- ↑ Kim TS, Leahy P, Freake HC (agosto de 1996). «Promoter usage determines tissue specific responsiveness of the rat acetyl-CoA carboxylase gene». Biochemical and Biophysical Research Communications. 225 (2): 647–653. PMID 8753813. doi:10.1006/bbrc.1996.1224
- ↑ a b Barber MC, Price NT, Travers MT (março de 2005). «Structure and regulation of acetyl-CoA carboxylase genes of metazoa». Biochimica et Biophysica Acta (BBA) - Molecular and Cell Biology of Lipids. 1733 (1): 1–28. PMID 15749055. doi:10.1016/j.bbalip.2004.12.001
- ↑ Monteuuis G, Suomi F, Kerätär JM, Masud AJ, Kastaniotis AJ (novembro de 2017). «A conserved mammalian mitochondrial isoform of acetyl-CoA carboxylase ACC1 provides the malonyl-CoA essential for mitochondrial biogenesis in tandem with ACSF3». The Biochemical Journal. 474 (22): 3783–3797. PMID 28986507. doi:10.1042/BCJ20170416
- ↑ Kastaniotis, Alexander J.; Autio, Kaija J.; R. Nair, Remya (abril de 2021). «Mitochondrial Fatty Acids and Neurodegenerative Disorders». The Neuroscientist (em inglês). 27 (2): 143–158. ISSN 1073-8584. PMID 32644907. doi:10.1177/1073858420936162
- ↑ Field FJ, Born E, Murthy S, Mathur SN (dezembro de 2002). «Polyunsaturated fatty acids decrease the expression of sterol regulatory element-binding protein-1 in CaCo-2 cells: effect on fatty acid synthesis and triacylglycerol transport». The Biochemical Journal. 368 (Pt 3): 855–864. PMC 1223029
 . PMID 12213084. doi:10.1042/BJ20020731
. PMID 12213084. doi:10.1042/BJ20020731
- ↑ Ishii S, Iizuka K, Miller BC, Uyeda K (novembro de 2004). «Carbohydrate response element binding protein directly promotes lipogenic enzyme gene transcription». Proceedings of the National Academy of Sciences of the United States of America. 101 (44): 15597–15602. Bibcode:2004PNAS..10115597I. PMC 524841
 . PMID 15496471. doi:10.1073/pnas.0405238101
. PMID 15496471. doi:10.1073/pnas.0405238101
- ↑ Martin DB, Vagelos PR (junho de 1962). «The mechanism of tricarboxylic acid cycle regulation of fatty acid synthesis». The Journal of Biological Chemistry. 237 (6): 1787–1792. PMID 14470343. doi:10.1016/S0021-9258(19)73938-6
- ↑ Boone AN, Chan A, Kulpa JE, Brownsey RW (abril de 2000). «Bimodal activation of acetyl-CoA carboxylase by glutamate». The Journal of Biological Chemistry. 275 (15): 10819–10825. PMID 10753875. doi:10.1074/jbc.275.15.10819
- ↑ Faergeman NJ, Knudsen J (abril de 1997). «Role of long-chain fatty acyl-CoA esters in the regulation of metabolism and in cell signalling». The Biochemical Journal. 323 (Pt 1): 1–12. PMC 1218279
 . PMID 9173866. doi:10.1042/bj3230001
. PMID 9173866. doi:10.1042/bj3230001
- ↑ Pham T, Walden E, Huard S, Pezacki J, Fullerton MD, Baetz K (julho de 2022). «Fine-tuning acetyl-CoA carboxylase 1 activity through localization: functional genomics reveals a role for the lysine acetyltransferase NuA4 and sphingolipid metabolism in regulating Acc1 activity and localization». Genetics. 221 (4). PMC 9339284
 . PMID 35608294. doi:10.1093/genetics/iyac086
. PMID 35608294. doi:10.1093/genetics/iyac086
- ↑ Peng IC, Chen Z, Hsu PH, Su MI, Tsai MD, Shyy JY (abril de 2010). «Glucagon Activates the AMP-Activated Protein Kinase/Acetyl-CoA Carboxylase Pathway in Adipocytes». The FASEB Journal. 24 (S1). ISSN 0892-6638. doi:10.1096/fasebj.24.1_supplement.995.4
- ↑ Koh HJ, Hirshman MF, He H, Li Y, Manabe Y, Balschi JA, Goodyear LJ (maio de 2007). «Adrenaline is a critical mediator of acute exercise-induced AMP-activated protein kinase activation in adipocytes». The Biochemical Journal. 403 (3): 473–481. PMC 1876380
 . PMID 17253964. doi:10.1042/BJ20061479
. PMID 17253964. doi:10.1042/BJ20061479
- ↑ Park SH, Gammon SR, Knippers JD, Paulsen SR, Rubink DS, Winder WW (junho de 2002). «Phosphorylation-activity relationships of AMPK and acetyl-CoA carboxylase in muscle». Journal of Applied Physiology. 92 (6): 2475–2482. PMID 12015362. doi:10.1152/japplphysiol.00071.2002
- ↑ Wei J, Tong L (setembro de 2018). «How Does Polymerization Regulate Human Acetyl-CoA Carboxylase 1?». Biochemistry. 57 (38): 5495–5496. PMID 30211541. doi:10.1021/acs.biochem.8b00881
- ↑ Brownsey RW, Boone AN, Elliott JE, Kulpa JE, Lee WM (abril de 2006). «Regulation of acetyl-CoA carboxylase». Biochemical Society Transactions. 34 (Pt 2): 223–227. PMID 16545081. doi:10.1042/BST20060223
- ↑ Selwood T, Jaffe EK (março de 2012). «Dynamic dissociating homo-oligomers and the control of protein function». Archives of Biochemistry and Biophysics. 519 (2): 131–143. PMC 3298769
 . PMID 22182754. doi:10.1016/j.abb.2011.11.020
. PMID 22182754. doi:10.1016/j.abb.2011.11.020