Água-viva (animal)
Água-viva
| |||||||
|---|---|---|---|---|---|---|---|
 Água-viva do Pacífico (Chrysaora fuscescens) | |||||||
| Classificação científica | |||||||
| |||||||
| Grupos incluídos | |||||||
| Grupos excluídos | |||||||
As águas-vivas, também conhecidas como medusas ou mães d'água, são a fase de medusa de certos membros gelatinosos do subfilo Medusozoa, que é uma parte importante do filo Cnidaria. As águas-vivas são principalmente animais marinhos de natação livre, embora algumas sejam ancoradas ao fundo do mar por pedúnculos, em vez de serem móveis. Elas são compostas por um corpo principal em forma de guarda-chuva, feito de mesogleia, conhecido como sino, e uma coleção de tentáculos pendentes na parte inferior.
Por meio de contrações pulsantes, o sino pode fornecer propulsão para locomoção em águas abertas. Os tentáculos são armados com células urticantes (os cnidócitos) e podem ser usados para capturar presas ou se defender contra predadores. As águas-vivas possuem um ciclo de vida complexo, e a fase medusa é normalmente a fase sexual, que produz larvas plânulas. Estas se dispersam amplamente e entram em uma fase de polipo sedentária, que pode incluir brotamento assexual antes de atingir a maturidade sexual.
As águas-vivas são encontradas em todo o mundo, desde águas superficiais até o fundo do mar. As Scyphozoas (as "águas-vivas verdadeiras") são exclusivamente marinhas, mas algumas Hydrozoas com aparência semelhante vivem em água doce. Águas-vivas grandes e muitas vezes coloridas são comuns em zonas costeiras em todo o mundo. As medusas da maioria das espécies crescem rapidamente, amadurecem em poucos meses e morrem logo após a reprodução, mas a fase de pólipo, fixada ao fundo do mar, pode ser muito mais longeva. As águas-vivas existem há pelo menos 500 milhões de anos,[1] e possivelmente 700 milhões de anos ou mais, tornando-as o grupo animal multiorgânico mais antigo.[2]
As águas-vivas são consumidas por humanos em certas culturas. Elas são consideradas uma iguaria em alguns países asiáticos, onde espécies da ordem Rhizostomeae são prensadas e salgadas para remover o excesso de água. Pesquisadores australianos as descreveram como um "alimento perfeito": sustentável e rico em proteínas, mas relativamente baixo em energia alimentar.[3]
Elas também são usadas em pesquisas de células e moléculas, especialmente da proteína verde fluorescente usada por algumas espécies para bioluminescência. Essa proteína foi adaptada como um repórter fluorescente para genes inseridos e teve um grande impacto na microscopia de fluorescência.
As células urticantes usadas pelas águas-vivas para subjugar suas presas podem ferir humanos. Milhares de nadadores em todo o mundo são ferroados todos os anos, com efeitos que variam de leve desconforto a lesões graves ou até a morte. Quando as condições são favoráveis, as águas-vivas podem formar grandes enxames, que podem danificar equipamentos de pesca ao encher redes de pesca e, às vezes, entupir os sistemas de refrigeração de usinas de energia e usinas de dessalinização que retiram água do mar.
Nomenclatura
O nome água-viva, que no inglês é "jellyfish", em uso desde 1796,[4] tem sido tradicionalmente aplicado a medusas e todos os animais semelhantes, incluindo os ctenóforos (outro filo).[5][6] Entretanto, o nome popular no inglês têm sido substituído por outros termos (como apenas "jellies" ou "sea jellies") em aquários públicos em um esforço para evitar o uso da palavra "peixe" ("fish") com sua conotação moderna de um animal com espinha dorsal, embora mariscos ("shellfish"), lulas ("cuttlefish") e estrelas-do-mar ("starfish") também não sejam vertebrados.[7][8] Na literatura científica em inglês, "jelly" e "jellyfish" têm sido usados indistintamente.[9][10] Muitas fontes referem-se apenas às Scyphozoas como "águas-vivas verdadeiras".[11]
Um grupo de águas-vivas é chamado de "bando"[12] ou "agregado".[13]
Mapeamento para grupos taxonômicos

Filogenia
Definição
O termo água-viva corresponde amplamente às medusas,[4] ou seja, uma fase do ciclo de vida do grupo Medusozoa. A bióloga evolucionista americana Paulyn Cartwright oferece a seguinte definição geral:
| “ | Tipicamente, os cnidários medusozoários têm uma fase de água-viva pelágica e predatória em seu ciclo de vida; as estauromedusas são as exceções [pois são pedunculadas].[14] | ” |
O dicionário Merriam-Webster define água-viva da seguinte forma:
| “ | Um celenterado marinho de natação livre que é a forma reprodutiva sexual de um hidrozoário ou esifozoário e tem um corpo em forma de disco quase transparente e tentáculos marginais extensíveis repletos de células urticantes.[15] | ” |
Dado que água-viva é um nome comum, seu mapeamento para grupos biológicos é inexato. Algumas autoridades chamaram os ctenóforos[16] e certas salpas[16] de águas-vivas, embora outras autoridades afirmem que nenhuma dessas são águas-vivas, que deveriam ser limitadas a certos grupos dentro dos medusozoários.[17][18]
Os clados não-medusozoários chamados de águas-vivas por algumas autoridades, mas não por todas (tanto as citações que concordam quanto as que discordam são fornecidas em cada caso), são indicados com "???" no seguinte cladograma do reino animal:
| Animalia |
| ||||||||||||||||||||||||||||||||||||
Águas-vivas medusozoárias
As águas-vivas não são um clado, pois incluem a maioria dos Medusozoa, exceto alguns dos Hydrozoa.[19][20] Os grupos de medusozoários incluídos pelas autoridades são indicados na árvore filogenética a seguir pela presença de citações. Os nomes das águas-vivas incluídas, em inglês quando possível, são mostrados em negrito; a presença de um exemplo nomeado e citado indica que pelo menos aquela espécie dentro de seu grupo foi chamada de água-viva.
As águas-vivas não formam um único clado, pois incluem a maioria dos Medusozoa, exceto algumas Hydrozoa.[19][20] Os grupos medusozoários incluídos pelas autoridades são indicados na seguinte árvore filogenética pela presença de citações. Os nomes das águas-vivas incluídas, em português quando possível, são apresentados em negrito; a presença de um exemplo nomeado e citado indica que pelo menos essa espécie dentro de seu grupo foi chamada de água-viva.
| Cnidaria |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Taxonomia
O subfilo Medusozoa inclui todos os cnidários com uma fase de medusa em seu ciclo de vida. O ciclo básico é ovo, larva plânula, pólipo e medusa, sendo a medusa a fase sexual. A fase de pólipo é, por vezes, secundariamente perdida. O subfilo inclui os principais táxons: Scyphozoa (águas-vivas grandes), Cubozoa (cubomedusas) e Hydrozoa (águas-vivas pequenas), e exclui Anthozoa (corais e anêmonas marinhas).[25] Isso sugere que a forma de medusa evoluiu após os pólipos.[26] Os medusozoários têm simetria tetramérica, com partes em quatro ou múltiplos de quatro.[25]
As quatro principais classes de Cnidaria medusozoários são:
- Scyphozoa são por vezes chamadas de águas-vivas verdadeiras, embora não sejam mais verdadeiramente águas-vivas do que as outras listadas aqui. Elas têm simetria tetra-radial. A maioria possui tentáculos ao redor da margem externa do sino em forma de tigela e braços orais longos ao redor da boca no centro da subumbrela.[25]
- Cubozoa (cubomedusas) têm um sino em forma de caixa (arredondado), e seu velário as auxilia a nadar mais rapidamente. As cubomedusas podem ser mais próximas das águas-vivas Scyphozoa do que qualquer uma delas dos Hydrozoa.[26]
- As medusas Hydrozoa também têm simetria tetra-radial, quase sempre possuem um véu (diafragma usado na natação) fixado logo dentro da margem do sino, não têm braços orais, mas uma estrutura central em forma de haste muito menor, o manúbrio, com uma abertura bucal terminal, e são distinguidas pela ausência de células na mesogleia. Os Hydrozoa mostram grande diversidade de estilo de vida; algumas espécies mantêm a forma de pólipo por toda a sua vida e não formam medusas (como as Hydras, que, portanto, não são consideradas como água-viva), e algumas são inteiramente medusais e não possuem forma de pólipo.[25]
- Staurozoa (águas-vivas pedunculadas) são caracterizadas por uma forma de medusa que é geralmente séssil, orientada de cabeça para baixo e com um pedúnculo emergindo do ápice do "cálice" (sino), que se fixa ao substrato. Pelo menos algumas Staurozoa também têm uma forma de pólipo que alterna com a porção medusoide do ciclo de vida. Até recentemente, as Staurozoa eram classificadas dentro de Scyphozoa.[25]
Existem mais de 200 espécies de Scyphozoa, cerca de 50 espécies de Staurozoa, cerca de 50 espécies de Cubozoa, e os Hydrozoa incluem cerca de 1000–1500 espécies que produzem medusas, mas muitas outras espécies que não o fazem.[27][28]
História fóssil
_(1907)_(14799088733).jpg)


Como as águas-vivas não possuem partes duras, fósseis são raros. O fóssil mais antigo e inequívoco de uma medusa de natação livre é Burgessomedusa [en] do folhelho Burgess do Canadá, do Cambriano Médio, que provavelmente é um grupo-tronco de cubomedusas (Cubozoa) ou Acraspeda (o clado que inclui Staurozoa, Cubozoa e Scyphozoa). Outros registros alegados do Cambriano da China e de Utah, nos Estados Unidos, são incertos e possivelmente representam ctenóforos em vez disso.[29]
Anatomia
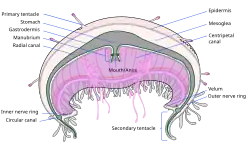
A principal característica de uma água-viva verdadeira é o sino em forma de guarda-chuva. Esta é uma estrutura oca composta por uma massa de material gelatinoso transparente conhecido como mesogleia, que forma o esqueleto hidrostático [en] do animal.[25] A mesogleia é composta por 95% ou mais de água,[30] e também contém colágeno e outras proteínas fibrosas, além de amebócitos errantes que podem englobar detritos e bactérias. A mesogleia é delimitada pela epiderme na parte externa e pela gastroderme na parte interna. A borda do sino é frequentemente dividida em lobos arredondados conhecidos como "lappets", que permitem que o sino se flexione. Nos espaços ou nichos entre os lappets, encontram-se órgãos sensoriais rudimentares pendentes conhecidos como ropálios, e a margem do sino frequentemente apresenta tentáculos.[25]
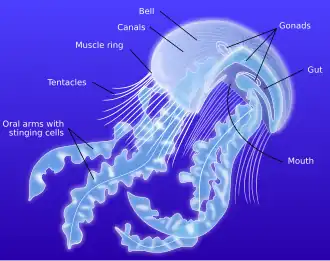
Na parte inferior do sino encontra-se o manúbrio, uma estrutura em forma de haste que pende do centro, com a boca, que também funciona como ânus, na sua extremidade. Frequentemente, há quatro braços orais conectados ao manúbrio, que se estendem para a água abaixo.[31] A boca se abre para a cavidade gastrovascular, onde ocorre a digestão e os nutrientes são absorvidos. Esta é subdividida por quatro septos espessos em um estômago central e quatro bolsas gástricas. Os quatro pares de gônadas estão presos aos septos, e próximos a eles, quatro funis septais se abrem para o exterior, talvez fornecendo boa oxigenação às gônadas. Perto das bordas livres dos septos, filamentos gástricos se estendem para a cavidade gástrica; estes são armados com nematocistos e células produtoras de enzimas e desempenham um papel na subjugação e digestão da presa. Em algumas esifozoárias, a cavidade gástrica é conectada a canais radiais que se ramificam extensivamente e podem se unir a um canal de anel marginal. Cílios nesses canais fazem o fluido circular em uma direção regular.[25]
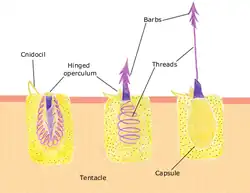
As cubomedusas são em grande parte semelhantes em estrutura. Elas têm um sino de formato quadrado, em forma de caixa. Um pedalium curto ou haste pende de cada um dos quatro cantos inferiores. Um ou mais tentáculos longos e esguios estão presos a cada pedalium.[32] A borda do sino é dobrada para dentro, formando uma prateleira conhecida como velário, que restringe a abertura do sino e cria um jato poderoso quando o sino pulsa, permitindo que as cubomedusas nadem mais rápido que as águas-vivas verdadeiras. Os hidrozoários são também semelhantes, geralmente com apenas quatro tentáculos na borda do sino, embora muitos hidrozoários sejam coloniais e possam não ter uma fase de medusa de vida livre. Em algumas espécies, forma-se um broto não destacável conhecido como gonóforo, que contém uma gônada, mas carece de muitas outras características de medusa, como tentáculos e ropálios. As águas-vivas pedunculadas são fixadas a uma superfície sólida por um disco basal e se assemelham a um pólipo, cuja extremidade oral se desenvolveu parcialmente em uma medusa com lobos portadores de tentáculos e um manúbrio central com boca de quatro lados.[25]
A maioria das águas-vivas não possui sistemas especializados para osmorregulação, respiração e circulação, e não possui um sistema nervoso central. Os nematocistos, que liberam a ferroada, estão localizados principalmente nos tentáculos; as águas-vivas verdadeiras também os possuem ao redor da boca e do estômago.[33] As águas-vivas não precisam de um sistema respiratório, pois o oxigênio suficiente difunde através da epiderme. Elas têm controle limitado sobre seu movimento, mas podem navegar com as pulsações do corpo em forma de sino; algumas espécies são nadadoras ativas na maior parte do tempo, enquanto outras derivam amplamente.[34] Os ropálios contêm órgãos sensoriais rudimentares capazes de detectar luz, vibrações transmitidas pela água, odores e orientação.[25] Uma rede frouxa de nervos chamada "rede nervosa" está localizada na epiderme.[35][36] Embora tradicionalmente se pense que as águas-vivas não possuem um sistema nervoso central, a concentração de redes nervosas e estruturas semelhantes a gânglios poderia ser considerada como tal em muitas espécies.[37] Uma água-viva detecta estímulos e transmite impulsos tanto através da rede nervosa quanto ao redor de um anel nervoso circular, para outras células nervosas. Os gânglios ropaliais contêm neurônios marca-passos que controlam a taxa e a direção da natação.[25]
Em muitas espécies de águas-vivas, os ropálios incluem ocelos, órgãos sensíveis à luz capazes de distinguir luz de escuridão. Estes são geralmente ocelos de mancha pigmentada, que possuem algumas de suas células pigmentadas. Os ropálios são suspensos em hastes com cristais pesados de carbonato de cálcio em uma extremidade, funcionando como giroscópios para orientar os olhos para o céu. Certas águas-vivas olham para cima, para o dossel do mangue, enquanto fazem uma migração diária dos pântanos de mangue para a lagoa aberta, onde se alimentam, e de volta.[2]
As cubomedusas têm uma visão mais avançada que os outros grupos. Cada indivíduo possui 24 olhos, dois dos quais são capazes de ver cores, e quatro áreas paralelas de processamento de informações que atuam em competição,[38] supostamente tornando-as um dos poucos tipos de animais a ter uma visão de 360 graus de seu ambiente.[39]
Olho das cubomedusas
O estudo da evolução dos olhos das águas-vivas é um intermediário para uma melhor compreensão de como os sistemas visuais evoluíram na Terra. As águas-vivas exibem uma imensa variação nos sistemas visuais, que vão desde manchas de células fotorreceptoras vistas em sistemas fotorreceptivos simples até olhos complexos observados em cubomedusas.[40] Tópicos principais da pesquisa sobre sistemas visuais de águas-vivas (com ênfase nas cubomedusas) incluem: a evolução da visão de águas-vivas de sistemas visuais simples para complexos, a morfologia e estruturas moleculares dos olhos das cubomedusas (incluindo comparações com olhos de vertebrados) e diversos usos da visão, incluindo comportamentos guiados por tarefas e especialização de nicho.
Evolução
Evidências experimentais de fotossensibilidade e fotorrecepção em cnidários precedem meados do século XX, e um rico corpo de pesquisa desde então abordou a evolução dos sistemas visuais em águas-vivas.[41] Os sistemas visuais de águas-vivas variam de células fotorreceptoras simples a olhos formadores de imagens complexos. Sistemas visuais mais ancestrais incorporam visão extraocular (visão sem olhos) que abrange inúmeros receptores dedicados a comportamentos de função única. Sistemas visuais mais derivados compreendem percepção capaz de comportamentos guiados por múltiplas tarefas.
Embora não possuam um cérebro verdadeiro, as águas-vivas cnidárias têm um sistema nervoso em "anel" que desempenha um papel significativo na atividade motora e sensorial. Essa rede de nervos é responsável pela contração muscular e movimento, culminando no surgimento de estruturas fotossensíveis.[40] Em Cnidaria, há grande variação nos sistemas que sustentam a fotossensibilidade. As estruturas fotossensíveis variam de grupos de células não especializadas a olhos mais "convencionais" semelhantes aos de vertebrados.[41] As etapas evolutivas gerais para desenvolver uma visão complexa incluem (de estados mais ancestrais a mais derivados): fotorrecepção não direcional, fotorrecepção direcional, visão de baixa resolução e visão de alta resolução. A complexidade de habitat e tarefas aumentada favoreceu os sistemas visuais de alta resolução comuns em cnidários derivados, como as cubomedusas.[40]
Sistemas visuais basais observados em vários cnidários exibem fotossensibilidade representativa de uma única tarefa ou comportamento. A fotorrecepção extraocular (uma forma de fotorrecepção não direcional) é a forma mais básica de sensibilidade à luz e orienta uma variedade de comportamentos entre os cnidários. Ela pode funcionar para regular o ritmo circadiano (como visto em hidrozoários sem olhos) e outros comportamentos guiados pela luz responsivos à intensidade e espectro da luz. A fotorrecepção extraocular pode funcionar adicionalmente em fototaxia positiva (em larvas plânulas de hidrozoários),[41] bem como na evitação de quantidades prejudiciais de radiação UV por meio de fototaxia negativa. A fotorrecepção direcional (a capacidade de perceber a direção da luz incidente) permite respostas fototáxicas mais complexas à luz e provavelmente evoluiu por meio do empilhamento de membranas.[40] As respostas comportamentais resultantes podem variar desde eventos de desova guiados pela luz lunar até respostas a sombras para evitar potenciais predadores.[41][42] Comportamentos guiados pela luz são observados em numerosos esifozoários, incluindo a comum medusa-da-lua, Aurelia aurita, que migra em resposta a mudanças na luz ambiente e na posição solar, mesmo sem possuir olhos propriamente ditos.[41]
O sistema visual de baixa resolução das cubomedusas é mais derivado que a fotorrecepção direcional, e, portanto, a visão das cubomedusas representa a forma mais básica de visão verdadeira, na qual múltiplos fotorreceptores direcionais se combinam para criar a primeira formação de imagem e resolução espacial. Isso é diferente da visão de alta resolução observada em olhos do tipo câmera ou compostos de vertebrados e cefalópodes, que dependem de ótica de foco.[41] Criticamente, os sistemas visuais das cubomedusas são responsáveis por guiar múltiplas tarefas ou comportamentos, em contraste com sistemas visuais menos derivados em outras águas-vivas que guiam funções comportamentais únicas. Esses comportamentos incluem fototaxia baseada na luz solar (positiva) ou sombras (negativa), evitação de obstáculos e controle da taxa de pulsação de nado.[43]
As cubomedusas possuem "olhos verdadeiros" (semelhantes aos de vertebrados) que lhes permitem habitar ambientes que medusas menos derivadas não conseguem. De fato, elas são consideradas a única classe no clado Medusozoa que possui comportamentos que necessitam de resolução espacial e visão genuína.[41] No entanto, as lentes em seus olhos são mais funcionalmente semelhantes a olhos em forma de taça exibidos em organismos de baixa resolução e têm pouca ou nenhuma capacidade de foco.[44][43] A falta de capacidade de foco é devido ao comprimento focal exceder a distância até a retina, gerando imagens desfocadas e limitando a resolução espacial.[41] O sistema visual ainda é suficiente para as cubomedusas produzirem uma imagem que auxilia em tarefas como a evitação de objetos.
Utilidade como organismo modelo
Os olhos das cubomedusas são um sistema visual sofisticado em vários aspectos. Essas complexidades incluem a considerável variação na morfologia dos olhos das cubomedusas (incluindo sua especificação para tarefas/comportamentos) e a composição molecular de seus olhos, incluindo: fotorreceptores, opsinas, lentes e sinapses.[41] A comparação desses atributos com sistemas visuais mais derivados pode permitir uma compreensão mais aprofundada de como a evolução de sistemas visuais mais derivados pode ter ocorrido, e coloca em perspectiva como as cubomedusas podem desempenhar o papel de modelo evolutivo/desenvolvimental para todos os sistemas visuais.[45]
Características
Os sistemas visuais das cubomedusas são diversos e complexos, compreendendo múltiplos fotossistemas. É provável que haja uma variação considerável nas propriedades visuais entre as espécies de cubomedusas, dado a significativa variação morfológica e fisiológica entre as espécies. Os olhos tendem a diferir em tamanho e forma, assim como no número de receptores (incluindo opsinas) e na fisiologia entre as espécies de cubomedusas.[41]
As cubomedusas possuem uma série de olhos com lentes intricadas que são semelhantes aos de organismos multicelulares mais derivados, como os vertebrados. Seus 24 olhos se encaixam em quatro categorias morfológicas diferentes.[46] Essas categorias consistem em dois olhos mediais grandes, morfologicamente diferentes (um olho com lente inferior e um superior), contendo lentes esféricas, um par lateral de olhos de fenda pigmentada e um par lateral de olhos de fosseta pigmentada.[43] Os olhos estão situados em ropálios (pequenas estruturas sensoriais) que desempenham funções sensoriais das cubomedusas e emergem das cavidades da exumbrela (a superfície do corpo) na lateral dos sinos das águas-vivas.[41] Os dois olhos grandes estão localizados na linha média do clube e são considerados complexos porque contêm lentes. Os quatro olhos restantes estão lateralmente em cada lado de cada ropálio e são considerados simples. Os olhos simples são observados como pequenas taças invaginadas de epitélio que desenvolveram pigmentação. O maior dos olhos complexos contém uma córnea celular criada por um epitélio monociliado, uma lente celular, uma cápsula homogênea para a lente, corpo vítreo com elementos prismáticos e uma retina de células pigmentadas. O menor dos olhos complexos é considerado ligeiramente menos complexo, pois não possui uma cápsula, mas contém, por outro lado, a mesma estrutura do olho maior.[47]
As cubomedusas possuem múltiplos fotossistemas que compreendem diferentes conjuntos de olhos. Evidências incluem dados imunocitoquímicos [en] e moleculares que mostram diferenças de fotopigmento entre os diferentes tipos de olhos morfológicos, e experimentos fisiológicos realizados em cubomedusas sugerem diferenças comportamentais entre os fotossistemas. Cada tipo de olho individual constitui fotossistemas que trabalham coletivamente para controlar comportamentos guiados visualmente.[41] Os olhos das cubomedusas utilizam principalmente c-PRCs (células fotorreceptoras ciliares) semelhantes às dos olhos de vertebrados. Essas células passam por cascatas de fototransdução [en] (processo de absorção de luz pelos fotorreceptores) desencadeadas por c-opsinas.[48] Sequências de opsinas disponíveis sugerem que há dois tipos de opsinas possuídos por todos os cnidários, incluindo uma opsina filogenética antiga e uma opsina ciliar irmã do grupo de c-opsinas. As cubomedusas poderiam ter tanto opsinas ciliares quanto cnidops (opsinas cnidárias), algo que anteriormente não se acreditava ocorrer na mesma retina. No entanto, não é totalmente evidente se os cnidários possuem múltiplas opsinas capazes de ter sensibilidades espectrais distintas.[41]
Comparação com outros organismos
Pesquisas comparativas sobre a composição genética e molecular dos olhos das cubomedusas versus olhos mais derivados vistos em vertebrados e cefalópodes focam em: lentes e composição de cristalino, sinapses e genes Pax e suas evidências implícitas para genes primordiais (ancestrais) compartilhados na evolução dos olhos.[49]
Os olhos das cubomedusas são considerados um modelo evolutivo/desenvolvimental de todos os olhos com base em seu recrutamento evolutivo de cristalinos e genes Pax. Pesquisas realizadas em cubomedusas, incluindo Tripedalia cystophora, sugeriram que elas possuem um único gene Pax, PaxB. O PaxB funciona ligando-se a promotores de cristalino e ativando-os. A hibridização in situ de PaxB resultou em expressão de PaxB na lente, retina e estatocistos. Esses resultados e a rejeição da hipótese anterior de que o Pax6 era um gene Pax ancestral nos olhos levaram à conclusão de que o PaxB era um gene primordial na evolução dos olhos, e que os olhos de todos os organismos provavelmente compartilham um ancestral comum.[45]
Todos os quatro sistemas visuais das espécies de cubomedusas investigadas em detalhes (Carybdea marsupialis, Chiropsalmus quadrumanus, Tamoya haplonema e Tripedalia cystophora) possuem sinapses invaginadas, mas apenas nos olhos com lente superior e inferior. Diferentes densidades foram encontradas entre as lentes superior e inferior, e entre as espécies. Quatro tipos de sinapses químicas foram descobertos nos ropálios, o que poderia ajudar a entender a organização neural, incluindo: unidirecional clara, unidirecional de núcleo denso, bidirecional clara e bidirecional clara e de núcleo denso. As sinapses dos olhos com lente poderiam ser úteis como marcadores para aprender mais sobre o circuito neural nas áreas retinianas das cubomedusas.[46]
Evolução como resposta a estímulos naturais
As principais respostas adaptativas à variação ambiental observadas nos olhos das cubomedusas incluem velocidades de constrição pupilar em resposta a ambientes luminosos, bem como ajustes de fotorreceptores e adaptação de lentes para melhor responder às mudanças entre ambientes luminosos e escuridão. Os olhos de algumas espécies de cubomedusas parecem ter evoluído uma visão mais focada em resposta ao seu habitat.[50]
A constrição pupilar parece ter evoluído em resposta à variação no ambiente luminoso em nicho ecológicos entre três espécies de cubomedusas (Chironex fleckeri, Chiropsella bronzie e Carukia barnesi). Estudos comportamentais sugerem que taxas de constrição pupilar mais rápidas permitem maior evitação de objetos, e, de fato, espécies em habitats mais complexos exibem taxas mais rápidas. C. bronzie habita praias rasas com baixa visibilidade e poucos obstáculos, portanto, a constrição pupilar rápida em resposta a objetos em seu ambiente não é importante. C. barnesi e C. fleckeri são encontradas em ambientes tridimensionalmente mais complexos, como mangues com abundância de obstáculos naturais, onde a constrição pupilar mais rápida é mais adaptativa.[50] Estudos comportamentais apoiam a ideia de que taxas de constrição pupilar mais rápidas auxiliam na evitação de obstáculos, bem como em ajustes de profundidade em resposta a diferentes intensidades de luz.
A adaptação claro/escuro por meio de reflexos pupilares à luz é uma forma adicional de resposta evolutiva ao ambiente luminoso. Isso está relacionado à resposta da pupila às mudanças entre intensidades de luz (geralmente da luz solar para a escuridão). No processo de adaptação claro/escuro, os olhos com lente superior e inferior de diferentes espécies de cubomedusas variam em função específica. A lente superior de C. bronzie não exibe poder óptico considerável, enquanto a de T. cystophora (uma espécie de cubomedusa que tende a viver em manguezais) sim. A capacidade de usar a luz para guiar o comportamento visualmente não é tão importante para C. bronzie quanto para espécies em ambientes cheios de obstáculos.[43] Diferenças no comportamento guiado visualmente servem como evidência de que espécies que compartilham o mesmo número e estrutura de olhos podem exibir diferenças em como controlam o comportamento.
Maiores e menores
As águas-vivas variam de cerca de um milímetro em altura e diâmetro do sino,[51] a quase 2 m em altura e diâmetro do sino; os tentáculos e partes bucais geralmente se estendem além dessa dimensão do sino.[25]
As menores águas-vivas são as peculiares águas-vivas rastejantes dos gêneros Staurocladia e Eleutheria, que têm discos de sino de 0.5 mm a alguns mm de diâmetro, com tentáculos curtos que se estendem além disso, os quais essas águas-vivas usam para se mover pela superfície de algas ou fundos de piscinas rochosas;[51] muitas dessas pequenas águas-vivas rastejantes não podem ser vistas a olho nu sem uma lente de mão ou microscópio. Elas podem se reproduzir assexuadamente por fissão (divisão ao meio). Outras águas-vivas muito pequenas, com sinos de cerca de um milímetro, são as hidromedusas de muitas espécies que acabaram de ser liberadas de seus pólipos parentais;[52] algumas dessas vivem apenas alguns minutos antes de liberarem seus gametas no plâncton e depois morrerem, enquanto outras crescerão no plâncton por semanas ou meses. As hidromedusas Cladonema radiatum e C. californicum também são muito pequenas, vivendo por meses, mas nunca crescendo além de alguns milímetros em altura e diâmetro do sino.[53]

A água-viva-juba-de-leão, Cyanea capillata, foi por muito tempo citada como a maior água-viva, e possivelmente o animal mais longo do mundo, com tentáculos finos, semelhantes a fios, que podem se estender em até 36.5 m de comprimento (embora a maioria não seja nem de longe tão grande).[54][55] Elas têm uma ferroada moderadamente dolorosa, mas raramente fatal.[56] A cada vez mais comum água-viva de Nomura, Nemopilema nomurai [en], encontrada em alguns, mas não todos os anos, nas águas do Japão, Coreia e China no verão e outono, é outra candidata a "maior água-viva", em termos de diâmetro e peso, já que as maiores águas-vivas de Nomura no final do outono podem atingir 2 m no diâmetro do sino (corpo) e cerca de 200 kg de peso, com espécimes médios frequentemente alcançando 0.9 m no diâmetro do sino e cerca de 150 kg de peso.[57][58] A grande massa do sino da água-viva de Nomura gigante[59] pode superar um mergulhador e é quase sempre muito maior que a juba-de-leão, cujo diâmetro do sino pode alcançar 1 m.[60]
A raramente encontrada água-viva fantasma gigante Stygiomedusa gigantea é outra candidata a "maior água-viva", com seu sino espesso e maciço de até 100 cm de largura, e quatro braços orais grossos, em forma de "tira", que se estendem até 6 m de comprimento, muito diferentes dos tentáculos finos e filiformes típicos que margeiam o guarda-chuva de águas-vivas de aparência mais típica, incluindo a juba-de-leão.[61]
Desmonema glaciale, que vive na região antártica, pode atingir um tamanho muito grande (vários metros).[62][63] A medusa-de-riscas-púrpuras (C. colorata) também pode ser extremamente longa (até 4,5 metros).[64]
História de vida e comportamento
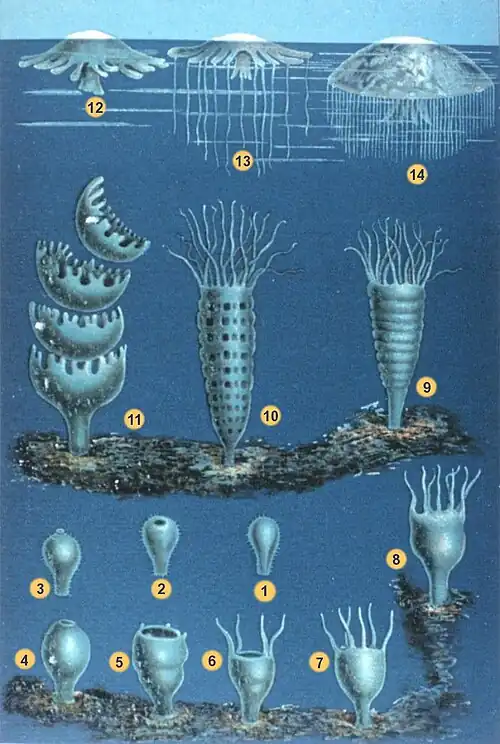
1–3 Larva procura um local
4–8 Pólipo cresce
9–11 Pólipo estrobila.
12–14 Medusa cresce.
Ciclo de vida
As águas-vivas possuem um ciclo de vida complexo que inclui fases sexuadas e assexuadas, sendo a medusa a fase sexual na maioria dos casos. Os espermatozoides fertilizam os ovos, que se desenvolvem em larvas plânulares, tornam-se pólipos, brotam em efiras e, em seguida, transformam-se em medusas adultas. Em algumas espécies, certos estágios podem ser pulados.[65]
Ao atingir o tamanho adulto, as águas-vivas desovam regularmente se houver suprimento suficiente de alimento. Na maioria das espécies, a desova é controlada pela luz, com todos os indivíduos desovando aproximadamente ao mesmo tempo do dia; em muitos casos, isso ocorre ao amanhecer ou ao entardecer.[66] As águas-vivas são geralmente machos ou fêmeas (com hermafroditas ocasionais). Na maioria dos casos, os adultos liberam espermatozoides e ovos na água circundante, onde os ovos desprotegidos são fertilizados e se desenvolvem em larvas. Em algumas espécies, os espermatozoides nadam até a boca da fêmea, fertilizando os ovos dentro de seu corpo, onde permanecem durante os estágios iniciais de desenvolvimento. Em águas-vivas lunares, os ovos alojam-se em cavidades nos braços orais, que formam uma câmara de cria temporária para as larvas plânulas em desenvolvimento.[67]
A plânula é uma pequena larva coberta com cílios. Quando suficientemente desenvolvida, ela se fixa em uma superfície firme e se desenvolve em um pólipo. O pólipo geralmente consiste em um pequeno pedúnculo encimado por uma boca cercada por tentáculos voltados para cima. Os pólipos se assemelham aos de antozoários próximos, como anêmonas marinhas e corais. O pólipo de água-viva pode ser séssil, vivendo no fundo de cascos de barcos ou outros substratos, ou pode ser flutuante ou preso a pequenos pedaços de plâncton de vida livre[68] ou, raramente, peixes[69][70] ou outros invertebrados. Os pólipos podem ser solitários ou coloniais.[71] A maioria dos pólipos tem apenas milímetros de diâmetro e se alimenta continuamente. O estágio de pólipo pode durar anos.[25]
Após um intervalo e estimulado por mudanças sazonais ou hormonais, o pólipo pode começar a se reproduzir assexuadamente por brotamento e, nos Scyphozoa, é chamado de pólipo segmentador, ou escifistoma. O brotamento produz mais escifistomas e também efiras.[25] Os locais de brotamento variam por espécie; dos bulbos dos tentáculos, do manúbrio (acima da boca) ou das gônadas de hidromedusas.[68] Em um processo conhecido como estrobilização, os tentáculos do pólipo são reabsorvidos e o corpo começa a se estreitar, formando constrições transversais em vários lugares próximos à extremidade superior do pólipo. Essas constrições se aprofundam à medida que os locais de constrição migram pelo corpo, e segmentos separados conhecidos como efiras se soltam. Estes são precursores nadadores livres do estágio de medusa adulta, que é a fase de vida tipicamente identificada como uma água-viva.[25][72] As efiras, geralmente com apenas um ou dois milímetros de diâmetro inicialmente, nadam para longe do pólipo e crescem. Pólipos de Limnomedusae podem produzir assexuadamente uma forma larval de frustule, que rasteja antes de se desenvolver em outro pólipo.[25] Algumas espécies podem produzir novas medusas por brotamento diretamente do estágio de medusa. Algumas hidromedusas se reproduzem por fissão.[68]
Expectativa de vida
Pouco se sabe sobre as histórias de vida de muitas águas-vivas, pois os locais no fundo do mar onde vivem as formas bentônicas dessas espécies não foram encontrados. No entanto, uma forma estróbila que se reproduz assexuadamente pode, por vezes, viver por vários anos, produzindo novas medusas (larvas efiras) a cada ano.[73]
Uma espécie incomum, Turritopsis dohrnii, anteriormente classificada como T. nutricula,[74] pode ser efetivamente imortal devido à sua capacidade, sob certas circunstâncias, de se transformar de medusa de volta ao estágio de pólipo, escapando assim da morte que normalmente aguarda as medusas após a reprodução, se não tiverem sido comidas por algum outro organismo. Até agora, essa reversão foi observada apenas em laboratório.[75]
Locomoção
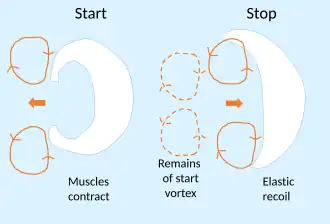
Usando a medusa-da-lua (A. aurita) como exemplo, as águas-vivas demonstraram ser os nadadores mais eficientes em termos energéticos entre todos os animais.[76] Elas se movem pela água expandindo e contraindo radialmente seus corpos em forma de sino para empurrar a água para trás. Elas pausam entre as fases de contração e expansão para criar dois anéis de vórtice. Os músculos são usados para a contração do corpo, que cria o primeiro vórtice e impulsiona o animal para a frente, mas a mesogleia é tão elástica que a expansão é alimentada exclusivamente pelo relaxamento do sino, que libera a energia armazenada da contração. Enquanto isso, o segundo anel de vórtice começa a girar mais rápido, sugando água para o sino e empurrando contra o centro do corpo, dando um impulso secundário e "gratuito" para a frente. O mecanismo, chamado de recaptura passiva de energia, funciona apenas em águas-vivas relativamente pequenas movendo-se a baixas velocidades, permitindo que o animal viaje 30% mais longe em cada ciclo de natação. As águas-vivas alcançaram um custo de transporte 48% menor (ingestão de alimentos e oxigênio versus energia gasta em movimento) do que outros animais em estudos semelhantes. Uma razão para isso é que a maior parte do tecido gelatinoso do sino é inativa, não usando energia durante a natação.[77]
Ecologia
Dieta
As águas-vivas, como outros cnidários, são geralmente carnívoras (ou parasitas),[78] alimentando-se de organismos planctônicos, crustáceos, peixes pequenos, ovos e larvas de peixes, e outras águas-vivas, ingerindo alimentos e eliminando resíduos não digeridos pela boca. Elas caçam passivamente usando seus tentáculos como linhas de deriva, ou afundam na água com os tentáculos amplamente espalhados; os tentáculos, que contêm nematocistos para atordoar ou matar a presa, podem então se flexionar para levá-la à boca.[25] Sua técnica de natação também ajuda na captura de presas; quando seu sino se expande, ele suga água, trazendo mais presas potenciais ao alcance dos tentáculos.[79]
Algumas espécies, como a Aglaura hemistoma [en], são onívoras, alimentando-se de microplâncton, que é uma mistura de zooplâncton e fitoplâncton (plantas microscópicas) como dinoflagelados.[80] Outras abrigam algas mutualistas (zooxantelas) em seus tecidos;[25] a água-viva-pintada-de-laguna (Mastigias papua [en]) é típica dessas, obtendo parte de sua nutrição dos produtos da fotossíntese e parte de zooplâncton capturado.[81][82] A água-viva-de-ponta-cabeça (Cassiopea andromeda) também tem uma relação simbiótica com microalgas, mas captura pequenos animais para complementar sua dieta. Isso é feito liberando pequenas bolas de células vivas compostas de mesogleia. Essas usam cílios para se moverem pela água e células urticantes que atordoam a presa. As bolas também parecem ter capacidades digestivas.[83]
Predação
Outras espécies de águas-vivas estão entre os predadores mais comuns e importantes de águas-vivas. As anêmonas-do-mar podem comer águas-vivas que derivam para o seu alcance. Outros predadores incluem atuns, tubarões, peixes-espada, tartarugas marinhas e pinguins.[84][85] Águas-vivas levadas para a praia são consumidas por raposas, outros mamíferos terrestres e aves.[86] Em geral, poucos animais predam águas-vivas; elas podem ser amplamente consideradas predadores de topo na cadeia alimentar. Uma vez que as águas-vivas se tornam dominantes em um ecossistema, por exemplo, por meio da pesca excessiva que remove predadores de larvas de águas-vivas, pode não haver uma maneira óbvia de restaurar o equilíbrio anterior: elas comem ovos e peixes juvenis, e competem com peixes por alimento, impedindo a recuperação dos estoques de peixes.[87]
Simbiose
Alguns peixes pequenos são imunes às ferroadas das águas-vivas e vivem entre os tentáculos, servindo como isca em uma armadilha para peixes; eles estão seguros de predadores potenciais e podem compartilhar os peixes capturados pelas águas-vivas.[88] A água-viva "bola de canhão" (Stomolophus meleagris [en]) tem uma relação simbiótica com dez espécies diferentes de peixes e com o caranguejo Libinia dubia, que vive dentro do sino, compartilhando a comida da água-viva e mordiscando seus tecidos.[89]
Eflorescências
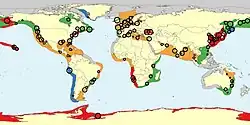
As águas-vivas formam grandes massas ou eflorescências em certas condições ambientais de corrente oceânicas, nutrientes, luz solar, temperatura, estação, disponibilidade de presas, redução de predação e concentração de oxigênio. As correntes reúnem as águas-vivas, especialmente em anos com populações excepcionalmente altas. As águas-vivas podem detectar correntes marítimas e nadar contra a corrente para se reunir em florescimentos.[91][92] As águas-vivas são mais capazes de sobreviver em águas ricas em nutrientes e pobres em oxigênio do que seus competidores, podendo assim se alimentar de plâncton sem concorrência.
As águas-vivas também podem se beneficiar de águas mais salgadas, pois estas contêm mais iodo, necessário para que os pólipos se transformem em medusas. O aumento da temperatura do mar causado pela mudança climática também pode contribuir para florescimentos de águas-vivas, porque muitas espécies de águas-vivas conseguem sobreviver em águas mais quentes.[93] O aumento de nutrientes de escoamento agrícola ou urbano com nutrientes, incluindo compostos de nitrogênio e fósforo, aumenta o crescimento de fitoplâncton, causando eutrofização e floração algal.
Quando o fitoplâncton morre, pode criar zonas mortas [en], assim chamadas porque são hipóxicas (baixas em oxigênio). Isso, por sua vez, mata peixes e outros animais, mas não as águas-vivas,[94] permitindo que elas floresçam.[95][96] As populações de águas-vivas podem estar se expandindo globalmente como resultado do escoamento terrestre e da pesca excessiva de seus predadores naturais.[97][98] As águas-vivas estão bem posicionadas para se beneficiar da perturbação dos ecossistemas marinhos. Elas se reproduzem rapidamente; predam muitas espécies, enquanto poucas espécies as predam; e se alimentam pelo toque, em vez de visualmente, o que permite que se alimentem eficazmente à noite e em águas turvas.[99][100] Pode ser difícil para os estoques de peixes se restabelecerem em ecossistemas marinhos uma vez dominados por águas-vivas, porque as águas-vivas se alimentam de plâncton, que inclui ovos e larvas de peixe.[101][102][96]
.jpg)
Como suspeitado no início deste século,[107][108] as eflorescências de águas-vivas estão aumentando em frequência. Entre 2013 e 2020, a Comissão de Ciência do Mediterrâneo monitorou semanalmente a frequência desses surtos em águas costeiras, de Marrocos ao mar Negro, revelando uma frequência relativamente alta desses florescimentos quase o ano todo, com picos observados de março a julho e, frequentemente, novamente no outono. Os florescimentos são causados por diferentes espécies de águas-vivas, dependendo de sua localização na bacia: observa-se uma clara predominância de surtos de Pelagia noctiluca [en] e Velella velella no Mediterrâneo ocidental, de Rhizostoma pulmo [en] e Rhopilema nomadica no Mediterrâneo oriental, e de Aurelia aurita e Mnemiopsis leidyi no Mar Negro.[109]
Algumas populações de águas-vivas que mostraram aumentos claros nas últimas décadas são espécies invasoras, recém-chegadas de outros habitats, como do Mar Negro, Mar Cáspio, Mar Báltico, Mediterrâneo central e oriental, Havaí, e partes tropicais e subtropicais do Atlântico Ocidental (incluindo o Mar do Caribe, Golfo do México e Brasil).[105][106]
Os florescimentos de águas-vivas podem ter um impacto significativo na estrutura da comunidade. Algumas espécies carnívoras de águas-vivas predam zooplâncton, enquanto outras pastam em produtores primários.[110] Reduções no zooplâncton e ictioplâncton devido a um florescimento de águas-vivas podem reverberar pelos níveis tróficos. Populações de águas-vivas de alta densidade podem superar outros predadores e reduzir o recrutamento de peixes.[111] O aumento do pastoreio em produtores primários por águas-vivas também pode interromper a transferência de energia para níveis tróficos superiores.[112]
Durante os florescimentos, as águas-vivas alteram significativamente a disponibilidade de nutrientes em seu ambiente. Os florescimentos requerem grandes quantidades de nutrientes orgânicos disponíveis na coluna de água para crescer, limitando a disponibilidade para outros organismos.[113] Algumas águas-vivas têm uma relação simbiótica com dinoflagelados unicelulares, permitindo-lhes assimilar carbono inorgânico, fósforo e nitrogênio, criando concorrência para o fitoplâncton.[113] Sua grande biomassa as torna uma fonte importante de matéria orgânica dissolvida e particulada para comunidades microbianas por meio da excreção, produção de muco e decomposição.[90][114] Os micróbios decompõem a matéria orgânica em amônio e fosfato inorgânicos. No entanto, a baixa disponibilidade de carbono desloca o processo de produção para respiração, criando áreas de baixo oxigênio, tornando o nitrogênio e fósforo inorgânicos dissolvidos amplamente indisponíveis para a produção primária.
Esses florescimentos também causam impactos nas indústrias. As águas-vivas podem superar os peixes ao utilizar nichos abertos em pescarias com excesso de pesca.[115] A captura de águas-vivas pode sobrecarregar os equipamentos de pesca e levar a despesas relacionadas a equipamentos danificados. Usinas de energia foram desligadas devido a águas-vivas bloqueando o fluxo de água de resfriamento.[116] Os florescimentos também foram prejudiciais para o turismo, causando um aumento nos casos de ferroadas e, por vezes, o fechamento de praias.[117]
As águas-vivas formam um componente de "quedas de geleia", eventos em que o zooplâncton gelatinoso cai para o fundo do mar, fornecendo alimento para os organismos bentônicos ali.[118] Em regiões temperadas e subpolares, as quedas de geleia geralmente ocorrem imediatamente após um florescimento.[119]
Habitats

A maioria das águas-vivas são animais marinhos, embora algumas hidromedusas habitem água doce. O exemplo de água -vida de água doce mais conhecido é a hidromedusa de distribuição cosmopolita, Craspedacusta sowerbii [en]. Ela tem menos de 2,5 cm de diâmetro, é incolor e não ferroa.[120] Algumas populações de águas-vivas tornaram-se restritas a lagos salgados costeiros, como o "Lago das Águas-vivas" em Palau.[121] O Lago das Águas-vivas é um lago marinho onde milhões de águas-vivas douradas (Mastigias spp.) migram horizontalmente pelo lago diariamente.[82]
Embora a maioria das águas-vivas viva bem longe do fundo do oceano e faça parte do plâncton, algumas espécies estão intimamente associadas ao fundo por grande parte de suas vidas e podem ser consideradas bentônicas. As águas-vivas de cabeça para baixo do gênero Cassiopea geralmente ficam no fundo de lagoas rasas, onde às vezes pulsam suavemente com o topo do guarda-chuva voltado para baixo. Mesmo algumas espécies de hidromedusas e esifozoárias de águas profundas são geralmente coletadas no fundo ou perto dele. Todas as Stauromedusas são encontradas fixadas a algas ou materiais rochosos, ou outros materiais firmes no fundo.[122]
Algumas espécies se adaptam explicitamente ao fluxo maré. Na baía de Roscoe (Canadá), as águas-vivas seguem a corrente na maré baixa até atingirem uma área de cascalho elevado, e então descem abaixo da corrente. Elas permanecem em águas paradas até que a maré suba, ascendendo e permitindo que a corrente as leve de volta à baía. Elas também evitam ativamente a água doce do derretimento de neve das montanhas, mergulhando até encontrarem sal suficiente.[2]
Parasitas
As águas-vivas são hospedeiras de uma ampla variedade de organismos parasitas. Elas atuam como hospedeiras intermediárias de vermes endoparasitas, com a infecção sendo transferida para o hospedeiro definitivo, peixes, após a predação. Alguns trematódeos do gênero Digenea, usam águas-vivas como seus segundos hospedeiros intermediários. Os peixes são infectados pelos trematódeos quando se alimentam de águas-vivas infectadas.[123][124]
Relação com humanos

Pesca
As águas-vivas são consumidas há muito tempo em algumas partes do mundo.[3] Pescadores começaram a colher a água-viva Stomolophus meleagris [en] ao longo da costa sul do Atlântico dos Estados Unidos e no Golfo do México para exportação para a Ásia.[126]
As águas-vivas também são colhidas por seu colágeno, que está sendo investigado para uso em várias aplicações, incluindo o tratamento de artrite reumatoide.[127]
Aquacultura e pescadores de outras espécies frequentemente sofrem perdas severas – e, consequentemente, perdas de produtividade – devido às águas-vivas.[128][129]
Produtos

Aristóteles afirmou em Partes dos Animais IV, 6 que as águas-vivas (urtigas-do-mar) eram consumidas no inverno em um ensopado de peixe.[130]
Em alguns países, incluindo China, Japão e Coreia, as águas-vivas são uma iguaria. A água-viva é seca para evitar deterioração. Apenas cerca de 12 espécies de águas-vivas esifozoárias pertencentes à ordem Rhizostomeae são colhidas para alimentação, principalmente no sudeste da Ásia.[131] Rizostomas, especialmente Rhopilema esculentum na China (海蜇 hǎizhé, 'ferrões do mar') e S. meleagris nos Estados Unidos, são preferidas devido aos seus corpos maiores e mais rígidos e porque suas toxinas são inofensivas para humanos.[126]
Os métodos tradicionais de processamento, realizados por um mestre de águas-vivas, envolvem um procedimento multifásico de 20 a 40 dias no qual, após a remoção das gônadas e membranas mucosas, o guarda-chuva e os braços orais são tratados com uma mistura de sal de cozinha e alume, e depois são comprimidos. O processamento torna a água-viva mais seca e ácida, produzindo uma textura crocante. As águas-vivas preparadas dessa forma retêm 7–10% de seu peso original, e o produto processado consiste em aproximadamente 94% de água e 6% de proteína. A água-viva recém-processada tem uma cor branca e cremosa e fica amarela ou marrom durante o armazenamento prolongado.[126]
Na China, as águas-vivas processadas são dessalinizadas por imersão em água durante a noite e consumidas cozidas ou cruas. O prato é frequentemente servido desfiado com um molho de óleo, molho de soja, vinagre e açúcar, ou como uma salada com vegetais. No Japão, as águas-vivas curadas são enxaguadas, cortadas em tiras e servidas com vinagre como aperitivo.[126][132] Produtos dessalinizados prontos para consumo também estão disponíveis.[126]
Biotecnologia
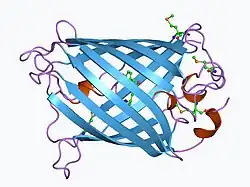
Plínio, o Velho relatou em sua História Natural que o muco da água-viva "Pulmo marinus" produzia luz quando esfregado em uma bengala.[133]
Em 1961, Osamu Shimomura extraiu a proteína fluorescente verde (GFP) e outra proteína bioluminescente, chamada equorina [en], da hidromedusa abundante Aequorea victoria, enquanto estudava fotoproteínas que causam bioluminescência nesta espécie.[134] Três décadas depois, Douglas Prasher sequenciou e clonou o gene para a GFP.[135] Martin Chalfie descobriu como usar a GFP como um marcador fluorescente de genes inseridos em outras células ou organismos.[136] Roger Tsien manipulou quimicamente a GFP para produzir outras cores fluorescentes para uso como marcadores.
Em 2008, Shimomura, Chalfie e Tsien ganharam o Prêmio Nobel de Química pelo seu trabalho com a proteína verde fluorescente.[134] A GFP produzida artificialmente tornou-se amplamente utilizada como uma etiqueta fluorescente para mostrar quais células ou tecidos expressam genes específicos. A técnica de engenharia genética funde o gene de interesse ao gene da GFP. O DNA fundido é então inserido em uma célula, para gerar uma linhagem celular ou (via técnicas de FIV) um animal inteiro portando o gene. Na célula ou animal, o gene artificial é ativado nos mesmos tecidos e no mesmo momento que o gene normal, criando uma fusão da proteína normal com a GFP anexada ao final, iluminando o animal ou célula revela quais tecidos expressam essa proteína — ou em que estágio de desenvolvimento. A fluorescência mostra onde o gene é expresso.[137]
Exibição em aquários

As águas-vivas são exibidas em muitos aquários públicos. Frequentemente, o fundo do tanque é azul e os animais são iluminados por luz lateral, aumentando o contraste entre o animal e o fundo. Em condições naturais, muitas águas-vivas são tão transparentes que são quase invisíveis.[138] As águas-vivas não são adaptadas a espaços fechados. Elas dependem de correntes para transportá-las de um lugar para outro. Exposições profissionais, como as do aquário da baía de Monterey, apresentam fluxos de água precisos, geralmente em tanques circulares para evitar que os espécimes fiquem presos nos cantos. A saída de água é espalhada por uma grande área de superfície e a entrada de água entra como uma lâmina de água em frente à saída, para que as águas-vivas não sejam sugadas para dentro dela.[139] A partir de 2009, as águas-vivas estavam se tornando populares em aquários domésticos, onde requerem equipamentos semelhantes.[140]
Ferroadas
As águas-vivas estão armadas com nematocistos, um tipo de célula urticante especializada.[141] O contato com um tentáculo de água-viva pode desencadear milhões de nematocistos que perfuram a pele e injetam veneno,[142] mas apenas o veneno de algumas espécies causa uma reação adversa em humanos.[143] Em um estudo publicado na Communications Biology, pesquisadores descobriram uma espécie de água-viva chamada Cassiopea xamachana [en] que, quando acionada, libera pequenas bolas de células que nadam ao redor da água-viva, ferroando tudo em seu caminho. Os pesquisadores descreveram essas bolas como "granadas microscópicas autopropulsadas" e as nomearam "cassiosomas".[144]
Os efeitos das ferroadas variam de leve desconforto a dor extrema e morte.[145][146] A maioria das ferroadas de águas-vivas não é fatal, mas as ferroadas de algumas águas-vivas cubozoárias, como a vespa-do-mar, podem ser mortais. As ferroadas podem causar anafilaxia (uma forma de choque), que pode ser fatal. As águas-vivas matam de 20 a 40 pessoas por ano apenas nas Filipinas. Em 2006, a Cruz Vermelha espanhola tratou 19.000 nadadores ferroados ao longo da Costa Brava.[146][147]
O vinagre (3–10% de ácido acético aquoso) pode ajudar com ferroadas de águas-vivas cubozoárias[148][149] mas não com as ferroadas da caravela-portuguesa.[148] Limpar a área de restos de água-viva e tentáculos reduz a ativação de nematocistos.[150] Raspar a pele afetada, como com a borda de um cartão de crédito, pode remover nematocistos remanescentes.[151] Após a limpeza da pele de nematocistos, o creme de hidrocortisona aplicado localmente reduz a dor e a inflamação.[152] Antihistamínicos podem ajudar a controlar a coceira.[151] Antivenenos baseados em imunidade são usados para ferroadas graves de águas-vivas cubozoárias.[153][154]
Na Ilha de Elba e em Córsega, a planta Dittrichia viscosa é agora usada por residentes e turistas para tratar ferroadas de águas-vivas, abelhas e vespas, pressionando folhas frescas na pele com resultados rápidos.
-
 Cubomedusas são pequenas e venenosas.
Cubomedusas são pequenas e venenosas. -
 Dermatite por contato com água-viva.
Dermatite por contato com água-viva. -
 Uma bandeira na praia de Zarautz alertando sobre a presença de águas-vivas na água.
Uma bandeira na praia de Zarautz alertando sobre a presença de águas-vivas na água. -
![Bengisu Avcı [en], uma nadadora turca, em maio de 2024 após entrar em contato com águas-vivas enquanto tentava atravessar o Canal de Molokaʻi no Havaí.](./_assets_/0c70a452f799bfe840676ee341124611/Denizanas%C4%B1_temas_eden_Bengisu_Avc%C4%B1%252C_tekneye_%C3%A7%C4%B1kmak_zorunda_kald%C4%B1.jpg) Bengisu Avcı [en], uma nadadora turca, em maio de 2024 após entrar em contato com águas-vivas enquanto tentava atravessar o Canal de Molokaʻi no Havaí.
Bengisu Avcı [en], uma nadadora turca, em maio de 2024 após entrar em contato com águas-vivas enquanto tentava atravessar o Canal de Molokaʻi no Havaí.
Problemas mecânicos
Águas-vivas em grandes quantidades podem encher e rasgar redes de pesca e esmagar peixes capturados.[155] Elas podem entupir equipamentos de resfriamento, tendo desativado usinas elétricas em vários países; águas-vivas causaram um apagão em cascata nas Filipinas em 1999,[146] além de danificar a usina nuclear de Diablo Canyon na Califórnia em 2008.[156] Elas também podem interromper usinas de dessalinização e motores de navios.[155][157]
Ver também
- Peixe-lua, um predador significativo de águas-vivas
- Ctenophora
Referências
- ↑ «Fossil Record Reveals Elusive Jellyfish More Than 500 Million Years Old». ScienceDaily (em inglês). Consultado em 10 de fevereiro de 2023
- ↑ a b c Angier, Natalie (6 de junho de 2011). «So Much More Than Plasma and Poison». The New York Times. Consultado em 2 de dezembro de 2011. Cópia arquivada em 18 de maio de 2013
- ↑ a b Isabelle Rodd (20 de outubro de 2020). «Why jellyfish could be a 'perfect food'». BBC News. Consultado em 7 de maio de 2023
- ↑ a b «jellyfish». Online Etymology Dictionary. Consultado em 9 de junho de 2018
- ↑ Kelman, Janet Harvey; Rev. Theodore Wood (1910). The Sea-Shore, Shown to the Children. London: T. C. & E. C. Jack. p. 146. OL 7043926M
- ↑ Kaplan, Eugene H.; Kaplan, Susan L.; Peterson, Roger Tory (agosto de 1999). A Field Guide to Coral Reefs: Caribbean and Florida. [S.l.]: Boston : Houghton Mifflin. p. 55. ISBN 978-0-618-00211-5
- ↑ «Flower Hat Jelly». 6 de abril de 2009. Consultado em 10 de fevereiro de 2023. Arquivado do original em 6 de abril de 2009
- ↑ «What is a Fish?». Encyclopedia of Life. Consultado em 13 de outubro de 2018. Cópia arquivada em 24 de março de 2018.
And most people know that lampreys, sharks, rays, eels, seahorses, and other strange-looking aquatic creatures are fishes, while shellfish, cuttlefish, starfish, crayfish, and jellyfish (despite their names) are not fishes.
- ↑ Brotz, Lucas. Changing Jellyfish Populations: Trends in Large Marine Ecosystems Arquivado em 16 abril 2013 no Wayback Machine. 2011. p.1.
- ↑ Coulombe, Deborah A. (14 de fevereiro de 1990). Seaside Naturalist: A Guide to Study at the Seashore. [S.l.]: Simon & Schuster. p. 60. ISBN 978-0-671-76503-3. Consultado em 20 de março de 2013. Cópia arquivada em 31 de dezembro de 2013
- ↑ Klappenbach, Laura. «Ten Facts about Jellyfish». Consultado em 24 de janeiro de 2010. Cópia arquivada em 26 de fevereiro de 2009
- ↑ Lipton, James (1991). An Exaltation of Larks (em inglês). [S.l.]: Viking. ISBN 978-0-670-30044-0
- ↑ Maciver, Angus (2004). First Aid in English (em inglês). [S.l.]: Hodder Gibson (Hachette). ISBN 978-1-444-19376-3
- ↑ Cartwright, Paulyn; Halgedahl, Susan L.; Hendricks, Jonathan R.; et al. (2007). Humphries, Stuart, ed. «Exceptionally Preserved Jellyfishes from the Middle Cambrian». PLOS ONE. 2 (10): e1121. Bibcode:2007PLoSO...2.1121C. ISSN 1932-6203. PMC 2040521
 . PMID 17971881. doi:10.1371/journal.pone.0001121
. PMID 17971881. doi:10.1371/journal.pone.0001121
- ↑ «Jellyfish». Merriam-Webster. 1 de setembro de 2018. Consultado em 11 de setembro de 2018
- ↑ a b c d e f g h i «Jellyfish Spotting | Species of Jellyfish». Policy-oriented marine Environmental Research in the Southern European Seas (PERSEUS). Consultado em 28 de agosto de 2018
- ↑ a b Mills, C. E. (8 de novembro de 2010). «Ctenophores». University of Washington. Consultado em 28 de agosto de 2018
- ↑ a b «Our jelly-like relatives: Common misconceptions about salps». Nereus Program. Consultado em 28 de agosto de 2018
- ↑ a b Zapata, Felipe; Goetz, Freya E.; Smith, Stephen A.; et al. (2015). «Phylogenomic Analyses Support Traditional Relationships within Cnidaria». PLOS ONE. 10 (10): e0139068. Bibcode:2015PLoSO..1039068Z. PMC 4605497
 . PMID 26465609. doi:10.1371/journal.pone.0139068
. PMID 26465609. doi:10.1371/journal.pone.0139068
- ↑ Kayal, Ehsan; Bentlage, Bastian; Sabrina Pankey, M.; et al. (2018). «Phylogenomics provides a robust topology of the major cnidarian lineages and insights on the origins of key organismal traits». BMC Evolutionary Biology. 18 (1). 68 páginas. Bibcode:2018BMCEE..18...68K. PMC 5932825
 . doi:10.1186/s12862-018-1142-0
. doi:10.1186/s12862-018-1142-0
- ↑ «STAUROMEDUSAE UK An online guide to the Stalked jellyfish (Stauromedusae) found around the coastal waters of the United Kingdom and Ireland. Includes notes on their identification, and where and how to find them. BACK UK Checklist for Stalked jellyfish (Stauromedusae)». Stauromedusae UK. Consultado em 28 de agosto de 2018
- ↑ Schierwater, Bernd; Helm, Rebecca R.; Dunn, Casey W. (2017). «Indoles induce metamorphosis in a broad diversity of jellyfish, but not in a crown jelly (Coronatae)». PLOS ONE. 12 (12): e0188601. Bibcode:2017PLoSO..1288601H. PMC 5744923
 . PMID 29281657. doi:10.1371/journal.pone.0188601
. PMID 29281657. doi:10.1371/journal.pone.0188601
- ↑ Osborn, K. J. (2014). «Red Paper Lantern Jellyfish». Smithsonian. Consultado em 13 de outubro de 2018
- ↑ Daley, Jason (1 de março de 2017). «Take a Peek at the Mesmerizing 'Cosmic Jellyfish'». Smithsonian. Consultado em 28 de agosto de 2018
- ↑ a b c d e f g h i j k l m n o p q r Ruppert, Edward E.; Fox, Richard, S.; Barnes, Robert D. (2004). Invertebrate Zoology, 7th edition. [S.l.]: Cengage Learning. pp. 148–174. ISBN 978-81-315-0104-7
- ↑ a b Cnidaria Arquivado em 2012-09-21 no Wayback Machine, Tree of Life.
- ↑ Marques, A.C.; A. G. Collins (2004). «Cladistic analysis of Medusozoa and cnidarian evolution». Invertebrate Biology. 123: 23–42. doi:10.1111/j.1744-7410.2004.tb00139.x
- ↑ Kramp, P.L. (1961). «Synopsis of the Medusae of the World». Journal of the Marine Biological Association of the United Kingdom. 40: 1–469. Bibcode:1961JMBUK..40....7K. doi:10.1017/s0025315400007347
- ↑ Moon, Justin; Caron, Jean-Bernard; Moysiuk, Joseph (9 de agosto de 2023). «A macroscopic free-swimming medusa from the middle Cambrian Burgess Shale». Proceedings of the Royal Society B: Biological Sciences (em inglês). 290 (2004). ISSN 0962-8452. PMC 10394413
 . PMID 37528711. doi:10.1098/rspb.2022.2490
. PMID 37528711. doi:10.1098/rspb.2022.2490
- ↑ Hsieh, Yun-Hwa; Rudloe, Jack (1994). «Potential of utilizing jellyfish as food in Western countries». Trends in Food Science & Technology. 5 (7): 225–229. doi:10.1016/0924-2244(94)90253-4
- ↑ «Jellyfish - Visual Dictionary». infovisual.info. Consultado em 10 de fevereiro de 2023. Arquivado do original em 11 de junho de 2023
- ↑ Waggoner, Ben; Collins, Allen G. «Cubozoa: More on Morphology». University of California Museum of Paleontology. Consultado em 6 de janeiro de 2019
- ↑ «Nematocysts». Jellieszone. 2 de abril de 2015. Consultado em 29 de março de 2014. Cópia arquivada em 2 de abril de 2015
- ↑ Kier, William (2012). «The diversity of hydrostatic skeletons». Journal of Experimental Biology. 215 (Pt 8): 1247–1257. PMID 22442361. doi:10.1242/jeb.056549

- ↑ Satterlie, R. A. (2002). «Neuronal control of swimming in jellyfish: a comparative story». Canadian Journal of Zoology. 80 (10): 1654–1669. doi:10.1139/z02-138. Arquivado do original (PDF) em 12 de julho de 2013
- ↑ Katsuki, Takeo; Greenspan, Ralph J. (2013). «Jellyfish nervous systems». Current Biology. 23 (14): R592–R594. Bibcode:2013CBio...23.R592K. PMID 23885868. doi:10.1016/j.cub.2013.03.057

- ↑ Satterlie, Richard A. (2011). «Do jellyfish have central nervous systems?». Journal of Experimental Biology. 214 (8): 1215–1223. PMID 21430196. doi:10.1242/jeb.043687

- ↑ Wehner, R. (2005). «Sensory physiology: brainless eyes» (PDF). Nature. 435 (7039): 157–159. Bibcode:2005Natur.435..157W. PMID 15889076. doi:10.1038/435157a. Cópia arquivada (PDF) em 29 de julho de 2013
- ↑ «Multi-eyed jellyfish helps with Darwin's puzzle». New Scientist (em inglês). Consultado em 10 de fevereiro de 2023
- ↑ a b c d Nilsson, DE (2013). «Eye evolution and its functional basis». Visual Neuroscience. 30 (1–2): 5–20. PMC 3632888
 . PMID 23578808. doi:10.1017/S0952523813000035
. PMID 23578808. doi:10.1017/S0952523813000035
- ↑ a b c d e f g h i j k l m Garm, Anders; Ekström, Peter (2010). «Evidence for Multiple Photosystems in Jellyfish». Chapter 2 – Evidence for Multiple Photosystems in Jellyfish. International Review of Cell and Molecular Biology. 280. [S.l.]: Academic Press. pp. 41–78. ISBN 9780123812605. ISSN 1937-6448. PMID 20797681. doi:10.1016/S1937-6448(10)80002-4
- ↑ Suga H, Tschopp P, Graziussi DF, et al. (10 de agosto de 2010). «Flexibly deployed Pax genes in eye development at the early evolution of animals demonstrated by studies on a hydrozoan jellyfish». PNAS. 107 (32): 14263–14268. Bibcode:2010PNAS..10714263S. PMC 2922549
 . PMID 20660753. doi:10.1073/pnas.1008389107
. PMID 20660753. doi:10.1073/pnas.1008389107
- ↑ a b c d O'Connor M, Garm A, Nilsson DE (2009). «Structure and Optics of the Eyes of the Box Jellyfish Chiropsella Bronzie». Journal of Comparative Physiology A. 195 (6): 557–569. PMID 19347342. doi:10.1007/s00359-009-0431-x
- ↑ Nilsson DE, Gislén L, Coates M, et al. (2005). «Advanced optics in a jellyfish eye». Nature. 435 (7039): 201–205. Bibcode:2005Natur.435..201N. PMID 15889091. doi:10.1038/nature03484
- ↑ a b Piatigorsky J, Kozmik Z (2004). «Cubozoan jellyfish: an Evo/Devo model for eyes and other sensory systems». Int. J. Dev. Biol. 48 (8–9): 719–729. PMID 15558464. doi:10.1387/ijdb.041851jp

- ↑ a b Gray GC, Martin VJ, Satterlie RA (agosto de 2009). «Ultrastructure of the retinal synapses in cubozoans» (PDF). Biol Bull. 217 (1): 35–49. PMID 19679721. doi:10.1086/BBLv217n1p35
- ↑ Berger, Edward W (1898). «The Histological Structure of the Eyes of Cubomedusae». Journal of Comparative Neurology. 8 (3): 223–230. doi:10.1002/cne.910080317
- ↑ Suga, Hiroshi; Schmid, Volker; Gehring, Walter J. (2008). «Evolution and Functional Diversity of Jellyfish Opsins». Current Biology. 18 (1): 51–55. Bibcode:2008CBio...18...51S. ISSN 0960-9822. PMID 18160295. doi:10.1016/j.cub.2007.11.059

- ↑ Piatigorsky J, Horwitz J, Kuwabara T, Cutress C (1989). «The Cellular Eye Lens and Crystallins of Cubomedusan Jellyfish». Journal of Comparative Physiology A. 164 (5): 577–587. PMID 2565398. doi:10.1007/bf00614500
- ↑ a b Seymour, Jamie E.; O'Hara, Emily P. (2020). «Pupillary Response to Light in Three Species of Cubozoa (Box Jellyfish)». Plankton and Benthos Research. 15 (2): 73–77. doi:10.3800/pbr.15.73

- ↑ a b Mills, C.E.; Hirano, Y.M. (2007). Encyclopedia of Tidepools and Rocky Shores: Hydromedusae. [S.l.]: University of California Press. pp. 286–288. ISBN 978-0-520-25118-2
- ↑ Mills, C.E. (1976). «Podocoryne selena, a new species of hydroid from the Gulf of Mexico, and a comparison with Hydractinia echinata». Biological Bulletin. 151 (1): 214–224. JSTOR 1540715. doi:10.2307/1540715
- ↑ Costello, J. (1988). «Laboratory culture and feeding of the hydromedusa Cladonema californicum Hyman (Anthomedusa: Cladonemidae)». Journal of Experimental Marine Biology and Ecology. 123 (2): 177–188. Bibcode:1988JEMBE.123..177C. doi:10.1016/0022-0981(88)90168-2
- ↑ «Rare sighting of a lion's mane jellyfish in Tramore Bay». Waterford Today. 1 de agosto de 2007. Consultado em 18 de outubro de 2010. Cópia arquivada em 30 de maio de 2010
- ↑ «Lion's Mane Jellyfish – Reference Library». redOrbit. 12 de junho de 2003. Consultado em 18 de outubro de 2010. Cópia arquivada em 30 de julho de 2010
- ↑ «150 Stung By Jellyfish At Rye Beach». Wmur.com. 21 de julho de 2010. Consultado em 11 de junho de 2018. Arquivado do original em 14 de outubro de 2011
- ↑ Omori, Makoto; Kitamura, Minoru (2004). «Taxonomic review of three Japanese species of edible jellyfish (Scyphozoa: Rhizostomeae)» (PDF). Plankton Biology and Ecology. 51 (1): 36–51. Cópia arquivada (PDF) em 23 de março de 2012
- ↑ Uye, Shin-Ichi (2008). «Blooms of the giant jellyfish Nemopilema nomurai: a threat to the fisheries sustainability of the East Asian Marginal Seas» (PDF). Plankton & Benthos Research. 3 (Supplement): 125–131. doi:10.3800/pbr.3.125
 . Cópia arquivada (PDF) em 16 de maio de 2013
. Cópia arquivada (PDF) em 16 de maio de 2013
- ↑ «Giant Echizen jellyfish off Japan coast». BBC. 30 de novembro de 2009. Cópia arquivada em 1 de janeiro de 2011
- ↑ Kramp, P.L. (1961). «Synopsis of the medusae of the world». Journal of the Marine Biological Association of the United Kingdom. 40: 1–469. Bibcode:1961JMBUK..40....7K. doi:10.1017/s0025315400007347
- ↑ Bourton, Jody (23 de abril de 2010). «Giant deep sea jellyfish filmed in Gulf of Mexico». BBC Earth News. Cópia arquivada em 5 de julho de 2010
- ↑ «Photos of Antarctic Giant Jelly (Desmonema glaciale) • iNaturalist»
- ↑ League, Michael (11 de outubro de 2011). «The Way to End a Dive». McMurdo Station, Antarctica. PolarTREC. Consultado em 13 de junho de 2023. Arquivado do original em 13 de junho de 2023
- ↑ «Diving underwater with giant jellyfish». 26 de abril de 2010
- ↑ «How do jellyfish reproduce? What effect does their sting have on humans? What's the difference between red and translucent jellyfish?». Scientific American. 15 de outubro de 2013. Consultado em 22 de outubro de 2013. Cópia arquivada em 23 de outubro de 2013
- ↑ Mills, Claudia (1983). «Vertical migration and diel activity patterns of hydromedusae: studies in a large tank». Journal of Plankton Research. 5 (5): 619–635. doi:10.1093/plankt/5.5.619
- ↑ Bishop, Andrew. «Moon Jelly (Aurelia aurita)». Marine Invertebrates of Bermuda. Consultado em 11 de junho de 2018. Arquivado do original em 5 de outubro de 2017
- ↑ a b c Mills, C. E. (1987). J. Bouillon; F. Boero; F. Cicogna; P. F. S. Cornelius, eds. In situ and shipboard studies of living hydromedusae and hydroids: preliminary observations of life-cycle adaptations to the open ocean. Modern Trends in the Systematics, Ecology, and Evolution of Hydroids and Hydromedusae. [S.l.]: Clarendon Press. ISBN 978-0-19-857190-2
- ↑ Fewkes, J. Walter (1887). «A hydroid parasitic on a fish». Nature. 36 (939): 604–605. Bibcode:1887Natur..36..604F. doi:10.1038/036604b0
- ↑ Schuchert, Peter. «The Hydrozoa». Consultado em 24 de janeiro de 2010. Cópia arquivada em 4 de fevereiro de 2010
- ↑ «How Jellyfish Grow, From Eggs to Polyps to Medusas». ThoughtCo (em inglês). Consultado em 10 de fevereiro de 2023
- ↑ Hughes, Clare. «Lifecycle of the Box Jellyfish». Artforlibraries.org. Consultado em 2 de janeiro de 2016. Cópia arquivada em 4 de março de 2016
- ↑ Brusca, Richard (2016). Invertebrates. [S.l.]: Sinauer Associates. p. 310. ISBN 978-1-60535-375-3
- ↑ Miglietta, M. P.; Piraino, S.; Kubota, S.; Schuchert, P. (2007). «Species in the genus Turritopsis (Cnidaria, Hydrozoa): a molecular evaluation». Journal of Zoological Systematics and Evolutionary Research. 45 (1): 11–19. doi:10.1111/j.1439-0469.2006.00379.x

- ↑ Piraino, S.; Boero, F.; Aeschbach, B.; Schmid, V. (1996). «Reversing the life cycle: medusae transforming into polyps and cell transdifferentiation in Turritopsis nutricula (Cnidaria, Hydrozoa)». Biological Bulletin. 190 (3): 302–312. JSTOR 1543022. PMID 29227703. doi:10.2307/1543022
- ↑ Rathi, Akshat (15 de maio de 2014). «Jellyfish are the most energy-efficient-swimmers, new metric confirms». Ars Technica. Consultado em 3 de dezembro de 2014. Cópia arquivada em 3 de novembro de 2014
- ↑ Gemmell, B. J.; Costello, J. H.; Colin, S. P.; et al. (2013). «Passive energy recapture in jellyfish contributes to propulsive advantage over other metazoans». Proceedings of the National Academy of Sciences. 110 (44): 17904–17909. Bibcode:2013PNAS..11017904G. PMC 3816424
 . PMID 24101461. doi:10.1073/pnas.1306983110
. PMID 24101461. doi:10.1073/pnas.1306983110
- ↑ Brusca, Richard (2016). Invertebrates. [S.l.]: Sinauer Associates. p. 296. ISBN 978-1-60535-375-3.
All cnidarians are carnivores (or parasites). Typically, nematocyst-laden feeding tentacles capture animal prey and carry it to the mouth region where it is ingested whole.
- ↑ «Bigger jellyfish inheriting the ocean, study finds». msnbc.com. 15 de setembro de 2011. Consultado em 3 de dezembro de 2014. Arquivado do original em 14 de julho de 2014
- ↑ Davies, C.H.; Slotwinski, A.S. «Australian Marine Zooplankton-Jellyfish, Cladocerans» (PDF). Institute for Marine and Antarctic Studies, University of Tasmania. Consultado em 12 de outubro de 2018
- ↑ Dawson, Michael N. (2000). «Variegated mesocosms as alternatives to shore-based planktonkreisels: notes on the husbandry of jellyfish from marine lakes». Journal of Plankton Research. 22 (9): 1673–1682. doi:10.1093/plankt/22.9.1673

- ↑ a b Dawson, Mike N.; Martin, Laura E.; Lolita K, Lolita K.; Penland (maio de 2001). Jellyfish swarms, tourists, and the Christ-child. Hydrobiologia. 451. [S.l.]: Springer. pp. 131–144. ISBN 978-0-7923-6964-6. doi:10.1023/A:1011868925383
- ↑ Nemo, Leslie (13 de fevereiro de 2020). «Venomous Snot Helps These Jellyfish Sting Without Their Tentacles». Discover. Consultado em 11 de julho de 2021
- ↑ Yin, Steph (29 de setembro de 2017). «Who's Eating Jellyfish? Penguins, That's Who». The New York Times. Consultado em 4 de outubro de 2017. Cópia arquivada em 1 de outubro de 2017
- ↑ Thiebot, Jean-Baptiste; Arnould, John P. Y.; Gómez-Laich, Agustina; et al. (2017). «Jellyfish and other gelata as food for four penguin species – insights from predator-borne videos». Frontiers in Ecology and the Environment. 15 (8): 437–441. Bibcode:2017FrEE...15..437T. doi:10.1002/fee.1529
- ↑ Gershwin, Lisa-Ann (2016). Jellyfish: A Natural History. [S.l.]: University of Chicago Press. p. 140. ISBN 978-0-226-28767-6
- ↑ Gershwin, Lisa-Ann (2013). Stung!: On Jellyfish Blooms and the Future of the Ocean. [S.l.]: University of Chicago Press. pp. 274–. ISBN 978-0-226-02010-5. Cópia arquivada em 6 de agosto de 2016
- ↑ colugo7 (2006). «The jellyfish». Tree of Life Web Project. Consultado em 7 de junho de 2018. Arquivado do original em 12 de junho de 2018
- ↑ Griffin, DuBose B.; Murphy, Thomas M. «Cannonball Jellyfish» (PDF). South Carolina Department of Natural Resources. Consultado em 7 de junho de 2018. Arquivado do original (PDF) em 19 de janeiro de 2008
- ↑ a b Brotz, Lucas; Cheung, William W. L.; Kleisner, Kristin; et al. (2012). «Increasing jellyfish populations: trends in Large Marine Ecosystems». Hydrobiologia. 688: 3–20. doi:10.1007/s10750-012-1039-7

- ↑ Gill, Victoria. «Jellyfish 'can sense ocean currents'». BBC News. Consultado em 26 de janeiro de 2015. Cópia arquivada em 26 de janeiro de 2015
- ↑ Hays, Graeme C. (2017). «Ocean currents and marine life». Current Biology. 27 (11): R470–R473. Bibcode:2017CBio...27.R470H. PMID 28586681. doi:10.1016/j.cub.2017.01.044
 . hdl:10536/DRO/DU:30100274
. hdl:10536/DRO/DU:30100274
- ↑ Shubin, Kristie (10 de dezembro de 2008). «Anthropogenic Factors Associated with Jellyfish Blooms – Final Draft II». Tropical Field Courses: Western Program: Miami University. Consultado em 19 de novembro de 2009. Cópia arquivada em 14 de junho de 2010
- ↑ «What is a dead zone?». National Ocean Service. Consultado em 3 de outubro de 2018
- ↑ Yong, Ed (6 de junho de 2011). «Jellyfish shift ocean food webs by feeding bacteria with mucus and excrement». Discover Magazine. Consultado em 3 de outubro de 2018. Arquivado do original em 6 de novembro de 2018
- ↑ a b «Jellyfish blooms could be sign of ailing seas». www.eurocbc.org. Consultado em 10 de fevereiro de 2023
- ↑ Hays, G. C.; Bastian, T.; Doyle, T. K.; et al. (2011). «High activity and Lévy searches: jellyfish can search the water column like fish» (PDF). Proceedings of the Royal Society B. 279 (1728): 465–473. PMC 3234559
 . PMID 21752825. doi:10.1098/rspb.2011.0978. Cópia arquivada (PDF) em 25 de dezembro de 2012
. PMID 21752825. doi:10.1098/rspb.2011.0978. Cópia arquivada (PDF) em 25 de dezembro de 2012
- ↑ Pauly, D.; Christensen, V.; Dalsgaard, J.; et al. (1998). «Fishing down marine food webs» (PDF). Science. 279 (5352): 860–863. Bibcode:1998Sci...279..860P. PMID 9452385. doi:10.1126/science.279.5352.860. Cópia arquivada (PDF) em 10 de julho de 2012
- ↑ Richardson, A. J.; Bakun, A.; Hays, G. C.; Gibbons, M. J. (2009). «The jellyfish joyride: causes, consequences and management responses to a more gelatinous future» (PDF). Trends in Ecology & Evolution. 24 (6): 312–322. Bibcode:2009TEcoE..24..312R. PMID 19324452. doi:10.1016/j.tree.2009.01.010 [ligação inativa]
- ↑ Aksnes, D. L.; Nejstgaard, J.; Sædberg, E.; Sørnes, T. (2004). «Optical control of fish and zooplankton populations». Limnology and Oceanography. 49 (1): 233–238. Bibcode:2004LimOc..49..233A. doi:10.4319/lo.2004.49.1.0233

- ↑ Lynam, C. P.; Gibbons, M. J.; Axelsen, B. E.; et al. (2006). «Jellyfish overtake fish in a heavily fished ecosystem» (PDF). Current Biology. 16 (13): 492–493. Bibcode:2006CBio...16.R492L. PMID 16824906. doi:10.1016/j.cub.2006.06.018
 . Cópia arquivada (PDF) em 23 de março de 2011
. Cópia arquivada (PDF) em 23 de março de 2011
- ↑ Pauly, D.; Graham, W.; Libralato, S.; et al. (2009). «Jellyfish in ecosystems, online databases, and ecosystem models». Hydrobiologia. 616: 67–85. doi:10.1007/s10750-008-9583-x. Arquivado do original (PDF) em 12 de julho de 2013
- ↑ Dawson, M. N.; Sen Gupta, A.; England, M. H. (2005). «Coupled biophysical global ocean model and molecular genetic analyses identify multiple introductions of cryptogenic species». Proc. Natl. Acad. Sci. USA. 102 (34): 11968–73. Bibcode:2005PNAS..10211968D. PMC 1189321
 . PMID 16103373. doi:10.1073/pnas.0503811102
. PMID 16103373. doi:10.1073/pnas.0503811102
- ↑ Dawson, M. N. (2003). «Macro-morphological variation among cryptic species of the moon jellyfish, Aurelia (Cnidaria: Scyphozoa)». Marine Biology. 143 (2): 369–79. Bibcode:2003MarBi.143..369D. doi:10.1007/s00227-003-1070-3
- ↑ a b Rinat, Zafrir (15 de junho de 2009). «World's Most Invasive Jellyfish Spreading Along Israel Coast». Haaretz. Consultado em 13 de outubro de 2018
- ↑ Briand, Frederic; Boero, Ferdinando (2001). «Gelatinous zooplankton outbreaks - an overview on jellyfish blooms». CIESM Monographs. 14: 5–17
- ↑ Mills, C. E. (2001). «Jellyfish blooms: are populations increasing globally in response to changing ocean conditions?» (PDF). Hydrobiologia. 451 (1–3): 55–68. doi:10.1023/A:1011888006302. Cópia arquivada (PDF) em 3 de março de 2016
- ↑ «CIESM GIS». www.ciesm.org. Consultado em 10 de fevereiro de 2023
- ↑ Purcell, J.; Arai, M. (2001). Purcell, J. E; Graham, W. M; Dumont, H. J, eds. «Interactions of pelagic cnidarians and ctenophores with fish: a review». Hydrobiologia. 541: 27–44. ISBN 978-94-010-3835-5. doi:10.1007/978-94-010-0722-1
- ↑ Brodeur, Richard D.; Link, Jason S.; Smith, B.E.; et al. (2016). «Ecological and Economic Consequences of Ignoring Jellyfish: A Plea for Increased Monitoring of Ecosystems». Fisheries. 41 (11): 630–637. Bibcode:2016Fish...41..630B. doi:10.1080/03632415.2016.1232964
- ↑ Ruzicka, J.J.; Brodeur, R.D.; Emmett, R.L.; et al. (2012). «Interannual variability in the Northern California Current food web structure: changes in energy flow pathways and the role of forage fish, euphausiids, and jellyfish». Progress in Oceanography. 102: 19–41. Bibcode:2012PrOce.102...19R. doi:10.1016/j.pocean.2012.02.002
- ↑ a b Pitt, Kylie; Welsh, David; Condon, Robert (janeiro de 2009). «Influence of jellyfish blooms on carbon, nitrogen and phosphorus cycling and plankton production». Hydrobiologia. 616: 133–149. doi:10.1007/s10750-008-9584-9
- ↑ Condon, Robert H.; Duarte, Carlos M.; Pitt, Kylie A.; et al. (15 de janeiro de 2013). «Recurrent jellyfish blooms are a consequence of global oscillations». Proceedings of the National Academy of Sciences. 110 (3): 1000–1005. Bibcode:2013PNAS..110.1000C. PMC 3549082
 . PMID 23277544. doi:10.1073/pnas.1210920110
. PMID 23277544. doi:10.1073/pnas.1210920110
- ↑ Lynam, Christopher P.; Gibbons, Mark J.; Axelsen, Bjørn E.; et al. (11 de julho de 2006). «Jellyfish overtake fish in a heavily fished ecosystem». Current Biology. 16 (13): R492–493. Bibcode:2006CBio...16.R492L. PMID 16824906. doi:10.1016/j.cub.2006.06.018

- ↑ Masilamani, J; Jesudoss, K; Kanavillil, Nandakumar; et al. (10 de setembro de 2000). «Jellyfish ingress: A threat to the smooth operation of coastal power plants». Current Science. 79: 567–569
- ↑ Purcell, Jennifer E.; Uye, Shin-ichi; Lo, Wen-Tseng (22 de novembro de 2007). «Anthropogenic causes of jellyfish blooms and their direct consequences for humans: a review». Marine Ecology Progress Series. 350: 153–174. Bibcode:2007MEPS..350..153P. doi:10.3354/meps07093

- ↑ Sweetman, Andrew K.; Smith, Craig R.; Dale, Trine; Jones, Daniel O. B. (2014). «Rapid scavenging of jellyfish carcasses reveals the importance of gelatinous material to deep-sea food webs». Proceedings of the Royal Society B: Biological Sciences. 281 (1796): 20142210. PMC 4213659
 . PMID 25320167. doi:10.1098/rspb.2014.2210
. PMID 25320167. doi:10.1098/rspb.2014.2210
- ↑ Lebrato, Mario; Pahlow, Markus; Oschlies, Andreas; et al. (2011). «Depth attenuation of organic matter export associated with jelly falls» (PDF). Limnology and Oceanography. 56 (5): 1917–1928. Bibcode:2011LimOc..56.1917L. doi:10.4319/lo.2011.56.5.1917. hdl:10072/43275

- ↑ Didžiulis, Viktoras. «Invasive Alien Species Fact Sheet: Craspedacusta sowerbyi» (PDF). NOBANIS. Consultado em 16 de junho de 2016. Cópia arquivada (PDF) em 17 de maio de 2014
- ↑ Dawson, Mike N.; Martin, Laura E.; Penland, Lolita K. (2001). Jellyfish swarms, tourists, and the Christ-child. Hydrobiologia. 451. [S.l.: s.n.] pp. 131–144. ISBN 978-0-7923-6964-6. doi:10.1023/A:1011868925383
- ↑ Mills, C. E.; Hirano, Y. M. (2007). «Stauromedusae». Encyclopedia of Tidepools and Rocky Shores: 541–543
- ↑ Kondo, Yusuke; Ohtsuka, Susumu; Hirabayashi, Takeshi; et al. (2016). «Seasonal changes in infection with trematode species utilizing jellyfish as hosts: evidence of transmission to definitive host fish via medusivory». Parasite. 23: 16. PMC 4824873
 . PMID 27055563. doi:10.1051/parasite/2016016. Cópia arquivada em 4 de novembro de 2017
. PMID 27055563. doi:10.1051/parasite/2016016. Cópia arquivada em 4 de novembro de 2017
- ↑ Leung, Tommy (26 de maio de 2016). «Opechona olssoni». Blog: Parasite of the Day. Consultado em 1 de junho de 2016. Cópia arquivada em 30 de junho de 2016
- ↑ «FAOSTAT». www.fao.org. Consultado em 10 de fevereiro de 2023
- ↑ a b c d e Hsieh, Y-H. Peggy; Leong, Fui-Ming; Rudloe, Jack (2001). «Jellyfish as food». Hydrobiologia. 451 (1–3): 11–17. doi:10.1023/A:1011875720415
- ↑ George, Aleta (1 de novembro de 2012). «Jellies in the Spotlight». Endocrine News. Endocrine Society. Consultado em 16 de junho de 2018. Arquivado do original em 16 de junho de 2018
- ↑ Clinton, Morag; Ferrier, David E K; Martin, Samuel A M; Brierley, Andrew S (2 de abril de 2021). Byron, Carrie, ed. «Impacts of jellyfish on marine cage aquaculture: an overview of existing knowledge and the challenges to finfish health». International Council for the Exploration of the Sea - Oxford University Press. ICES Journal of Marine Science. 78 (5): 1557–1573. ISSN 1054-3139. doi:10.1093/icesjms/fsaa254. hdl:10023/25136

- ↑ Bosch-Belmar, Mar; Milisenda, Giacomo; Basso, Lorena; et al. (3 de setembro de 2020). «Jellyfish Impacts on Marine Aquaculture and Fisheries». Taylor & Francis. Reviews in Fisheries Science & Aquaculture. 29 (2): 242–259. ISSN 2330-8249. doi:10.1080/23308249.2020.1806201
 . hdl:10447/531140
. hdl:10447/531140
- ↑ Aristotle; William Ogle (trans.) (2018). Parts of Animals. IV. [S.l.: s.n.] p. 6. ISBN 9782378989842 [ligação inativa]
- ↑ Omori, M.; Nakano, E. (2001). «Jellyfish fisheries in southeast Asia». Hydrobiologia. 451 (1–3): 19–26. doi:10.1023/A:1011879821323
- ↑ Firth, F. E. (1969). The Encyclopedia of Marine Resources. [S.l.]: Van Nostrand Reinhold. ISBN 978-0-442-22399-1
- ↑ «How the Jelly Got Its Glow». American Museum of Natural History. Consultado em 11 de junho de 2018. Arquivado do original em 12 de junho de 2018
- ↑ a b Shimomura, O.; Johnson, F. H.; Saiga, Y. (1962). «Extraction, purification and properties of aequorin, a bioluminescent protein from the luminous hydromedusan, Aequorea». Journal of Cellular and Comparative Physiology. 59 (3): 223–39. PMID 13911999. doi:10.1002/jcp.1030590302
- ↑ Prasher, D. C.; Eckenrode, V. K.; Ward, W. W.; et al. (1992). «Primary structure of the Aequorea victoria green-fluorescent protein». Gene. 111 (2): 229–33. PMID 1347277. doi:10.1016/0378-1119(92)90691-H
- ↑ Chalfie, M.; Tu, Y.; Euskirchen, G.; et al. (fevereiro de 1994). «Green fluorescent protein as a marker for gene expression». Science. 263 (5148): 802–5. Bibcode:1994Sci...263..802C. PMID 8303295. doi:10.1126/science.8303295
- ↑ Pieribone, V.; Gruber, D. F. (2006). Aglow in the Dark: The Revolutionary Science of Biofluorescence. [S.l.]: Harvard University Press. ISBN 978-0-674-02413-7
- ↑ Herring, Peter (2002). The Biology of the Deep Ocean Oxford University Press. [S.l.]: Oxford University Press. pp. 190–191. ISBN 978-0-19-854956-7
- ↑ «US Patent for Jellyfish Tank». Cópia arquivada em 20 de fevereiro de 2015
- ↑ Richtel, Matt (14 de março de 2009). «How to Avoid Liquefying Your Jellyfish». The New York Times. Consultado em 6 de maio de 2010. Cópia arquivada em 26 de março de 2010
- ↑ McGee, Richard G.; Webster, Angela C.; Lewis, Sharon R.; Welsford, Michelle (5 de junho de 2023). «Interventions for the symptoms and signs resulting from jellyfish stings». The Cochrane Database of Systematic Reviews. 2023 (6): CD009688. ISSN 1469-493X. PMC 10240560
 . PMID 37272501. doi:10.1002/14651858.CD009688.pub3
. PMID 37272501. doi:10.1002/14651858.CD009688.pub3
- ↑ Purves, W.K.; Sadava, D.; Orians, G.H.; Heller, H.C. 1998. Life. The Science of Biology. Part 4: The Evolution of Diversity. Chapter 31
- ↑ «Jellyfish Tanks and live pet Jellyfish for sale at Jellyfish Art – Buy Jellyfish and Jellyfish tanks». jellyfishart.com. Consultado em 3 de dezembro de 2014. Arquivado do original em 2 de março de 2012
- ↑ Giaimo, Cara (13 de fevereiro de 2020). «You Didn't Touch These Jellyfish, but They Can Sting You With Tiny Grenades». The New York Times (em inglês). ISSN 0362-4331. Consultado em 27 de fevereiro de 2020
- ↑ Mahon, Andrew; Mallinson, Tom E (2020). «Lion's mane jellyfish sting». International Paramedic Practice. 10 (2): 46–48. ISSN 2052-4889. doi:10.12968/ippr.2020.10.2.46
- ↑ a b c Tucker, Abigail (julho de 2010). «The New King of the Sea». Smithsonian. 54 (4): 540–561. PMID 28752797. doi:10.1177/1363461517722869
- ↑ Adams, Julie (13 de agosto de 2016). «Box Jellyfish: Why are they so deadly?». Our Beautiful Planet. Consultado em 17 de setembro de 2016. Cópia arquivada em 10 de setembro de 2016
- ↑ a b Fenner, P.; Williamson, J.; Burnett, J.; Rifkin, J. (1993). «First aid treatment of jellyfish stings in Australia. Response to a newly differentiated species». Medical Journal of Australia. 158 (7): 498–501. PMID 8469205. doi:10.5694/j.1326-5377.1993.tb137588.x
- ↑ Currie, B.; Ho, S.; Alderslade, P. (1993). «Box-jellyfish, Coca-Cola and old wine». Medical Journal of Australia. 158 (12): 868. PMID 8100984. doi:10.5694/j.1326-5377.1993.tb137688.x
- ↑ Hartwick, R.; Callanan, V.; Williamson, J. (1980). «Disarming the box-jellyfish: nematocyst inhibition in Chironex fleckeri». Medical Journal of Australia. 1 (1): 15–20. PMID 6102347. doi:10.5694/j.1326-5377.1980.tb134566.x
- ↑ a b Perkins, R.; Morgan, S. (2004). «Poisoning, envenomation, and trauma from marine creatures». American Family Physician. 69 (4): 885–90. PMID 14989575
- ↑ Simmons, Brian J.; Griffith, Robert D.; Falto-Aizpurua, Leyre A.; Nouri, Keyvan (2015). «Moon Jellyfish Stings». JAMA Dermatology. 151 (4): 454–6. PMID 25517656. doi:10.1001/jamadermatol.2014.4644

- ↑ Baxter, E. H.; Marr, A. G. M. (maio de 1974). «Sea wasp (Chironex fleckeri) antivenene: Neutralizing potency against the venom of three other jellyfish species». Toxicon. 12 (3): 223–225. Bibcode:1974Txcn...12..223B. PMID 4156430. doi:10.1016/0041-0101(74)90062-2
- ↑ «Jellyfish Stings: Treatment and Drugs». Mayo Clinic. Mayo Foundation for Medical Education and Research. 1 de setembro de 2011. Consultado em 15 de abril de 2013. Cópia arquivada em 20 de maio de 2013
- ↑ a b «Jellyfish Gone Wild — Text-only». Nsf.gov. Consultado em 18 de outubro de 2010. Arquivado do original em 12 de julho de 2010
- ↑ «Current Event Notification Report». NRC. 22 de outubro de 2008. Consultado em 14 de julho de 2010. Cópia arquivada em 5 de junho de 2011
- ↑ Ryall, Julian (2 de novembro de 2009). «Japanese fishing trawler sunk by giant jellyfish». London: Telegraph.co.uk. Arquivado do original em 4 de novembro de 2009
Leitura complementar
- Juli Berwald (2017). Spineless: The Science of Jellyfish and the Art of Growing a Backbone. [S.l.]: Riverhead Books. ISBN 978-0-7352-1126-1
Ligações externas
- Águas-vivas e Ctenóforos – Portal Oceânico Smithsonian
- Fatos sobre Águas-vivas – Informações sobre Águas-vivas e Segurança
- "Não existe tal coisa como uma água-viva" YouTube
- "Belezas Viciosas – Águas-vivas" – um documentário sobre águas-vivas
- Elas Estão Dominando! nybooks.com, 26 de setembro de 2013. Tim Flannery






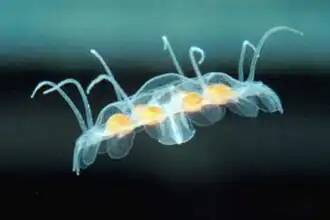

.jpg)


