Ácidos fosfóricos e fosfatos
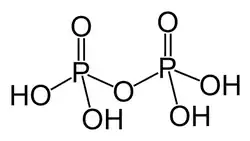
Na química, um ácido fosfórico, no sentido geral, é um oxoácido de fósforo no qual cada átomo de fósforo (P) está no estado de oxidação +5 e está ligado a quatro átomos de oxigênio (O), um deles por meio de uma ligação dupla, arranjados nos cantos de um tetraedro. Dois ou mais desses tetraedros PO
4 podem ser conectados por oxigênios compartilhados com ligações simples, formando cadeias lineares ou ramificadas, ciclos ou estruturas mais complexas. Os átomos de oxigênio com ligações simples que não são compartilhados são completados com átomos de hidrogênio acídicos. A fórmula geral de um ácido fosfórico é H
n+2-2xP
nO
3n+1-x, onde n é o número de átomos de fósforo e x é o número de ciclos fundamentais na estrutura da molécula, entre 0 e n + 2/2.

A remoção de prótons (H+
) de k grupos hidroxila –OH deixa ânions genericamente chamados fosfatos (se k = n − 2x + 2) ou hidrogenofosfatos (se k está entre 1 e n − 2x + 1), com fórmula geral [H
n-2x+2-kP
nO
3n+1-x]k-
. O ânion totalmente dissociado (k = n − 2x + 2) tem fórmula [P
nO
3n-x+1](n-2x+2)-
. O termo fosfato também é usado em química orgânica para os grupos funcionais que resultam quando um ou mais dos hidrogênios são substituídos por ligações a outros grupos.
Esses ácidos, juntamente com seus sais e ésteres, incluem alguns dos compostos de fósforo mais conhecidos, de grande importância em bioquímica, mineralogia, agricultura, farmácia, indústria química e pesquisa química.
Ácidos
Ácido fosfórico
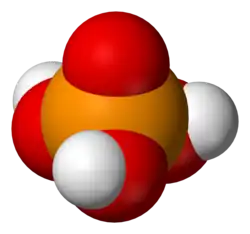
O mais simples e mais comumente encontrado dos ácidos fosfóricos é o ácido ortofosfórico, H
3PO
4. De fato, o termo ácido fosfórico frequentemente significa este composto especificamente (e esta também é a nomenclatura atual da IUPAC).[carece de fontes]
Ácidos oligofosfóricos e polifosfóricos
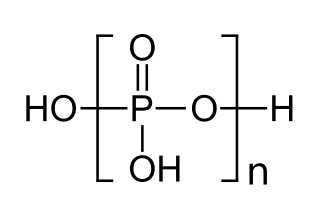
Duas ou mais moléculas de ácido ortofosfórico podem ser unidas por condensação em moléculas maiores pela eliminação de água. A condensação de poucas unidades produz os ácidos oligofosfóricos, enquanto moléculas maiores são chamadas ácidos polifosfóricos. (No entanto, a distinção entre os dois termos não é bem definida.)
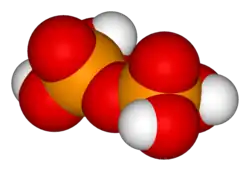
Por exemplo, os ácidos pirofosfórico, trifosfórico e tetrafosfórico podem ser obtidos pelas reações
A "espinha dorsal" de uma molécula de ácido polifosfórico é uma cadeia de átomos alternados de P e O. Cada unidade ortofosfórica extra que é condensada adiciona 1 átomo extra de H (hidrogênio), 1 átomo extra de P (fósforo) e 3 átomos extras de O (oxigênio). A fórmula geral de um ácido polifosfórico é H
n+2P
nO
3n+1 ou HO[–P(O)(OH)–O–]
nH.
Os ácidos polifosfóricos são usados em síntese orgânica para cicliizaçãos e acilaçãos; uma alternativa é o reagente de Eaton.[1][2][3]
Ácido metafosfórico
O ácido metafosfórico (HPO
3) é um sólido incolor, vítreo, delicuescente, com densidade de 2,2 a 2,5 g/cc, que sublima ao aquecer. É solúvel em etanol.[4]
Ácidos fosfóricos cíclicos
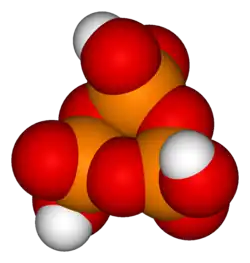
Unidades de ácido fosfórico podem ser ligadas em anéis (estruturas cíclicas). O composto mais simples desse tipo é o ácido trimetafosfórico ou ácido ciclo-trifosfórico, com fórmula H
3P
3O
9. Sua estrutura é mostrada na ilustração. Como as extremidades são condensadas, sua fórmula tem uma H
2O (água) a menos que o ácido tripolifosfórico.
A fórmula geral de um ácido fosfórico é H
n-2x+2P
nO
3n-x+1, onde n é o número de átomos de fósforo e x é o número de ciclos fundamentais na estrutura da molécula; isto é, o número mínimo de ligações que teriam de ser quebradas para eliminar todos os ciclos.
-
-
-
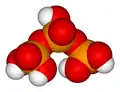 Ácido tripolifosfórico
Ácido tripolifosfórico
H
5P
3O
10 -
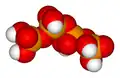 Ácido tetrapolifosfórico
Ácido tetrapolifosfórico
H
6P
4O
13 -
 Ácido trimetafosfórico
Ácido trimetafosfórico
H
3P
3O
9 -
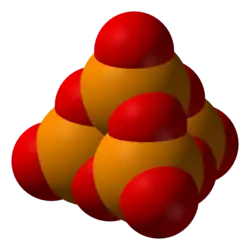
O caso limite de condensação interna, onde todos os átomos de oxigênio são compartilhados e não há átomos de hidrogênio (x = n+2/2) é um anidrido P
2nO
5n, pentóxido de fósforo P
4O
10.
Fosfatos
A remoção dos átomos de hidrogênio como prótons H+
transforma um ácido fosfórico em um ânion fosfato. A remoção parcial produz vários ânions hidrogenofosfato.
Ortofosfato
Os ânions do ácido ortofosfórico H
3PO
4 são ortofosfato (comumente chamado simplesmente "fosfato") PO3–
4, monohidrogenofosfato HPO2–
4, e dihidrogenofosfato H
2PO–
4.
Oligofosfatos e polifosfatos lineares
A dissociação do ácido pirofosfórico H
4P
2O
7 gera quatro ânions, [H
4-kP
2O
7]k-
, onde a carga k varia de 1 a 4. O último é pirofosfato [P
2O
7]4–. Os pirofosfatos são principalmente solúveis em água.
Da mesma forma, o ácido tripolifosfórico H
5P
3O
10 produz pelo menos cinco ânions [H
5-kP
3O
10]k-
, onde k varia de 1 a 5, incluindo tripolifosfato [P
3O
10]5–. O ácido tetrapolifosfórico H
6P
4O
13 produz pelo menos seis ânions, incluindo tetrapolifosfato [P
4O
13]6–, e assim por diante. Note que cada unidade fosfórica extra adiciona um átomo extra de P, três átomos extras de O e ou um átomo extra de hidrogênio ou uma carga negativa extra.
Ácidos polifosfóricos ramificados dão ânions polifosfato ramificados semelhantes. O exemplo mais simples disso é o fosfato triposfono [OP(OPO
3)
3]9– e suas versões parcialmente dissociadas.
A fórmula geral para tais ânions polifosfato (não cíclicos), lineares ou ramificados, é [H
n+2-kP
nO
3n+1]k-
, onde a carga k pode variar de 1 a n + 2. Geralmente em uma solução aquosa, o grau ou percentagem de dissociação depende do pH da solução.
Polifosfatos cíclicos
Sais ou ésteres de ácidos polifosfóricos cíclicos são frequentemente chamados "metafosfatos". O que são comumente chamados trimetafosfatos na verdade têm uma mistura de tamanhos de anel. Uma fórmula geral para tais compostos cíclicos é [HPO
3]
x onde x = número de unidades fosfóricas na molécula.
Quando os ácidos metafosfóricos perdem seus hidrogênios como H+
, ânions cíclicos chamados metafosfatos são formados. Um exemplo de um composto com tal ânion é o hexametafosfato de sódio (Na
6P
6O
18), usado como sequestrante e aditivo alimentar.
Propriedades químicas
Solubilidade
Essa série de ácidos fosfóricos é geralmente solúvel em água considerando a polaridade das moléculas. Fosfatos de amônio e alcalino também são bastante solúveis em água. Os sals de alcalinoterroso começam a se tornar menos solúveis e sais fosfato de vários outros metais são ainda menos solúveis.
Hidrólise e condensação
Em soluções aquosas (soluções de água), a água gradualmente (ao longo de horas) hidrolisa polifosfatos em fosfatos menores e finalmente em orto-fosfato, dado água suficiente. Temperatura mais alta ou condições ácidas podem acelerar consideravelmente as reações de hidrólise.[5] Inversamente, ácidos polifosfóricos ou polifosfatos são frequentemente formados pela desidratação de uma solução de ácido fosfórico; em outras palavras, removendo água dela, frequentemente por aquecimento e evaporação da água.
Usos
Compostos de orto-, piro- e tripolifosfato, como tripolifosfato de sódio, têm sido comumente usados em formulações de detergentes (i. e. limpadores). Às vezes pirofosfato, tripolifosfato, tetrapolifosfato, etc. são chamados difosfato, trifosfato, tetrafosfato, etc., especialmente quando fazem parte de ésteres fosfato em bioquímica. Eles também são usados para controle de incrustações e corrosão por fornecedores de água potável.[6] Como inibidor de corrosão, polifosfatos funcionam formando uma película protetora na superfície interna de tubos.[7]
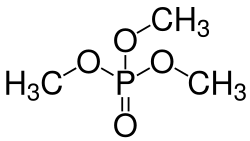
Ésteres fosfato
Os grupos –OH em ácidos fosfóricos também podem condensar com os grupos hidroxila de álcools para formar ésteres fosfato. Como o ácido ortofosfórico tem três grupos –OH, ele pode esterificar com uma, duas ou três moléculas de álcool para formar um mono-, di- ou triéster. Veja a imagem da estrutura geral de um orto- (ou mono-) fosfato éster abaixo à esquerda, onde qualquer dos grupos R pode ser um hidrogênio ou um radical orgânico. Di- e tripolifosfato (ou tri-) ésteres, etc. também são possíveis. Quaisquer grupos –OH nos fosfatos nessas moléculas de éster podem perder íons H+
para formar ânions, novamente dependendo do pH em uma solução. Na bioquímica de organismos vivos, há muitos tipos de compostos (mono)fosfato, difosfato e trifosfato (essencialmente ésteres), muitos dos quais desempenham um papel significativo no metabolismo, como adenosina difosfato (ADP) e trifosfato (ATP).
Ver também
- Adenosina monofosfato
- Adenosina difosfato
- Adenosina trifosfato
- Adenosina tetrafosfato
- Nucleosídeo trifosfato
- Organofosfato
- Ácido fosfônico
- Fosforamidato
- Ribonucleosídeo monofosfato
- Superfosfato
Referências
- ↑ Harwood, Laurence M.; Hodgkinson, Leslie C.; Sutherland, James K.; Towers, Patrick (1984). «Synthesis of anthracyclinones. Part 1. Regioselective alkylation of 5-hydroxyquinizarin». Canadian Journal of Chemistry. 62 (10): 1922–1925. doi:10.1139/v84-329

- ↑ Nakazawa, Koichi; Matsuura, Shin; Kusuda, Kosuke (1954). «Studies on the Application of Polyphosphoric Acid as a Condensing Agent. II». Yakugaku Zasshi. 74 (5): 495–497. doi:10.1248/yakushi1947.74.5_495

- ↑ Eaton, P. E.; Carlson, G. R.; Lee, J. T. (1973). «Phosphorus pentoxide-methanesulfonic acid. Convenient alternative to polyphosphoric acid». J. Org. Chem. 38 (23). 4071 páginas. doi:10.1021/jo00987a028
- ↑ CRC Handbook of Chemistry and Physics 49 ed. [S.l.]: Chemical Rubber Co. 1968. p. B-226
- ↑ «Phosphoric acid and phosphates». Encyclopedia of Chemical Technology. New York: The Interscience Encyclopedia, Inc. 1953. p. 421
- ↑ «Polyphosphates for scale and corrosion control». Tramfloc, INC. Janeiro de 2009. Consultado em 23 de dezembro de 2010
- ↑ «Ortho-Polyphosphate Corrosion Inhibitors» (PDF). Government Engineering:The Journal for Public Infrastructure (Setembro–Outubro, 2006): 48–49. Consultado em 23 de dezembro de 2010
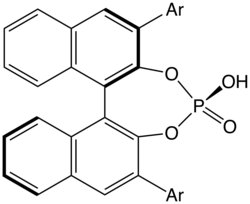
- ↑ Parmar, Dixit; Sugiono, Erli; Raja, Sadiya; Rueping, Magnus (2014). «Complete Field Guide to Asymmetric BINOL-Phosphate Derived Brønsted Acid and Metal Catalysis: History and Classification by Mode of Activation; Brønsted Acidity, Hydrogen Bonding, Ion Pairing, and Metal Phosphates». Chemical Reviews. 114 (18): 9047–9153. PMID 25203602. doi:10.1021/cr5001496

Leitura adicional
- Schröder HC, Kurz L, Muller WE, Lorenz B (Março de 2000). «Polyphosphate in bone» (PDF). Biochemistry (Moscow). 65 (3): 296–303. PMID 10739471. Arquivado do original (PDF) em 25 de agosto de 2011