Ácido beta-Schäffer
Ácido beta-Schäffer
| |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||
| Nomes | |||||||||||||
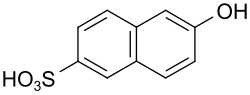
| Nome IUPAC | Ácido 6-hidroxinaftaleno-2-sulfônico | ||||||||||||
| Outros nomes | Ácido de Schäffer, Ácido β de Schaeffer, Ácido 2-naftol-6-sulfônico | ||||||||||||
| |||||||||||||
| |||||||||||||
| |||||||||||||
| |||||||||||||
| Página de dados suplementares | |||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||
Ácido beta-Schäffer, ácido β de Schaeffer, ácido 2-hidroxinaftaleno-6-sulfônico, ácido 6-hidróxi-2-naftalenossulfônico, ácido 2-naftol-6-sulfônico, ou ácido 6-hidroxinaftalen-2-sulfônico é o composto orgânico de fórmula química C10H8O4S, massa molecular 224,23. É um dos ácidos de letras, podendo ser entendido como o ácido sulfônico de posição 6 do 2-naftol, ou o naftol de posição 2 do ácido 2-naftaleno-sulfônico. É classificado com o CBNumber CB7301210. Possui ponto de fusão de 167 °C (anidro) ou 125 °C (monohidratado).[1]
É uma substância irritante. É obtido pela sulfonação por ácido sulfúrico concentrado sobre o 2-naftol. Apresenta-se como escamas, com ponto de fusão de 125 °C (monohidrato), sendo muito solúvel em água e álcool, praticamente insolúvel em éter.[2][3]
A fluorescência pode ser utilizada para indicar a pureza dos ácidos naftalenossulfônicos e para diferenciar e reconhecer os diferentes isômeros. O sal de sódio do ácido beta-Schäffer apresenta, em solução aquosa, uma leve fluorescência entre as cores violeta e azul.[4]
O composto é produzido após duas sulfonações do 2-Naftol: a primeira sulfonação ocorre na posição 1[Nota 1] e a segunda sulfonação na posição 6.[Nota 2] Em seguida é feita uma dessulfonação, que ocorre na posição 1.[5]
Este ácido é utilizado na síntese do corante Vermelho allura AC.[5][6] Como primeiro passo, o ácido 4-amino-5-metoxi-2-metilbenzenossulfônico reage com nitrito de sódio (NaNO2), gerando um sal de diazônio. O sal de diazônio reage com o ácido de Schäffer, no carbono 1 (considerando a hidroxila no carbono 2), produzindo o corante.[6][Nota 3]
A reação de acoplamento do ácido 4-aminobenzenossulfônico diazotado com o ácido 6-hidroxinaftaleno-2-sulfônico produz o corante alimentar Food Yellow No. 5 (Amarelo crepúsculo).[7]
-
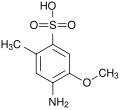 Ácido 4-amino-5-metoxi-2-metilbenzenossulfônico
Ácido 4-amino-5-metoxi-2-metilbenzenossulfônico -
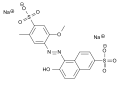 Vermelho allura AC (imagem errada)
Vermelho allura AC (imagem errada) -
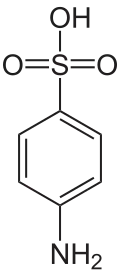 Ácido 4-aminobenzenossulfônico (ácido sulfanílico)
Ácido 4-aminobenzenossulfônico (ácido sulfanílico) -
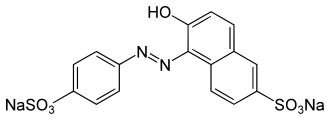 Amarelo crepúsculo
Amarelo crepúsculo
Notas e referências
Notas
- ↑ Produzindo o ácido 2-hidroxinaftaleno-1-sulfônico.
- ↑ O ácido intermediário é o ácido 2-hidroxi-naftaleno-1,6-dissulfônico.
- ↑ A imagem do corante Vermelho allura AC está errada em algumas fontes, com o acoplamento sendo representado incorretamente no carbono 3.
Referências
- ↑ «6-Hydroxynaphthalene-2-sulphonic acid». ChemicalBook. Consultado em 24 de janeiro de 2026
- ↑ «2-Naphthol-6-sulfonic acid». ChemSpider. Consultado em 24 de janeiro de 2026
- ↑ «2-Naphthol-6-sulfonic Acid». DrugFuture. Consultado em 24 de janeiro de 2026
- ↑ Hans Eduard Fierz-David; Louis Blangey (1942). Fundamental Processes of Dye Chemistry. [S.l.]: Interscience Publishers. p. 48
- ↑ a b Reinhard Brückner (2014). «Reaktionsmechanismen Organische Reaktionen, Stereochemie, Moderne Synthesemethoden». Springer-Verlag: 210. ISBN 978-3-662-45684-2
- ↑ a b Paula Bruice (2004). Organic Chemistry 4ª ed. [S.l.]: Pearson Education
- ↑ «Food Yellow No. 5». Japan Food Chemical Research Foundation. Consultado em 23 de agosto de 2013