Dímero
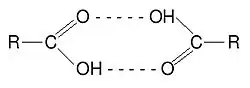
Um dímero é uma entidade química que consiste em duas moléculas (unidades monoméricas) estruturalmente similares unidas entre si por ligações fortes ou fracas, covalentes ou intermoleculares. Às vezes as duas moléculas são idênticas (homodímero) e outras são distintas (heterodímero). A união das duas moléculas para formar o dímero denomina-se dimerização[1], e o inverso da dimerização geralmente se chama dissociação. Analogamente, fala-se de heterodimerização e homodimerização.
- Em química, um dímero (composto por duas partes) é uma molécula composta por duas unidades similares ou monômeros unidos. É um caso especial de polímero. Os dímeros mais comuns são do tipo açúcares; sacarose, por exemplo, é um dímero de uma molécula de glucose e uma molécula de frutose.
Um exemplo é o diciclopentadieno, o qual é um o dímero de ciclopentadieno, relacionando-se a química de haletos, envolvendo ligações de halogênios.
- Em física, um dímero é um termo aplicado à interação intermolecular de duas moléculas idênticas mais próximas e juntas que outras. Não há ligações covalentes entre as moléculas que constituem um dímero físico. O ácido acético é um exemplo onde as ligações de hidrogênio proporcionam a interação.
- Em biologia e bioquímica, um dímero é uma proteína composta por duas subunidades. Em um homodímero, as duas subunidades são idênticas, e em um heterodímero são diferentes.
Em bioquímica
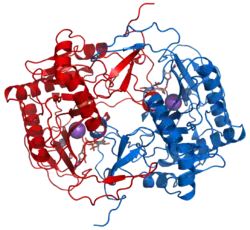
Em bioquímica, um dímero é um complexo macromolecular formado por duas moléculas, geralmente proteínas ou ácidos nucleicos, normalmente unidos de forma não covalente. As clorofilas do centro de reação dos fotossistemas formam também um dímero.
Proteínas dímeras
Nas proteínas os dímeros são um tipo de estrutura quaternária. Os homodímeros são formados por duas moléculas idênticas; um exemplo é a ciclooxigenase (COX). Os heterodímeros são formados por duas moléculas diferentes; um exemplo é a tubulina, formada por monómeros de alfa e beta tubulina.
A maioria dos dímeros em bioquímica não estão conectados por ligações covalentes. Um exemplo de heterodímero unido de forma não covalente é a enzima transcriptase reversa, que é composta por duas cadeias polipeptídicas diferentes.[2] Os dímeros unidos covalentemente (por pontes dissulfeto) são mais raros; um exemplo é a proteína homodímera NEMO.[3]
Algumas proteínas contêm domínios especializados que facilitam a dimerização, chamados domínios de dimerização. Um estudo encontrou que as interfaces pelas quais se unem os homodímeros e heterodímeros são algo diferentes. Nos homodímeros há no total mais resíduos de aminoácidos e pontes de hidrogénio, embora a densidade de pontes de hidrogénio por resíduo seja maior nos heterodímeros. Nas interfaces de heterodímeros há mais resíduos carregados e hidrofílicos e nos homodímeros predominam os hidrofóbicos.[4]
A dimerização ou a dissociação podem fazer mudar o estado funcional da proteína de ativo a inativo ou vice-versa. Por exemplo a glicogénio fosforilase existe como monómero inativo e só é ativada quando se dimeriza.[5]
Dímeros de pirimidinas
Os dímeros de pirimidinas formam-se por reação fotoquímica a partir de bases nitrogenadas pirimidínicas do ADN. Esta reação causa mutações no ADN, que podem ser carcinógenas e originar cancro de pele.
Em química
Dímeros não covalentes
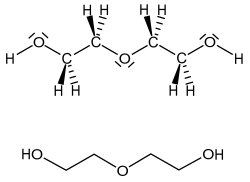
Os ácidos carboxílicos formam dímeros por formação de pontes de hidrogénio entre o hidrogénio ácido e o oxigénio carbonílico em condições anidras. Por exemplo, o ácido acético forma um dímero em fase de gás, no qual as unidades monoméricas se unem por pontes de hidrogénio. Em condições especiais, a maioria das moléculas que contêm grupos OH formam dímeros (por exemplo o dímero de água).
O borano ("BH3") aparece como o dímero diborano (B2H6), devido à alta acidez de Lewis do centro de boro.
Os excímeros e exciplexos são estruturas excitadas de curta duração. Por exemplo, os gases nobres não formam dímeros estáveis, mas formam os excímeros Ar2*, Kr2* e Xe2* em condições de altas pressões e estimulação elétrica.
Dímeros covalentes
Os dímeros moleculares formam-se frequentemente pela reação de dois compostos idênticos, como por exemplo: 2A → A-A. Neste exemplo, o monómero "A" diz-se que se dimeriza para dar o dímero "A-A". Um exemplo real são os diaminocarbenos, que se dimerizam dando um tetraaminoetileno:
- 2 C(NR2)2 → (R2N)2C=C(NR2)2
Os carbenos são muito reativos e formam ligações facilmente.
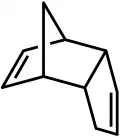
O diciclopentadieno é um dímero assimétrico de duas moléculas de ciclopentadieno que reagiram pela reação de Diels-Alder para dar o produto. Submetido a calor sofre a reação inversa (retro-Diels-Alder) para dar os dois monómeros iguais:
- C10H12 → 2 C5H6
Muitos elementos não metálicos aparecem como moléculas diatómicas e às vezes fala-se delas denominando-as dímeros: hidrogénio, nitrogénio, oxigénio, os halogéneos (flúor, cloro, bromo e iodo). O mercúrio aparece como mercúrio(I) catião (Hg2+), formalmente um heterodímero.
Química de polímeros
No contexto da química de polímeros, "dímero" também se refere ao grau de polimerização 2, em relação à estequiometria das reações de condensação. Um exemplo seriam os dissacarídeos, formados por dois monossacarídeos. Por exemplo, a celobiose é um dímero de glicose, embora na reação se produza água:
- 2C6H12O6 → C12H22O11 + H2O
Aqui, o dímero tem uma estequiometria diferente da do par de monómeros.
Ver também
Ligações externas
- «Reverse transcriptase» (em inglês)
- «Homo and hetero dimeric proteins» (em inglês)
Referências
- ↑ «IUPAC "Gold Book" definition». Consultado em 30 de abril de 2009
- ↑ Sluis-Cremer N, Hamamouch N, San Félix A, Velazquez S, Balzarini J, Camarasa MJ (2006). «Structure-activity relationships of [2',5'-bis-O-(tert-butyldimethylsilyl)-beta-D-ribofuranosyl]- 3'-spiro-5' '-(4' '-amino-1' ',2' '-oxathiole-2' ',2' '-dioxide)thymine derivatives as inhibitors of HIV-1 reverse transcriptase dimerization». J. Med. Chem. 49 (16): 4834–41. PMID 16884295. doi:10.1021/jm0604575
- ↑ Herscovitch M, Comb W, Ennis T, Coleman K, Yong S, Armstead B, Kalaitzidis D, Chandani S, Gilmore TD (2008). «Intermolecular disulfide bond formation in the NEMO dimer requires Cys54 and Cys347». Biochem. Biophys. Res. Commun. 367 (1): 103–8. PMC 2277332
 . PMID 18164680. doi:10.1016/j.bbrc.2007.12.123
. PMID 18164680. doi:10.1016/j.bbrc.2007.12.123
- ↑ Cui Zhanhua, Jacob Gah-Kok Gan, Li lei, Meena Kishore Sakharkar, and Pandjassarame Kangueane. Protein subunit interfaces: heterodimers versus homodimers Bioinformation. 2005; 1(2): 28–39. Published online 2005 August 11. PMCID: PMC1891636 [1]
- ↑ Browner MF, Fletterick RJ (1992). «Phosphorylase: a biological transducer». Trends in Biochemical Science. 17 (2): 66–71. PMID 1566331. doi:10.1016/0968-0004(92)90504-3