Bicarbonato de sódio
Bicarbonato de sódio
| |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||
| |||||||||||||||||
 | |||||||||||||||||
| |||||||||||||||||
| Nomes | |||||||||||||||||
| Nome IUPAC | hidrogenocarbonato de sodio | ||||||||||||||||
| Outros nomes | bicarbonato de sódio | ||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| Página de dados suplementares | |||||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||||

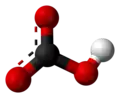
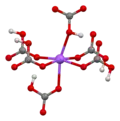
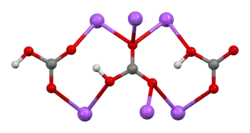
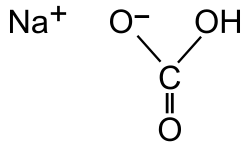
Bicarbonato de sódio (IUPAC: hidrogenocarbonato de sódio[1]) é um composto químico com a fórmula NaHCO3. É um sal composto de um cátion sódio (Na+) e um ânion bicarbonato (HCO3−). O bicarbonato de sódio é um sólido branco cristalino, mas geralmente aparece como um pó fino. Tem um sabor ligeiramente salgado e alcalino, semelhante ao do carbonato de sódio. A forma mineral natural é a nahcolita, embora seja mais comumente encontrada como um componente do mineral trona.[2]
O prefixo bi- em "bicarbonato" vem de um sistema de nomenclatura desatualizado anterior ao conhecimento molecular. Ele é baseado na observação de que há duas vezes mais carbonato (CO32-) por sódio no bicarbonato de sódio (NaHCO3) do que há no carbonato de sódio (Na2CO3).[3] As fórmulas químicas modernas desses compostos agora expressam suas composições químicas precisas que eram desconhecidas quando o nome bicarbonato de potássio foi cunhado.
Aplicações
Usa-se como antiácido para tratar a acidez do estômago porque tem o poder de neutralizar os excessos do ácido clorídrico do suco gástrico, devido ao facto de ser uma substância ligeiramente alcalina (ph=9). Em algumas formulações farmacêuticas, é misturado aos ácidos cítrico e tartárico, ambos sólidos.[4]
Devido à sua capacidade de libertar dióxido de carbono gasoso (CO2), o bicarbonato de sódio também é muito usado nas receitas de culinária como agente levedante ("fermentos químicos"), no crescimento da massa de pães, bolos e biscoitos durante o cozimento no forno, em especial quando misturado ao ácido tartárico, e na produção de bebidas gasosas (refrigerantes).
Além do uso farmacêutico e culinário, o bicarbonato de sódio também é um ótimo auxiliar na limpeza de ambientes e de roupas. Tem ação anti-mancha e anti-mofo e elimina o mau cheiro.
Outras utilizações do bicarbonato de sódio são como reagente de laboratório, na eletrodeposição de ouro e platina, em curtumes, no tratamento da lã e da seda, na nutrição de animais, na cerâmica e na preservação da manteiga e da madeira e é um dos componentes dos talcos e desodorantes. A sua forma anidra usa-se para absorver umidade e odores.
É utilizado na fabricação de extintores de incêndio com produção de espuma. No interior destes extintores encontra-se NaHCO3 sólido, em compartimento separado de uma solução de ácido sulfúrico (H2SO4). Quando se vira o extintor, o que causa seu acionamento, o NaHCO3 e o H2SO4 se misturam e reagem, com liberação de dióxido de carbono (CO2), o que gera pressão dentro do vaso e a ejeção do dióxido de carbono, com produção de espuma. Estes extintores são inadequados contra chamas em equipamentos e instalações elétricas, pois seu meio aquoso e salino conduz corrente elétrica, causando curtos-circuitos. Também é muito utilizado em tratamento de água de piscinas na elevação da Alcalinidade Total, imprescindível no tratamento adequado da mesma, sendo o primeiro parâmetro a ser corrigido.
As reações envolvidas são:
- 2 NaHCO3 + H2SO4 → Na2SO4 + 2 H2CO3
- H2CO3 → H2O + CO2(g)
É um dos componentes da droga chamada crack, onde entra como aditivo à pasta de cocaína. Utiliza-se no tratamento radiológico de contaminados por urânio.
Também se utiliza nas fraudes na produção de leite, pois tem capacidade de alcalizar o leite quando se inicia o processo de deterioração.[5]
Reações químicas
Quando o bicarbonato de sódio é misturado com um ácido, liberta dióxido de carbono e água. Exemplos:
Bicarbonato de sódio reage com bases tais como o hidróxido de sódio para formar carbonatos:
- NaHCO3 + NaOH → Na2CO3 + H2O
Quando aquecido, ao atingir a temperatura de 80 °C, decompõe-se de acordo com a reação:[6]
- 2 NaHCO3 → Na2CO3 + H2O + CO2
Ver também
Referências
- ↑ Nomenclature of Inorganic Chemistry IUPAC Recommendations 2005 (PDF), IUPAC, p. 137, cópia arquivada (PDF) em 18 de maio de 2017
- ↑ Gärtner, Robert S.; Witkamp, Geert-Jan (agosto de 2007). «Mixed solvent reactive recrystallization of trona (sodium sesqui-carbonate) into soda (sodium carbonate anhydrate)». Hydrometallurgy (em inglês). 88 (1–4): 75–91. Bibcode:2007HydMe..88...75G. doi:10.1016/j.hydromet.2007.03.006
- ↑ Wollaston, WH (janeiro de 1814). «I. A Synoptic scale of chemical equivalents». Philosophical Transactions of the Royal Society of London. 104: 1–22. doi:10.1098/rstl.1814.0001
- ↑ “bicarbonato de sodio“ Revisado.
- ↑ Julio Cezar Foschini Lisbôa e Monique Bossolani, EXPERIÊNCIAS LÁCTEAS (1997), Disponível em: http://qnesc.sbq.org.br/online/qnesc06/exper1.pdf
- ↑ «The Many Practical Uses of Baking Soda in the Kitchen». About.com Food. Consultado em 22 de janeiro de 2017