Modelo atômico de Rutherford
O modelo atômico (português brasileiro) ou modelo atómico (português europeu) de Rutherford (também conhecido como modelo planetário do átomo) é um modelo atômico proposto pelo físico Ernest Rutherford que descreve o átomo como um núcleo central denso positivo rodeado de elétrons.[1]
Experimento base do modelo
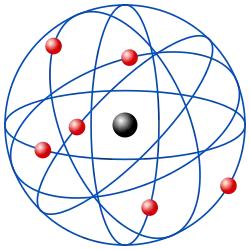
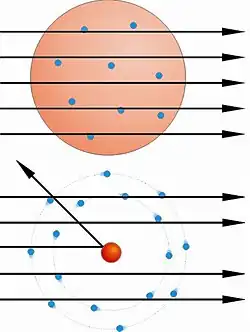
Para montar sua teoria, Rutherford analisou os resultados do experimento de Geiger-Marsden. Nesta experiência, utilizando uma fonte radioativa para emitir partículas alfa, um contador Geiger, e uma fina lâmina de ouro, Geiger e Mardsen mediram o número de partículas alfa que atravessaram esta folha. Porém, eles perceberam que, embora muitas das partículas atravessassem a folha, um número muito pequeno ddelas eram refletidas ou eram desviadas por esta folha.
Com base nisto, Rutherford elaborou o modelo em 1911, afirmando que o modelo vigente até então, conhecido como "pudim de passas", feito por J. J. Thomson, estava incorreto. Ele afirmou, com seu experimento, que o átomo não era apenas uma esfera maciça de carga elétrica positiva incrustada com elétrons, como dizia J. J. Thomson. O átomo teria na verdade um núcleo de carga elétrica positiva de tamanho muito pequeno em relação ao seu tamanho total, sendo este o núcleo, que conteria praticamente toda a massa do átomo e seria rodeado por elétrons de carga elétrica negativa.[2]
Tamanho do átomo
Analisando os resultados de números de partículas que passavam ou eram refletidas pela camada de ouro, Rutherford conseguiu inclusive calcular a provável proporção de tamanho entre núcleo e átomo, que segundo ele seria 1/100 000 a 1/1 000 000. É de costume comparar o tamanho do núcleo do átomo de Rutherford em relação ao seu todo, com uma formiga no meio de um campo de futebol, sendo a formiga o núcleo e o campo o tamanho total do átomo.[1]
Falha no modelo de Rutherford
A falha do modelo de Rutherford é mostrada pela teoria do electromagnetismo, de que toda partícula com carga elétrica submetida a uma aceleração origina a emissão de uma onda electromagnética. O elétron em seu movimento orbital está submetido a uma aceleração centrípeta e, portanto, emitirá energia na forma de onda eletromagnética. Essa emissão, pelo Princípio da conservação da energia, faria com que o elétron perdesse energia cinética e potencial, caindo progressivamente sobre o núcleo, fato que não ocorre na prática. A falha foi corrigida pelo modelo atômico de Bohr, de seu aluno e colega de trabalho Niels Bohr, que dizia que considerava a ideia de um modelo atômico planetário bonita demais para estar errada. Assim, com o auxílio das descrições quânticas da radiação eletromagnética propostas por Albert Einstein e Max Planck, conseguiu completar a teoria de Rutherford, ficando assim conhecida como modelo atômico-molecular de Rutherford-Bohr.
Ver também
- Modelo atômico de Thomson
- Modelo atômico de Bohr
- Modelo atômico de Dalton
Referências
- 1 2 «Modelo Atômico de Rutherford». Consultado em 20 de agosto de 2014. Arquivado do original em 24 de setembro de 2015
- ↑ «A experiência de Rutheford | Átomo». penta3.ufrgs.br. Consultado em 14 de abril de 2026
Bibliografia
- María José T. Molina.. Mecánica Global e Astrofísica: Teoria da Equivalência Global , Editora Molwick - 268 páginas. ISBN 8-415-36565-9