Efusão (química)
| Mecânica do contínuo |
|---|
 |
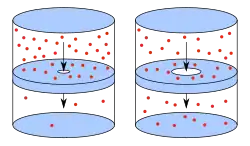
Em física e química, efusão é o processo no qual um gás escapa de um recipiente através de um orifício de diâmetro consideravelmente menor que o livre caminho médio das moléculas.[1] Tal orifício é frequentemente descrito como um pequeno furo e o escape do gás ocorre devido à diferença de pressão entre o recipiente e o exterior.
Sob essas condições, essencialmente todas as moléculas que chegam ao orifício continuam e passam através dele, já que as colisões entre moléculas na região do orifício são desprezíveis. Por outro lado, quando o diâmetro é maior que o livre caminho médio do gás, o fluxo obedece à Lei de fluxo de Sampson.
Na terminologia médica, uma efusão refere-se ao acúmulo de fluido em um espaço anatômico, geralmente sem loculação. Exemplos específicos incluem subdural, mastoide, pericárdico e efusões pleurais.
Etimologia
A palavra efusão deriva da palavra latina "effundo", que significa "derramar", "verter", "emanar", "expressar", "prodigalizar", "desperdiçar".
No vácuo
A efusão de um recipiente em equilíbrio para o vácuo externo pode ser calculada com base na teoria cinética.[2] O número de colisões atômicas ou moleculares com uma parede de um recipiente por unidade de área por unidade de tempo (taxa de impacto) é dado por: assumindo que o livre caminho médio é muito maior que o diâmetro do pequeno orifício e o gás pode ser tratado como um gás ideal.[3]
Se uma pequena área no recipiente é perfurada para se tornar um pequeno orifício, a taxa de fluxo de efusão será onde é a massa molar, é a constante de Avogadro, e é a constante universal dos gases.
A velocidade média das partículas efundidas é
Combinada com a taxa de fluxo de efusão, a força de recuo/empuxo no próprio sistema é
Um exemplo é a força de recuo em um balão com um pequeno furo voando no vácuo.
Medidas de taxa de fluxo
De acordo com a teoria cinética dos gases, a energia cinética para um gás a uma temperatura é
onde é a massa de uma molécula, é a velocidade quadrática média das moléculas, e é a constante de Boltzmann. A velocidade molecular média pode ser calculada a partir da distribuição de velocidades de Maxwell como (ou, equivalentemente, ). A taxa na qual um gás de massa molar efunde (tipicamente expressa como o número de moléculas passando pelo orifício por segundo) é então[4]
Aqui é a diferença de pressão do gás através da barreira, é a área do orifício, é a constante de Avogadro, é a constante dos gases e é a temperatura absoluta. Assumindo que a diferença de pressão entre os dois lados da barreira é muito menor que , a pressão absoluta média no sistema (isto é (i.e. )), é possível expressar o fluxo de efusão como uma taxa de fluxo volumétrico da seguinte forma:
ou
onde é a taxa de fluxo volumétrico do gás, é a pressão média em ambos os lados do orifício, e é o diâmetro do orifício.
Efeito do peso molecular
A pressão e temperatura constantes, a velocidade quadrática média e, portanto, a taxa de efusão é inversamente proporcional à raiz quadrada do peso molecular. Gases com menor peso molecular efundem mais rapidamente que gases com maior peso molecular, de modo que o número de moléculas mais leves passando pelo orifício por unidade de tempo é maior.
Lei de Graham
O químico escocês Thomas Graham (1805–1869) descobriu experimentalmente que a taxa de efusão de um gás é inversamente proporcional à raiz quadrada da massa de suas partículas.[5] Em outras palavras, a razão entre as taxas de efusão de dois gases à mesma temperatura e pressão é dada pela razão inversa das raízes quadradas das massas das partículas de gás.
onde e representam as massas molares dos gases. Esta equação é conhecida como Lei de efusão de Graham.
A taxa de efusão para um gás depende diretamente da velocidade média de suas partículas. Assim, quanto mais rápido as partículas de gás estiverem se movendo, mais provável é que passem pelo orifício de efusão.
Célula de Knudsen
A Célula de Knudsen é usada para medir a pressão de vapor de um sólido com pressão de vapor muito baixa. Tal sólido forma um vapor a baixa pressão por sublimação. O vapor lentamente efunde através de um pequeno orifício, e a perda de massa é proporcional à pressão de vapor e pode ser usada para determinar esta pressão.[4] O calor de sublimação também pode ser determinado medindo a pressão de vapor em função da temperatura, usando a relação de Clausius–Clapeyron.[6]
Referências
- ↑ K.J. Laidler and J.H. Meiser, Physical Chemistry, Benjamin/Cummings 1982, p.18. ISBN 0-8053-5682-7
- ↑ «5.62 Physical Chemistry II» (PDF). MIT OpenCourseWare
- ↑ «Low-Pressure Effusion of Gases». www.chem.hope.edu. Hope College. Consultado em 6 abril 2021
- ↑ a b Peter Atkins and Julio de Paula, Physical Chemistry (8th ed., W.H.Freeman 2006) p.756 ISBN 0-7167-8759-8
- ↑ Zumdahl, Steven S. (2008). Chemical Principles. Boston: Houghton Mifflin Harcourt Publishing Company. p. 164. ISBN 978-0-547-19626-8
- ↑ Drago, R.S. Physical Methods in Chemistry (W.B.Saunders 1977) p.563 ISBN 0-7216-3184-3