Plasmina
| plasmin | |||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Identificadores | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Nomes alternativos | |||||||||||||||||||||||||||||||||||||||||||||||||||
| IDs externos | GeneCards: | ||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Wikidata | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
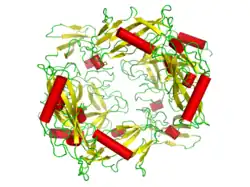
Plasmina é uma importante enzima presente no sangue que degrada muitas proteínas do plasma sanguíneo, mais notavelmente os coágulos de fibrina. A degradação da fibrina é chamada de fibrinólise.
Ela é uma protease serina que é liberada como plasminogênio na circulação e ativada pelo ativador de plasminogênio tecidual (AP-t), ativador de plasminogênio uroquinase (uPA), trombina, fibrina e fator XII. É inativada pela antiplasmina-alfa 2, uma inibidor de protease serina.
A deficiência de plasmina pode gerar um trombose, já que os coágulos não são degradados adequadamente.
- PAI
Sendo o PAI(Inibidor de Ativador de Plasminogênio)-1 endotelial e PAI-2 presente na placenta(durante gravides), ambos com função e inibir o plasminogênio e não ocorrer hemorragia e fibrinólise , como mecanismo homeostático do organismo , um receptor conhecido que expressa o PAI é o AT4 (Estimulado pela presença de Angeotesina II) do Eixo Renina Angeotensina.
- Fármacos:
Existem fármacos que geram atividade anti-trombótica, anticoagulantes, fibrinolíticas, antiplaquetárias sendo que podemos citar a Heparina(uma molécula grande de composição glicêmica-não podendo ser utilizada por via oral) que pode gerar atividade auto imune com potencial trombogênico (reverso) , Low Molecular Weight Heparine (mais seguro que, Heparina) e o mais seguro Fondaparinux , além da Hirudina (provida da sanguessuga) e Bivalirudina(Análogo da Hirudina). Sendo ambas a Hirudina e seu análogo Bivalirudina, aplicados de forma sub-cutânea. Para além o Rivaroxabam , Dabigatram Etexilato(Pró fármaco-com grupamento açúcar, que é digerido pela fisiologia bucal, porém libara o composto ativo). Das Drogas fibrinolíticas inespecíficas existem a Uroquinase(Não imunogênico) e Estreptoquinase(Imunogênico - pode ter alteração Imune), logo os específicos são Alteplase e Reteplase, sendo fármacos que atuam a nível fibrino específico(local do trombo). Como das classes dos antiplaquetários , os mais famosos são Acidoacetilsalicílico, Clopidogrel e Tirofiban. Assim como os antagonista da Vitamina K(Warfarin-Anticoagulante).
Mecanismo de ativação do plasminogênio
O plasminogênio completo compreende sete domínios. Além de um domínio C-terminal de serina protease semelhante à quimotripsina, o plasminogênio contém um domínio N-terminal Pan Apple (PAp) [en] juntamente com cinco domínios Kringle (KR1-5). O domínio Pan-Apple contém determinantes importantes para manter o plasminogênio na forma fechada, e os domínios kringle são responsáveis pela ligação aos resíduos de lisina presentes nos recetores e substratos.[9]
A estrutura cristalina de raios X do plasminogênio fechado revela que os domínios PAp e SP mantêm a conformação fechada por meio de interações realizadas em toda a matriz kringle.[9] Os iões de cloreto ligam ainda mais as interfaces PAp / KR4 e SP / KR2, explicando o papel fisiológico do cloreto sérico na estabilização do conformador fechado. Os estudos estruturais também revelam que as diferenças na glicosilação alteram a posição do KR3.
No plasminogênio fechado, o acesso à ligação de ativação (R561/V562) alvo da clivagem pelo tPA e uPA é bloqueado pela posição da sequência do ligante KR3/KR4 e do açúcar O-ligado em T346. A posição do KR3 também pode impedir o acesso ao loop de ativação. As interações entre domínios também bloqueiam todos os locais de ligação do ligante kringle, exceto o do KR-1, sugerindo que este último domínio controla o recrutamento da pró-enzima para os alvos. A análise de uma estrutura intermediária do plasminogênio sugere que a mudança conformacional do plasminogênio para a forma aberta é iniciada através do KR-5 que se separa transitoriamente do domínio PAp. Esses movimentos expõem o local de ligação da lisina KR5 a potenciais parceiros de ligação e sugerem a necessidade de resíduos de lisina espacialmente distintos para provocar o recrutamento do plasminogênio e a mudança conformacional, respectivamente.[9]
Ver também
- Trombospondina 1
Referências
- ↑ http://www.ncbi.nlm.nih.gov/pubmed/8639779
- ↑ https://books.google.com.br/books?id=IcSwW2iMCy8C&pg=PA75&lpg=PA75&dq=PAI+2+placentaria&source=bl&ots=KDnlueK-E8&sig=KSY_rZOGcfeU3b30V8UVPbHlX6w&hl=pt-BR&sa=X&ved=0CCgQ6AEwAmoVChMI56mRtf6RyAIVRoCQCh1VnA1O#v=onepage&q=PAI%202%20placentaria&f=false
- ↑ https://books.google.com.br/books?id=13g_niZy0usC&pg=PA114&dq=dabigatran&hl=pt-BR&sa=X&ved=0CBwQ6AEwAGoVChMIv66V6v6RyAIVA4uQCh0AZACX#v=onepage&q=dabigatran&f=false
- ↑ https://books.google.com.br/books?id=C7_NBQAAQBAJ&pg=PA611&dq=rivaroxaban&hl=pt-BR&sa=X&ved=0CCUQ6AEwAWoVChMIlcHWyICSyAIVSBqQCh1T4Q2j#v=onepage&q=rivaroxaban&f=false
- ↑ https://books.google.com.br/books?id=mK8kBQAAQBAJ&pg=PA218&dq=%C3%A1cido+acetilsalic%C3%ADlico&hl=pt-BR&sa=X&ved=0CCkQ6AEwAWoVChMI9cXTyIKSyAIVCiKQCh00YAzZ#v=onepage&q=%C3%A1cido%20acetilsalic%C3%ADlico&f=false
- ↑ https://books.google.com.br/books?id=7VsLZG7JgFgC&pg=PA36&dq=clopidogrel&hl=pt-BR&sa=X&ved=0CEkQ6AEwBWoVChMI1bSogoOSyAIVSxGQCh1jzwEB#v=onepage&q=clopidogrel&f=false
- ↑ https://books.google.com.br/books?id=y3R1Vd3NHqcC&pg=PA134&dq=tirofiban&hl=pt-BR&sa=X&ved=0CCsQ6AEwAmoVChMIyOmrm4OSyAIVRkKQCh1BFgOp#v=onepage&q=tirofiban&f=false
- ↑ https://books.google.com.br/books?id=b0d9A5HuidwC&printsec=frontcover&dq=warfarin&hl=pt-BR&sa=X&ved=0CBwQ6AEwAGoVChMIsPPRwoOSyAIVyouQCh3P6gI_#v=onepage&q=warfarin&f=false
- 1 2 3 Law RH, Caradoc-Davies T, Cowieson N, Horvath AJ, Quek AJ, Encarnacao JA, et al. (março 2012). «The X-ray crystal structure of full-length human plasminogen». Cell Reports. 1 (3): 185–190. PMID 22832192. doi:10.1016/j.celrep.2012.02.012
