Interleucina 8
Interleucina 8 (IL-8) é o principal mediador da resposta imune inata inicial aos micróbios intracelulares e é indutora-chave da imunidade mediada por célula, a resposta adquirida contra esses micróbios. Produzida pelos fagócitos mononucleares ativados e pelas células dendríticas, estimula a diferenciação dos linfócitos Th em Th1 produtores de IFN-γ.
Produção e Síntese
É produzida por macrófagos, células epiteliais e linfócitos T. Em seres humanos, a interleucina-8, proteína é codificada pelo IL8 gene. IL-8 é inicialmente produzida como um peptídeo precursor de 99 aminoácidos de comprimento, que é então submetido a clivagem para criar várias isoformas ativas de IL-8. Em cultura, um peptídeo de ácido amino 72 é a principal forma segregada por macrófagos.
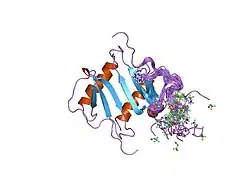
Gene e estrutura proteica
| Símbolo Oficial | CXCL8 C-X-C motif chemokine ligand 8 [ Homo sapiens (human) ] |
| Também conhecido como | L8; NAF; GCP1; LECT; LUCT; NAP1; GCP-1; LYNAP; MDNCF; MONAP; NAP-1 |
| Linhagem | Eukaryota; Metazoa; Chordata; Craniata; Vertebrata; Euteleostomi; Mammalia; Eutheria; Euarchontoglires; Primates; Haplorrhini; Catarrhini; Hominidae; Homo |
| Fonte primária | HGNC:HGNC:6025 |
| Tipo de gene | codificação de proteínas |
A interleucina-8 (IL-8) (Human Interleukin-8) é uma quimiocina membro da família das citocinas que possui atividade quimiotática para tipos de leucócitos específicos. Quimiocinas são basicamente proteínas com baixo massa molecular e com afinidade a heparina, aumentam a quimiocinese e são fator quimiotático. IL-8 está presente nos fluidos sinoviais de pacientes com artrite reumatóide. Esta também associada com sepse, asma e glomerulonefrites.
Atividade / função
A principal ação da IL-8 é o grande estímulo migratório para as células do sistema imune, principalmente neutrófilos, determinando ainda um aumento da expressão de moléculas de adesão por células endoteliais. Também ativa polimorfonucleares neutrofílicos, aumentando o metabolismo oxidativo. Antagoniza a produção de IgE estimulada pela IL-4, mas não afeta a produção das demais imunoglobulinas.
Papel em doenças/patologias associadas
Altas concentrações são observadas em psoríases, o que pode explicar a paraceratose e a hiperceratose observadas, uma vez que esta citocina estimula a divisão dos queratinócitos. Os microabscessos de Munro também podem ser atribuídos a esta citocina, pois são formados por neutrófilos.
Estudos realizados em culturas de células epiteliais de pacientes sem rinite alérgica, pacientes com rinite alérgica e pacientes portadores de polipose nasal demonstraram que as células de pacientes com rinite e pólipo sintetizam significativamente grande quantidade de IL-8 e GM-CSF. Esta citocina, IL-8, apresenta importante função na fase tardia da reação alérgica, especialmente, na indução da liberação de histamina e leucotrienos. Foi localizada nas células epiteliais da mucosa nasal, semelhante a IL-6, e nas células das glândulas da camada superficial da lâmina própria, próxima dos sinusóides e perto das veias da camada profunda da lâmina própria. Biópsias de mucosa nasal foram colhidas antes e após 1 hora, 24 horas e 1 semana da estimulação alergênica. Observou-se um aumento significante de eosinófilos, IL-8, IL-1B e RANTES (Regulated and normal t cell expressed and secreted) na primeira hora e nas 24 horas seguintes.
Regulação da expressão de CXCL8
O gene CXCL8 está localizado no cromossoma 4q13-21 e consiste em quatro exões e três intrões, apresentando uma estrutura única semelhante a CAT e TATA.[1] A região promotora proximal, contendo aproximadamente 200 nucleótidos na região flanqueante 5', desempenha um papel significativo na regulação transcricional [en] do CXCL8. Notavelmente, esta região flanqueante 5' difere significativamente de outros genes de citocinas e reagentes de fase aguda.[1]
Nas células em repouso, o CXCL8 está presente em níveis extremamente baixos, tornando-o difícil de detectar. No entanto, a expressão do CXCL8 é induzida por uma série de fatores e estressores, com os fatores de transcrição NF-κB e proteína ativadora-1 (AP-1) desempenhando papéis fundamentais na mediação dessa resposta. Essa indução resulta num aumento significativo na expressão de CXCL8, variando normalmente de 10 a 100 vezes.[1] A IL-8 e outras citocinas inflamatórias formam um ciclo vicioso com o NF-κB.[2]
Também se descobriu que as vias que conduzem à indução da fosforilação da proteína ribossomal S6 (rpS6) aumentam a síntese da proteína IL-8. Este controlo translacional da expressão da IL-8 depende de sequências proximais ricas em AU (APS), que se encontram na região 3 ' não traduzida (3' UTR) da IL-8 imediatamente após o códon de paragem. A 3' UTR da CXCL8 também contém elementos ricos em adenilato-uridilato (AREs), que aceleram a degradação do mRNA.[3]
Além disso, o MicroRNA-146a-5p (miR-146a-5p) reprime indiretamente a expressão de IL-8 ao silenciar o IRAK1 [en].[4] Entre vários microRNAs (miRs), o miR-146a-5p foi identificado como um regulador anti-inflamatório que tem como alvo moléculas de sinalização na via NF-κB.[5]
Notavelmente, os polimorfismos genéticos no gene CXCL8 podem influenciar a sua atividade transcricional, alterando potencialmente a produção de IL-8 e contribuindo para variações na suscetibilidade, progressão e gravidade da doença entre os indivíduos.[1]
Referências
- 1 2 3 4 Shkundin A, Halaris A (maio 2024). «IL-8 (CXCL8) Correlations with Psychoneuroimmunological Processes and Neuropsychiatric Conditions». Journal of Personalized Medicine. 14 (5): 488. PMC 11122344
 . PMID 38793070. doi:10.3390/jpm14050488
. PMID 38793070. doi:10.3390/jpm14050488
- ↑ Rottner M, Freyssinet JM, Martínez MC (março 2009). «Mechanisms of the noxious inflammatory cycle in cystic fibrosis». Respiratory Research. 10 (1). PMC 2660284
 . PMID 19284656. doi:10.1186/1465-9921-10-23
. PMID 19284656. doi:10.1186/1465-9921-10-23
- ↑ Ang Z, Koean RA, Er JZ, Lee LT, Tam JK, Guo H, Ding JL (abril 2019). «Novel AU-rich proximal UTR sequences (APS) enhance CXCL8 synthesis upon the induction of rpS6 phosphorylation». PLOS Genetics. 15 (4). PMC 6476525
 . PMID 30969964. doi:10.1371/journal.pgen.1008077
. PMID 30969964. doi:10.1371/journal.pgen.1008077
- ↑ Bhaumik D, Scott GK, Schokrpur S, Patil CK, Orjalo AV, Rodier F, Lithgow GJ, Campisi J (abril 2009). «MicroRNAs miR-146a/b negatively modulate the senescence-associated inflammatory mediators IL-6 and IL-8». Aging. 1 (4): 402–411. PMC 2818025
 . PMID 20148189. doi:10.18632/aging.100042
. PMID 20148189. doi:10.18632/aging.100042 - ↑ Lo WY, Wang SJ, Wang HJ (30 de outubro de 2020). «Non-canonical Interaction Between O-Linked N-Acetylglucosamine Transferase and miR-146a-5p Aggravates High Glucose-Induced Endothelial Inflammation». Frontiers in Physiology. 11. PMC 7662465
 . PMID 33192537. doi:10.3389/fphys.2020.01091
. PMID 33192537. doi:10.3389/fphys.2020.01091