Diálise
Diálise renal[a] é o processo de remoção do excesso de água, solutos e toxinas do sangue em pessoas cujos rins já não conseguem realizar estas funções naturalmente. Juntamente com o transplante renal, é um tipo de terapia de substituição renal.
A diálise pode necessitar de ser iniciada quando ocorre uma perda rápida e súbita da função renal, conhecida como lesão renal aguda (anteriormente chamada insuficiência renal aguda), ou quando um declínio gradual da função renal, insuficiência renal crónica, atinge o estágio 5. O estágio 5 da insuficiência renal crónica é alcançado quando a taxa de filtração glomerular é inferior a 15% do normal, a depuração da creatinina é inferior a 10 mL por minuto e a uremia está presente.[1]
A diálise é utilizada como uma medida temporária na lesão renal aguda ou naqueles que aguardam um transplante renal, e como uma medida permanente naqueles para quem o transplante não é indicado ou não é possível.[2]
Nos países da Europa Ocidental, Austrália, Canadá, Reino Unido e Estados Unidos, a diálise é paga pelo governo para aqueles que são elegíveis.[3][4] A primeira diálise bem-sucedida foi realizada em 1943.
Contexto

Os rins têm um papel importante na manutenção da saúde. Quando a pessoa está saudável, os rins mantêm o equilíbrio interno de água e minerais do corpo (sódio, potássio, cloreto, cálcio, fósforo, magnésio, sulfato). Os produtos finais do metabolismo ácido que o corpo não consegue eliminar através da respiração também são excretados pelos rins. Os rins também funcionam como parte do sistema endócrino, produzindo eritropoietina, calcitriol e renina. A eritropoietina está envolvida na produção de glóbulos vermelhos e o calcitriol desempenha um papel na formação óssea.[5] A diálise é um tratamento imperfeito para substituir a função renal porque não corrige as funções endócrinas comprometidas do rim. Os tratamentos de diálise substituem algumas destas funções através da difusão (remoção de resíduos) e ultrafiltração (remoção de fluidos).[6] A diálise utiliza água altamente purificada (também conhecida como "ultrapura").[7]
Princípio
A diálise funciona baseada nos princípios da difusão de solutos e na ultrafiltração de fluidos através de uma membrana semipermeável. A difusão é uma propriedade das substâncias na água; as substâncias na água tendem a mover-se de uma área de alta concentração para uma área de baixa concentração.[8] O sangue flui por um lado de uma membrana semipermeável, e um dialisante, ou fluido de diálise especial, flui pelo lado oposto. Uma membrana semipermeável é uma fina camada de material que contém furos de vários tamanhos, ou poros. Solutos menores e fluidos passam através da membrana, mas a membrana bloqueia a passagem de substâncias maiores (por exemplo, glóbulos vermelhos e grandes proteínas). Isto replica o processo de filtragem que ocorre nos rins quando o sangue entra nos mesmos e as substâncias maiores são separadas das menores no glomérulo.[8]

Os dois tipos principais de diálise, hemodiálise e diálise peritoneal, removem resíduos e excesso de água do sangue de formas diferentes.[2] A hemodiálise remove resíduos e água circulando o sangue fora do corpo através de um filtro externo, chamado dialisador, que contém uma membrana semipermeável. O sangue flui numa direção e o dialisante flui na direção oposta. O fluxo em contracorrente do sangue e do dialisante maximiza o gradiente de concentração de solutos entre o sangue e o dialisante, o que ajuda a remover mais ureia e creatinina do sangue. As concentrações de solutos normalmente encontrados na urina (por exemplo, potássio, fósforo e ureia) são indesejavelmente altas no sangue, mas baixas ou ausentes na solução de diálise, e a substituição constante do dialisante garante que a concentração de solutos indesejados seja mantida baixa deste lado da membrana. A solução de diálise possui níveis de minerais como potássio e cálcio que são semelhantes à sua concentração natural no sangue saudável. Para outro soluto, o bicarbonato, o nível da solução de diálise é ajustado para um nível ligeiramente superior ao do sangue normal, para incentivar a difusão de bicarbonato para o sangue, para atuar como um tampão de pH para neutralizar a acidose metabólica que está frequentemente presente nestes pacientes. Os níveis dos componentes do dialisante são tipicamente prescritos por um nefrologista de acordo com as necessidades individuais do paciente.
Na diálise peritoneal, os resíduos e a água são removidos do sangue dentro do corpo utilizando o peritoneu como uma membrana semipermeável natural. Os resíduos e o excesso de água movem-se do sangue, através do peritoneu visceral devido à sua grande área de superfície, para uma solução de diálise especial, chamada dialisante, na cavidade peritoneal dentro do abdómen.
Tipos
Existem três tipos primários e dois secundários de diálise: hemodiálise (primário), diálise peritoneal (primário), hemofiltração (primário), hemodiafiltração (secundário) e diálise intestinal (secundário).
Hemodiálise
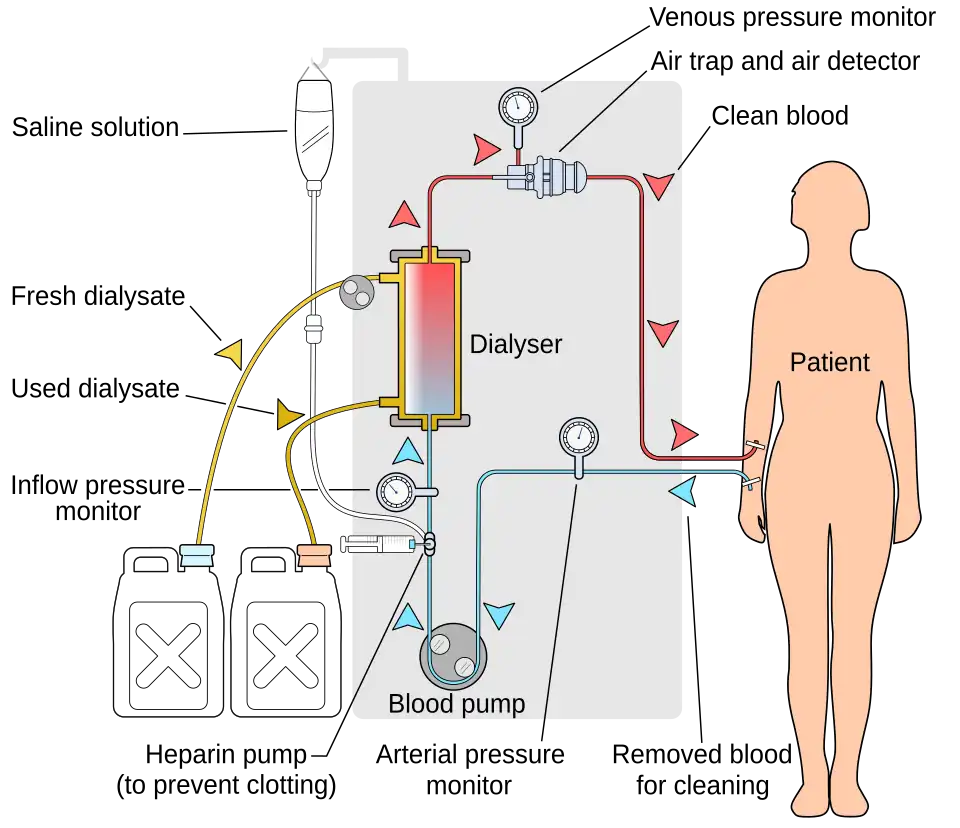
Na hemodiálise, o sangue do paciente é bombeado através do compartimento de sangue de um dialisador, expondo-o a uma membrana parcialmente permeável. O dialisador é composto por milhares de minúsculas fibras sintéticas ocas. A parede da fibra atua como a membrana semipermeável. O sangue flui através das fibras, a solução de diálise flui pelo lado de fora das fibras, e a água e os resíduos movem-se entre estas duas soluções.[9] O sangue limpo é então devolvido através do circuito de volta ao corpo. A ultrafiltração ocorre através do aumento da pressão hidrostática através da membrana do dialisador. Isto é feito habitualmente aplicando uma pressão negativa ao compartimento do dialisante no dialisador. Este gradiente de pressão faz com que a água e os solutos dissolvidos se movam do sangue para o dialisante e permite a remoção de vários litros de excesso de fluido durante um tratamento típico de 4 horas. Nos Estados Unidos, os tratamentos de hemodiálise são tipicamente administrados num centro de diálise três vezes por semana (devido às regras de reembolso do Medicare); no entanto, em 2005, mais de 2.500 pessoas nos Estados Unidos faziam diálise em casa com mais frequência para vários períodos de tratamento.[10] Estudos demonstraram os benefícios clínicos de dialisar 5 a 7 vezes por semana, durante 6 a 8 horas. Este tipo de hemodiálise é habitualmente chamado de hemodiálise diária noturna e um estudo mostrou que proporciona uma melhoria significativa na depuração de moléculas de pequeno e grande peso molecular e diminui a necessidade de quelantes de fosfato.[11] Estes tratamentos longos e frequentes são muitas vezes feitos em casa enquanto se dorme, mas a diálise domiciliária é uma modalidade flexível e os horários podem ser alterados de dia para dia ou semana para semana. Em geral, os estudos mostram que tanto o aumento da duração como da frequência do tratamento são clinicamente benéficos.[12]
A hemodiálise foi um dos procedimentos mais comuns realizados nos hospitais dos EUA em 2011, ocorrendo em 909.000 estadias (uma taxa de 29 estadias por 10.000 habitantes).[13]
Diálise peritoneal
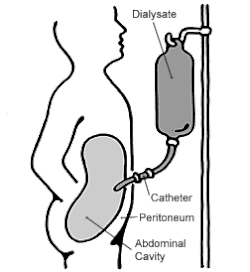
Na diálise peritoneal, uma solução estéril contendo glicose (chamada dialisante) é introduzida através de um tubo na cavidade peritoneal, a cavidade abdominal ao redor do intestino, onde a membrana peritoneal atua como uma membrana parcialmente permeável.
Esta troca é repetida 4–5 vezes por dia; sistemas automáticos podem realizar ciclos de troca mais frequentes durante a noite. A diálise peritoneal é menos eficiente que a hemodiálise, mas como é realizada por um período de tempo mais longo, o efeito líquido em termos de remoção de produtos residuais e de sal e água é semelhante à hemodiálise. A diálise peritoneal é realizada em casa pelo paciente, muitas vezes sem ajuda. Isto liberta os pacientes da rotina de terem de ir a uma clínica de diálise num horário fixo várias vezes por semana. A diálise peritoneal pode ser realizada com pouco ou nenhum equipamento especializado (além dos sacos de dialisante fresco).
Hemofiltração
.svg.png)
A hemofiltração é um tratamento semelhante à hemodiálise, mas utiliza um princípio diferente. O sangue é bombeado através de um dialisador ou "hemofiltro" como na diálise, mas não é utilizado dialisante. É aplicado um gradiente de pressão; como resultado, a água move-se através da membrana muito permeável rapidamente, "arrastando" consigo muitas substâncias dissolvidas, incluindo aquelas com grandes pesos moleculares, que não são tão bem eliminadas pela hemodiálise. Os sais e a água perdidos do sangue durante este processo são substituídos por um "fluido de substituição" que é infundido no circuito extracorpóreo durante o tratamento.
Hemodiafiltração
.svg.png)
A hemodiafiltração é uma combinação entre hemodiálise e hemofiltração, sendo assim utilizada para purificar o sangue de toxinas quando o rim não está a funcionar normalmente e também utilizada para tratar a lesão renal aguda (LRA).
Diálise intestinal
Em humanos saudáveis, os intestinos removem toxinas urémicas (ureia, creatina, ácido úrico) do sangue e adicionam toxinas urémicas (sulfato de indoxilo, amónia, etc.) ao sangue. Mais toxinas urémicas são excretadas através do intestino (como fezes) do que através dos rins (como urina). Esta troca de substâncias é possibilitada pela enorme área de superfície da rede capilar intestinal e do muco intestinal, que juntos servem como uma grande membrana semipermeável. Em pacientes com insuficiência renal, os intestinos recebem um maior influxo de toxinas urémicas devido a uma maior concentração no sangue, mas isto não se traduz automaticamente num benefício na redução dos níveis de toxinas no sangue, uma vez que as bactérias intestinais utilizam estas toxinas como alimento, produzindo mais toxinas no processo. O objetivo da diálise intestinal é maximizar a remoção de toxinas urémicas para os intestinos, minimizando simultaneamente a produção de novas moléculas de toxinas nos mesmos. Serve como uma terapia de substituição renal mais conservadora para aqueles incapazes de tolerar a diálise convencional. Existem algumas formas de diálise intestinal:[14]
- A diálise do intestino delgado coloca o dialisante no intestino delgado através de uma abertura cirúrgica (ileostomia), utilizando as paredes intestinais como membrana semipermeável para a remoção de toxinas. Não mostrou qualquer benefício real de sobrevivência global e foi substituída por métodos modernos de diálise.[14]
- A diarreia induzida demonstrou proporcionar a remoção de toxinas em estudos pequenos e não controlados aleatoriamente. Um método utiliza a ingestão de 1 a 1,5 litros de soluções não absorvíveis de polietilenoglicol ou manitol a cada quatro horas.[15]
- A diálise colónica coloca o dialisante no cólon, o que pode ser feito sem uma abertura cirúrgica: um cateter anal inserido através do ânus pode atingir o cólon ascendente e injetar o dialisante ali. O uso clínico da diálise colónica está ainda nas fases iniciais (em 2020), sendo estudado principalmente no Irão e na China.[14][16]
- Os adsorventes orais são utilizados na esperança de que absorvam as toxinas à medida que passam pelo intestino. Um deles, o AST-120, foi submetido a dois ensaios clínicos aleatorizados controlados multinacionais nos quais falhou em mostrar benefício no retardamento da progressão da DRC. No entanto, uma análise post-hoc encontrou algum benefício num subgrupo de pacientes.[16]
Um desenvolvimento relacionado é a suplementação com fibras solúveis, como a fibra de acácia, na dieta. Estas fibras são digeridas por bactérias no cólon. Este crescimento bacteriano aumenta a quantidade de nitrogénio que é eliminado nos resíduos fecais.[17][18]
Indicações
A decisão de iniciar a diálise ou hemofiltração em pacientes com insuficiência renal depende de vários fatores. Estes podem ser divididos em indicações agudas ou crónicas.
A depressão e os sintomas de insuficiência renal podem ser semelhantes entre si. É importante que exista uma comunicação aberta entre a equipa de diálise e o paciente. A comunicação aberta permitirá proporcionar uma melhor qualidade de vida. Conhecer as necessidades dos pacientes permitirá que a equipa de diálise ofereça mais opções como: mudanças no tipo de diálise, como a diálise domiciliária para que os pacientes possam ser mais ativos, ou mudanças nos hábitos alimentares para evitar produtos residuais desnecessários.
Indicações agudas
As indicações para diálise num paciente com lesão renal aguda são resumidas com a mnemónica vocálica de "AEIOU":[19]
- Acidemia por acidose metabólica em situações em que a correção com bicarbonato de sódio é impraticável ou pode resultar em sobrecarga de fluidos.
- Anormalidade de eletrólitos, como hipercaliemia grave, especialmente quando combinada com LRA.
- Intoxicação, ou seja, envenenamento agudo com uma substância dialisável. Estas substâncias podem ser representadas pela mnemónica SLIME: ácido salicílico, lítio, isopropanol, laxantes contendo magnésio e etilenoglicol.
- Sobrecarga de fluidos que não se espera que responda ao tratamento com diuréticos.
- Complicações de Uremia, como pericardite, encefalopatia ou hemorragia gastrointestinal.
Indicações crónicas
A diálise crónica pode ser indicada quando um paciente tem insuficiência renal sintomática e baixa taxa de filtração glomerular (TFG < 15 mL/min).[20] Entre 1996 e 2008, houve uma tendência para iniciar a diálise em TFGe progressivamente mais elevadas. Uma revisão da evidência não mostra benefício ou danos potenciais com o início precoce da diálise, que tem sido definido pelo início da diálise com uma TFG estimada superior a 10 ml/min/1,732. Dados observacionais de grandes registos de pacientes em diálise sugerem que o início precoce da diálise pode ser prejudicial.[21] As diretrizes publicadas mais recentemente no Canadá, para quando iniciar a diálise, recomendam a intenção de adiar a diálise até que um paciente tenha sintomas definitivos de insuficiência renal, o que pode ocorrer com uma TFG estimada de 5–9 ml/min/1,732.[22]
Impacto
Eficácia
Embora não seja uma cura para a insuficiência renal, a diálise é um tratamento muito eficaz.[23] As taxas de sobrevivência da insuficiência renal são geralmente mais longas com diálise do que sem ela (tendo apenas gestão renal conservadora). No entanto, a partir dos 80 anos e em pacientes idosos com comorbilidades, não há diferença na sobrevivência entre os dois grupos.[24]
Qualidade de vida
A diálise é um tratamento intensivo que tem um impacto sério naqueles que são tratados com ela. Estar em diálise geralmente leva a uma má qualidade de vida. No entanto, existem estratégias que podem torná-la mais tolerável.[25] Receber diálise em casa pode melhorar a qualidade de vida e a autonomia das pessoas.[25]
Horário e adesão
A diálise é tipicamente realizada num horário regular de três vezes por semana.
Dado que os pacientes em diálise têm pouca ou nenhuma capacidade de filtrar solutos e regular o seu volume de fluidos devido à disfunção renal,[26] faltar à diálise é potencialmente letal. Estes pacientes podem ficar hipercaliémicos, levando a disritmias cardíacas e potencial paragem cardíaca,[27] bem como fluido nos alvéolos dos seus pulmões, o que pode prejudicar a respiração.[28]
Alguns medicamentos podem ser utilizados a curto prazo para diminuir o potássio sérico e estabilizar o músculo cardíaco, de modo a facilitar a estabilização de pacientes agudos em situação de falta de diálise. O Salbutamol e a insulina podem diminuir o potássio sérico em até 1,0 mmol/L cada, deslocando o potássio do espaço extracelular para os espaços intracelulares dentro das células musculares esqueléticas, e o gluconato de cálcio é utilizado para estabilizar o miocárdio em pacientes hipercaliémicos, numa tentativa de reduzir a probabilidade de ocorrência de arritmias letais resultantes de um potássio sérico elevado.[29]
Sobrevivência sem diálise
As pessoas que decidem não fazer o tratamento de diálise ao atingirem a doença renal crónica terminal podem sobreviver vários anos e experienciar melhorias no seu bem-estar mental, além de bem-estar físico sustentado e qualidade de vida global até tarde no curso da sua doença. No entanto, o uso de serviços de cuidados agudos nestes casos é comum e a intensidade dos cuidados de fim de vida é altamente variável entre as pessoas que optam por não fazer diálise.[30][31]
Expectativa de Vida Após o Início da Diálise Renal
A expectativa de vida após o início da diálise renal para a doença renal terminal (DRT) varia significativamente com base em fatores como idade, comorbilidades, modalidade de diálise e acesso a cuidados de saúde. A diálise prolonga a vida em comparação com a DRT não tratada, mas não restaura a função renal normal. A sobrevivência média é de aproximadamente 3–5 anos, com taxas de sobrevivência de 5 anos em torno de 35–42% para pacientes em hemodiálise (HD).[32][33] A mortalidade é mais elevada no primeiro ano (15–20%), principalmente por eventos cardiovasculares ou infeções.
Sobrevivência global
Para pacientes incidentes em diálise (idade média ~65 anos), a sobrevivência média é de cerca de 3 anos, com taxas de mortalidade ajustadas de 187,7 por 1.000 pacientes-ano.[32][34]
Sobrevivência a 1 ano: 80–85% global; 60–70% para pacientes ≥65 anos.[35] Sobrevivência a 3 anos: ~57% para HD, ~68% para diálise peritoneal (DP).[36] Sobrevivência a 5 anos: 35–42% para HD; os resultados da DP convergem a longo prazo.[32][37]
Sobrevivência por idade
A taxa de sobrevivência dos pacientes em diálise diminui significativamente com a idade. A diálise peritoneal tem um resultado ligeiramente melhor do que a hemodiálise, particularmente para pacientes mais velhos.[38]
| Grupo etário | Modalidade | taxa de sobrevivência (%) | |||
|---|---|---|---|---|---|
| 1 ano | 3 anos | 5 anos | 10 anos | ||
| <45 | hemodiálise | 92 | 80 | 70 | |
| peritoneal | 94 | 82 | 72 | ||
| 45–64 | hemodiálise | 88 | 70 | 55 | |
| peritoneal | 90 | 74 | 58 | ||
| 65–74 | hemodiálise | 82 | 57 | 40 | |
| peritoneal | 85 | 62 | 45 | ||
| 75–84 | hemodiálise | 70 | 37 | 20 | |
| peritoneal | 75 | 45 | 28 | ||
| 85+ | hemodiálise | 50 | 15 | 5 | |
| peritoneal | 60 | 25 | 10 | ||
Notas
- ↑ Do grego διάλυσις, dialysis, 'dissolução'; de διά, dia, 'através', e λύσις, lysis, 'afrouxamento ou divisão'
Ver também
Referências
- ↑ AMGEN Canada Inc. Essential Concepts in Chronic Renal Failure. A Practical Continuing Education Series. Mississauga, 2008: p. 36.
- 1 2 Pendse S, Singh A, Zawada E. "Initiation of Dialysis". In: Handbook of Dialysis. 4th ed. New York; 2008:14–21
- ↑ Kelly DM, Anders HJ, Bello AK, Choukroun G, Coppo R, Dreyer G, Eckardt KU, Johnson DW, Jha V, Harris DC, Levin A, Lunney M, Luyckx V, Marti HP, Messa P, Mueller TF, Saad S, Stengel B, Vanholder RC, Weinstein T, Khan M, Zaidi D, Osman MA, Ye F, Tonelli M, Okpechi IG, Rondeau E (maio 2021). «International Society of Nephrology Global Kidney Health Atlas: structures, organization, and services for the management of kidney failure in Western Europe». Kidney International Supplements. 11 (2): e106–e118. PMC 8084721
 . PMID 33981476. doi:10.1016/j.kisu.2021.01.007
. PMID 33981476. doi:10.1016/j.kisu.2021.01.007 - ↑ «Financial Help for Treatment of Kidney Failure» (em inglês). National Institute of Diabetes and Digestive and Kidney Diseases. Consultado em 14 de abril de 2021
- ↑ Brundage D. Renal Disorders. St. Louis, MO: Mosby; 1992
- ↑ «Atlas of Diseases of the Kidney, Volume 5, Principles of Dialysis: Diffusion, Convection, and Dialysis Machines» (PDF). Consultado em 2 de setembro de 2011. Cópia arquivada (PDF) em 26 de julho de 2011
- ↑ «Home Hemodialysis and Water Treatment». Davita. Consultado em 3 junho 2017. Cópia arquivada em 25 setembro 2017
- 1 2 Mosby's Dictionary of Medicine, Nursing, & Health Professions. 7th ed. St. Louis, MO; Mosby: 2006
- ↑ Ahmad S, Misra Hemodialysis Apparatus. In: Handbook of Dialysis. 4th ed. New York, NY; 2008:59-78.
- ↑ «USRDS Treatment Modalities» (PDF). United States Renal Data System. Consultado em 2 de setembro de 2011. Arquivado do original (PDF) em 30 de setembro de 2011
- ↑ Rocco MV (julho 2007). «More frequent hemodialysis: back to the future?». Advances in Chronic Kidney Disease. 14 (3): e1–e9. PMID 17603969. doi:10.1053/j.ackd.2007.04.006
- ↑ «5 Types of Hemodialysis: Home Dialysis Central». www.homedialysis.org. Cópia arquivada em 5 de março de 2011
- ↑ Pfuntner A., Wier L.M., Stocks C. Most Frequent Procedures Performed in U.S. Hospitals, 2011. HCUP Statistical Brief #165. October 2013. Agency for Healthcare Research and Quality, Rockville, MD. .
- 1 2 3 Puri I, Shirazi NM, Yap E, Saggi SJ (2020). «Intestinal dialysis for conservative management of Uremia». Current Opinion in Nephrology and Hypertension. 29 (1): 64–70. PMID 31725008. doi:10.1097/MNH.0000000000000571
- ↑ Miskowiak J (1991). «Continuous intestinal dialysis for uraemia by intermittent oral intake of non-absorbable solutions. An experimental study». Scandinavian Journal of Urology and Nephrology. 25 (1): 71–4. PMID 1904625. doi:10.3109/00365599109024532
- 1 2 Sumida, K; Lau, WL; Kalantar-Zadeh, K; Kovesdy, CP (1 janeiro 2022). «Novel intestinal dialysis interventions and microbiome modulation to control uremia.». Current Opinion in Nephrology and Hypertension. 31 (1): 82–91. PMID 34846313. doi:10.1097/MNH.0000000000000753
- ↑ Al-Mosawi AJ (outubro 2004). «Acacia gum supplementation of a low-protein diet in children with end-stage renal disease». Pediatric Nephrology (Berlin, Germany). 19 (10): 1156–9. PMID 15293039. doi:10.1007/s00467-004-1562-5
- ↑ Ali AA, Ali KE, Fadlalla AE, Khalid KE (janeiro 2008). «The effects of gum arabic oral treatment on the metabolic profile of chronic renal failure patients under regular haemodialysis in Central Sudan». Natural Product Research. 22 (1): 12–21. PMID 17999333. doi:10.1080/14786410500463544
- ↑ Irwin RS, Rippe JM (2008). Irwin and Rippe's intensive care medicine. [S.l.]: Lippincott Williams & Wilkins. pp. 988–999. ISBN 978-0-7817-9153-3
- ↑ Tattersall J, Dekker F, Heimbürger O, Jager KJ, Lameire N, Lindley E, Van Biesen W, Vanholder R, Zoccali C (julho 2011). «When to start dialysis: updated guidance following publication of the Initiating Dialysis Early and Late (IDEAL) study». Nephrology, Dialysis, Transplantation. 26 (7): 2082–2086. PMID 21551086. doi:10.1093/ndt/gfr168

- ↑ Rosansky S, Glassock RJ, Clark WF (maio 2011). «Early start of dialysis: a critical review». Clinical Journal of the American Society of Nephrology. 6 (5): 1222–1228. PMID 21555505. doi:10.2215/cjn.09301010

- ↑ Nesrallah GE, Mustafa RA, Clark WF, Bass A, Barnieh L, Hemmelgarn BR, Klarenbach S, Quinn RR, Hiremath S, Ravani P, Sood MM, Moist LM (fevereiro 2014). «Canadian Society of Nephrology 2014 clinical practice guideline for timing the initiation of chronic dialysis». CMAJ. 186 (2): 112–117. PMC 3903737
 . PMID 24492525. doi:10.1503/cmaj.130363
. PMID 24492525. doi:10.1503/cmaj.130363 - ↑ «Dialysis». National Kidney Foundation (em inglês). Consultado em 27 de setembro de 2024
- ↑ Buur LE, Madsen JK, eidemak I, Krarup E, Lauridsen TG, Taasti LH, et al. (2021). «Does conservative kidney management offer a quantity or quality of life benefit compared to dialysis? A systematic review.». BMC Nephrol. 22 (1): 307. PMC 8434727
 . PMID 34507554. doi:10.1186/s12882-021-02516-6
. PMID 34507554. doi:10.1186/s12882-021-02516-6
- 1 2 «Dialysis for kidney failure: evidence to improve care»
 . National Institute for Health and Care Research. NIHR Evidence. 18 setembro 2024. doi:10.3310/nihrevidence_63287
. National Institute for Health and Care Research. NIHR Evidence. 18 setembro 2024. doi:10.3310/nihrevidence_63287 - ↑ Anderson AH, Cohen AJ, Kutner NG, Kopp JB, Kimmel PL, Muntner P (junho 2009). «Missed dialysis sessions and hospitalization in hemodialysis patients after Hurricane Katrina». Kidney International. 75 (11): 1202–1208. PMID 19212421. doi:10.1038/ki.2009.5

- ↑ Hunter RW, Bailey MA (dezembro 2019). «Hyperkalemia: pathophysiology, risk factors and consequences». Nephrology, Dialysis, Transplantation. 34 (Suppl 3): iii2–iii11. PMC 6892421
 . PMID 31800080. doi:10.1093/ndt/gfz206
. PMID 31800080. doi:10.1093/ndt/gfz206 - ↑ Campos I, Chan L, Zhang H, Deziel S, Vaughn C, Meyring-Wösten A, Kotanko P (2016). «Intradialytic Hypoxemia in Chronic Hemodialysis Patients». Blood Purification (em inglês). 41 (1–3): 177–187. PMC 6109968
 . PMID 26765143. doi:10.1159/000441271
. PMID 26765143. doi:10.1159/000441271 - ↑ Ahee P, Crowe AV (maio 2000). «The management of hyperkalaemia in the emergency department». Journal of Accident & Emergency Medicine. 17 (3): 188–191. PMC 1725366
 . PMID 10819381. doi:10.1136/emj.17.3.188
. PMID 10819381. doi:10.1136/emj.17.3.188 - ↑ Wong SP, Rubenzik T, Zelnick L, Davison SN, Louden D, Oestreich T, et al. (2022). «Long-term Outcomes Among Patients With Advanced Kidney Disease Who Forgo Maintenance Dialysis: A Systematic Review.». JAMA Netw Open. 5 (3): e222255. PMC 9907345
 . PMID 35285915. doi:10.1001/jamanetworkopen.2022.2255
. PMID 35285915. doi:10.1001/jamanetworkopen.2022.2255 - ↑ C. K. Liu, M. Kurella Tamura: Conservative Care for Kidney Failure-The Other Side of the Coin. In: JAMA network open. Band 5, Nummer 3, März 2022, S. e222252, doi:10.1001/jamanetworkopen.222252, PMID 35285925.
- 1 2 3 «2023 USRDS Annual Data Report». United States Renal Data System. Consultado em 12 de outubro de 2025
- ↑ Vaidya, S.; Aeddula, N.R. (2024). Chronic Kidney Disease. [S.l.]: StatPearls Publishing. PMID 30571025
- ↑ Chen, T.K.; Knicely, D.H.; Grams, M.E. (2019). «Chronic Kidney Disease Diagnosis and Management: A Review». JAMA. 322 (13): 1294–1304. Bibcode:2019JAMA..322.1294C. PMC 7015670
 . PMID 31573641. doi:10.1001/jama.2019.14745
. PMID 31573641. doi:10.1001/jama.2019.14745 - ↑ «2024 USRDS Annual Data Report». National Institute of Diabetes and Digestive and Kidney Diseases. Consultado em 12 de outubro de 2025
- ↑ Kim, Y.S.; Song, J.H.; Lee, S.H. (2019). «Better quality of life of peritoneal dialysis compared to hemodialysis over a two-year period». Sci Rep. 9 (1): 10239. doi:10.1038/s41598-019-46744-1
- ↑ Malhotra, A.; Soundararajan, K.; Kalra, S. (2014). «Survival of chronic hemodialysis patients over 80 years of age». J Am Geriatr Soc. 62 (2): 392–393. PMID 24521374. doi:10.1111/jgs.12682
- ↑ United States Renal Data System. 2022 USRDS Annual Data Report: Epidemiology of Kidney Disease in the United States. National Institutes of Health, National Institute of Diabetes and Digestive and Kidney Diseases; 2022. Available from: https://adr.usrds.org/2022