Crescimento bacteriano
Crescimento bacteriano[1] é a proliferação de bactérias em duas células-filhas ocorre em um processo chamado fissão binária. Se não ocorrer nenhuma mutação, as células-filhas resultantes são geneticamente idênticas à célula original. Portanto, ocorre o crescimento bacteriano. Nem todas as células-filhas da divisão sobrevivem necessariamente. No entanto, se o número de sobreviventes exceder a unidade em média, a população bacteriana entra em crescimento exponencial. A medição da curva de crescimento bacteriano exponencial em cultura descontínua era tradicionalmente parte do treinamento de todos os microbiologistas; o método básico requer a enumeração bacteriana (contagem de células) por métodos diretos e individuais (microscopia, citometria de fluxo[2]), métodos diretos e em massa (biomassa), indiretos e individuais (contagem de colônias) ou indiretos e em massa (número mais provável, turbidez, absorção de nutrientes). Os modelos conciliam a teoria com as medições.[3]
Fases
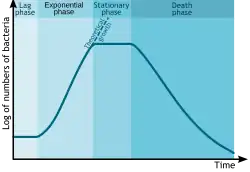
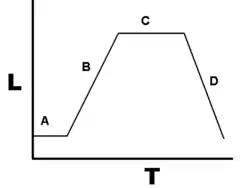
Em estudos autecológicos, o crescimento de bactérias (ou outros microrganismos, como protozoários, microalgas ou leveduras) em cultura de batelada pode ser modelado em quatro fases diferentes: fase lag ou de latência (A), fase log ou fase exponencial (B), fase estacionária (C) e fase de morte ou declínio (D).[4]
- Durante a fase lag (latência), as bactérias adaptam-se às condições de crescimento. É o período em que as bactérias individuais estão amadurecendo e ainda não são capazes de se dividir. Durante a fase lag do ciclo de crescimento bacteriano, ocorre a síntese de RNA, enzimas e outras moléculas. Durante esta fase, as células mudam muito pouco porque não se reproduzem imediatamente em um novo meio. Este período de pouca ou nenhuma divisão celular pode durar de 1 hora a vários dias. Durante esta fase, as células não estão dormentes.[5]
- A fase log (às vezes chamada de fase logarítmica ou fase exponencial) é um período caracterizado pela duplicação celular.[6] O número de novas bactérias que aparecem por unidade de tempo é proporcional à população atual. Se o crescimento não for limitado, a duplicação continuará a uma taxa constante, de modo que tanto o número de células quanto a taxa de aumento populacional dobram a cada período de tempo consecutivo. Para este tipo de crescimento exponencial, a plotagem do logaritmo natural do número de células em relação ao tempo produz uma linha reta. A inclinação desta linha é a taxa de crescimento específica do organismo, que é uma medida do número de divisões por célula por unidade de tempo.[6] A taxa real deste crescimento (ou seja, a inclinação da linha na figura) depende das condições de crescimento, que afetam a frequência dos eventos de divisão celular e a probabilidade de sobrevivência de ambas as células-filhas. Sob condições controladas, as cianobactérias podem dobrar sua população quatro vezes por dia e, em seguida, triplicar sua população.[7] O crescimento exponencial não pode continuar indefinidamente, no entanto, porque o meio logo se esgota de nutrientes e se enriquece com resíduos.
- A fase estacionária é frequentemente devida a um fator limitante do crescimento, como o esgotamento de um nutriente essencial e/ou a formação de um produto inibitório, como um ácido orgânico. A fase estacionária resulta de uma situação em que a taxa de crescimento e a taxa de morte são iguais. O número de novas células criadas é limitado pelo fator de crescimento e, como resultado, a taxa de crescimento celular corresponde à taxa de morte celular. O resultado é uma parte linear horizontal e "suave" da curva durante a fase estacionária. Mutações podem ocorrer durante a fase estacionária. Bridges et al. (2001)[8] apresentaram evidências de que danos no DNA (danos naturais no DNA) são responsáveis por muitas das mutações que surgem nos genomas de bactérias em fase estacionária ou em inanição. Espécies reativas de oxigênio geradas endogenamente aparecem ser uma importante fonte de tais danos.[8] As bactérias nesta fase às vezes entram em dormência, usando fatores de hibernação para retardar seu metabolismo.[9]
- Na fase de morte (fase de declínio), as bactérias morrem. Isso pode ser causado por falta de nutrientes, temperatura ambiental acima ou abaixo da faixa de tolerância para a espécie, ou outras condições prejudiciais.
Este modelo básico de crescimento em cultura de batelada extrai e enfatiza aspectos do crescimento bacteriano que podem diferir do crescimento da macrofauna. Ele enfatiza a clonalidade, a divisão binária assexuada, o curto tempo de desenvolvimento em relação à própria replicação, a taxa de mortalidade aparentemente baixa, a necessidade de passar de um estado dormente para um estado reprodutivo ou de condicionar o meio e, finalmente, a tendência de linhagens adaptadas em laboratório de exaurirem seus nutrientes. Na realidade, mesmo em cultura de batelada, as quatro fases não são bem definidas. As células não se reproduzem em sincronia sem estímulo explícito e contínuo (como em experimentos com bactérias pedunculadas [10]) e seu crescimento na fase exponencial muitas vezes não ocorre a uma taxa constante, mas sim a uma taxa de declínio lento, uma resposta estocástica constante a pressões tanto para se reproduzir quanto para entrar em dormência diante do declínio das concentrações de nutrientes e do aumento das concentrações de resíduos.
A diminuição do número de bactérias pode até se tornar logarítmica. Portanto, esta fase de crescimento também pode ser chamada de fase de crescimento logarítmico negativo ou exponencial negativo.
Perto do final da fase logarítmica de uma cultura de batelada, a competência para a transformação genética natural pode ser induzida, como em Bacillus subtilis[11] e em outras bactérias. A transformação genética natural é uma forma de transferência de DNA que parece ser uma adaptação para reparar danos no DNA.
Cultura de batelada é o método de crescimento laboratorial mais comum no qual o crescimento bacteriano é estudado, mas é apenas um entre muitos. É idealmente não estruturada espacialmente e estruturada temporalmente. A cultura bacteriana é incubada em um recipiente fechado com um único lote (batelada) de meio. Em alguns regimes experimentais, parte da cultura bacteriana é periodicamente removida e adicionada a um meio estéril fresco. No caso extremo, isso leva à renovação contínua dos nutrientes. Este é o quimiostato, também conhecido como cultura contínua. É idealmente não estruturado espacialmente e temporalmente, em um estado estacionário definido pelas taxas de suprimento de nutrientes e crescimento bacteriano. Em comparação com a cultura de batelada, as bactérias são mantidas na fase de crescimento exponencial, e a taxa de crescimento das bactérias é conhecida. Dispositivos relacionados incluem turbidostatos e auxostatos. Quando a Escherichia coli cresce muito lentamente com um tempo de duplicação de 16 horas em um quimiostato, a maioria das células tem um único cromossomo.[2]
O crescimento bacteriano pode ser suprimido com bacteriostáticos, sem necessariamente matar as bactérias. Certas toxinas podem ser usadas para suprimir o crescimento bacteriano ou matar bactérias. Antibióticos (ou, mais propriamente, drogas antibacterianas) são drogas usadas para matar bactérias; eles podem ter efeitos colaterais ou até causar reações adversas em pessoas, no entanto, não são classificados como toxinas. Em uma situação sinecologia, fiel à natureza, na qual mais de uma espécie bacteriana está presente, o crescimento de micróbios é mais dinâmico e contínuo.
O líquido não é o único ambiente laboratorial para o crescimento bacteriano. Ambientes espacialmente estruturados, como biofilmes ou superfícies de ágar, apresentam modelos de crescimento complexos adicionais.
Crescimento poliaúxico
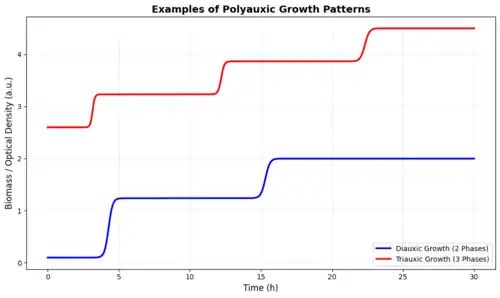
Crescimento poliaúxico (do grego poly que significa "muitos" e auxein que significa "crescer") refere-se a um padrão de crescimento microbiano multifásico caracterizado por múltiplas fases exponenciais distintas separadas por períodos estacionários ou de latência temporários. Este fenômeno ocorre quando microrganismos são cultivados em um meio complexo contendo uma mistura de fontes de carbono (substratos) que são consumidas sequencialmente em vez de simultaneamente.
A forma mais simples e clássica é o crescimento diaúxico (duas fases), descrito pela primeira vez com rigor por Jacques Monod em sua tese de doutorado (1941) e artigos subsequentes (1945).[12][13] Em seus experimentos com Escherichia coli, Monod observou que, quando fornecidas tanto glicose quanto lactose, as bactérias utilizavam preferencialmente a glicose primeiro porque é termodinamicamente mais eficiente de metabolizar. Durante esta primeira fase, as enzimas necessárias para o metabolismo da lactose são inibidas — um mecanismo regulador conhecido como repressão por catabólito. Somente após a glicose ser completamente exaurida, a população entra em uma fase lag temporária para sintetizar as enzimas necessárias (por exemplo, beta-galactosidase), levando a uma segunda fase de crescimento exponencial em lactose.
Em contextos ambientais ou industriais complexos, como a fermentação de hidrolisados de lignocelulose ou fluxos de resíduos, as bactérias podem encontrar diversos conjuntos de nutrientes, levando a padrões poliaúxicos de ordem superior (por exemplo, crescimento triáuxico ou tetra-áuxico). A modelagem matemática precisa dessas dinâmicas é essencial para o controle de bioprocessos. Enquanto modelos clássicos (como a Função de Gompertz) descrevem o crescimento de fase única, as estruturas semimecanísticas modernas representam a poliauxia como uma soma de múltiplas fases sigmoidais. Esses modelos permitem que pesquisadores estimem explicitamente parâmetros cinéticos como a taxa de crescimento específica máxima () e a duração da fase lag () para cada fase individual de consumo de substrato.[14][15]
A 5ª fase: Fase estacionária de longo prazo
A fase estacionária de longo prazo, ao contrário da fase estacionária inicial (na qual há pouca divisão celular), é um período altamente dinâmico no qual as taxas de nascimento e morte são equilibradas. Foi provado que, após a fase de morte, a E. coli pode ser mantida em cultura de batelada por longos períodos sem a adição de nutrientes.[16][17] Ao fornecer água destilada estéril para manter o volume e a osmolaridade, as culturas cultivadas aerobicamente podem ser mantidas em densidades de ~106 unidades formadoras de colônias (UFCs) por ml por mais de 5 anos sem a adição de nutrientes em cultura de batelada.[18]
Condições ambientais
Fatores ambientais influenciam a taxa de crescimento bacteriano, tais como acidez (pH), temperatura, atividade de água, macro e micronutrientes, níveis de oxigênio e toxinas. As condições tendem a ser relativamente consistentes entre as bactérias, com exceção dos extremófilos. As bactérias possuem condições ideais de crescimento sob as quais prosperam, mas, uma vez fora dessas condições, o estresse pode resultar em crescimento reduzido ou estagnado, dormência (como a formação de esporos) ou morte. Manter condições de crescimento subótimas é um princípio fundamental para a preservação de alimentos.
Temperatura
A maioria dos micróbios cresce melhor em temperaturas moderadas. Manter temperaturas de crescimento subótimas é vital para a preservação de alimentos. Este princípio levou à adoção da refrigeração e de métodos de cozimento completos. Os micróbios são classificados pelas temperaturas em que crescem e prosperam:
- Psicrófilos
Psicrófilos são micróbios extremófilos adaptados a temperaturas mais baixas. A temperatura ideal para o crescimento é entre 0 a 15 graus Celsius.[19] Os psicrófilos são normalmente encontrados em ecossistemas extremamente frios da Terra, como regiões de calotas polares, permafrost, superfícies polares e oceanos profundos. Para sobreviver nesses locais, os psicrófilos devem estar adaptados às baixas temperaturas, bem como às condições ambientais extremas. Algumas adaptações incluem a regulação da fluidez da membrana, síntese de proteínas aclimatadas ao frio e tolerância ao congelamento. No nível enzimático, a desestabilização do sítio ativo ou de toda a proteína permite que a proteína permaneça ativa e flexível em temperaturas que geralmente congelariam o movimento molecular.[20]
- Mesófilos
Mesófilos são nomeados por sua preferência em crescer em temperaturas moderadas, entre 20-45 graus Celsius. Os mesófilos abrangem a maioria dos micróbios. Patógenos que afetam o corpo humano são tipicamente mesófilos, pois crescem melhor na faixa de temperatura moderada do corpo humano.
- Termófilos
Termófilos são micróbios que prosperam em temperaturas mais altas, entre 45-80 graus Celsius. Eles incluem termófilos moderados, que crescem entre 45-70 graus Celsius, e termófilos extremos, que crescem acima de 70 graus Celsius. Os termófilos extremos são frequentemente encontrados em ambientes aquecidos geotermicamente ou vulcanicamente. Os termófilos possuem uma variedade de mecanismos para sobreviver a essas temperaturas. Proteínas de ligação ao DNA compactam o DNA em nucleossomos para maior estabilidade em altas temperaturas. Modificações na membrana são feitas para melhorar a rigidez, como ácidos graxos iso-ramificados. Muitos termófilos têm tamanhos de genoma menores, o que reduz a energia necessária para a divisão celular.
Acidez
A acidez ideal para as bactérias tende a ser em torno de pH 6,5 a 7,0 (neutro); aquelas que vivem em pH menor são acidófilas e em pH maior são alcalófilas. Algumas bactérias podem alterar o pH, como por exemplo, excretando ácido, resultando em condições subótimas.[21]
Atividade de água
As condições ambientais que afetam o crescimento microbiano são normalmente estudadas individualmente. No entanto, as condições de temperatura e umidade estão frequentemente ligadas. Independentemente das condições de temperatura, as taxas de crescimento bacteriano diminuem em níveis mais baixos de umidade do solo.[22]
Oxigênio
As bactérias podem ser aeróbias ou anaeróbias. Dependendo do grau de oxigênio necessário, as bactérias podem se enquadrar nas seguintes classes:
- Anaeróbios facultativos (ou aerotolerantes): ausência ou mínimo de oxigênio necessário para seu crescimento.
- Anaeróbios obrigatórios: crescem apenas na ausência completa de oxigênio.
- Aeróbios facultativos: podem crescer tanto na presença quanto no mínimo de oxigênio.
- Aeróbios obrigatórios: crescem apenas na presença de oxigênio.
Micronutrientes
Os micróbios precisam de nutrientes suficientes para o crescimento. Os micronutrientes necessários para o crescimento microbiano incluem zinco, cobre, manganês e ferro. Embora os micronutrientes normalmente não sejam um fator limitante para o crescimento microbiano na natureza, eles atuam como cofatores e auxiliam as enzimas.[23] Os requisitos nutricionais variam conforme a espécie microbiana. Por exemplo, as diatomáceas requerem vitaminas do complexo B, como a B12, para a síntese de aminoácidos e metionina sintase. Embora os micronutrientes sejam necessários em quantidades adequadas para o crescimento e eficiência, o excesso de micronutrientes pode ser prejudicial ao crescimento microbiano.
Compostos tóxicos
Compostos tóxicos como o etanol podem dificultar o crescimento ou matar bactérias. Isso é usado beneficially para desinfecção e na conservação de alimentos.
Ver também
- Equação de Monod
- Cinética de Michaelis-Menten
- Proliferação celular
Referências
- ↑ Fernández-Martínez, LT; Javelle, A; Hoskisson, PA (fevereiro 2024). «Microbial Primer: Bacterial growth kinetics». Microbiology. 170 (2). 001428 páginas. PMC 10924458
 . PMID 38329407. doi:10.1099/mic.0.001428
. PMID 38329407. doi:10.1099/mic.0.001428
- 1 2 Skarstad, K; Steen, HB; Boye, E (1983). «Cell cycle parameters of slowly growing Escherichia coli B/r studied by flow cytometry». J. Bacteriol. 154 (2): 656–62. PMC 217513
 . PMID 6341358. doi:10.1128/jb.154.2.656-662.1983
. PMID 6341358. doi:10.1128/jb.154.2.656-662.1983 - ↑ Zwietering, MH; Jongenburger, I; Rombouts, FM; van 'T Riet, K (1990). «Modeling of the Bacterial Growth Curve». Applied and Environmental Microbiology. 56 (6): 1875–1881. Bibcode:1990ApEnM..56.1875Z. PMC 184525
 . PMID 16348228. doi:10.1128/aem.56.6.1875-1881.1990
. PMID 16348228. doi:10.1128/aem.56.6.1875-1881.1990 - ↑ Fankhauser DB (17 de julho de 2004). «Bacterial Growth Curve». University of Cincinnati Clermont College. Consultado em 29 de dezembro de 2015. Cópia arquivada em 13 de fevereiro de 2016
- ↑ Case C, Funke B, Tortora G (2010). Microbiology An Introduction Tenth ed. [S.l.]: Pearson Benjamin Cummings. ISBN 978-0-321-55007-1
- 1 2 «Bacterial Growth». BACANOVA project. European Commission. Consultado em 7 de maio de 2008. Cópia arquivada em 24 de outubro de 2007
- ↑ Coutts DA (15 de dezembro de 2011). «Marshall T. Savage - An Exponentialist View». Famous Exponentialists. Exponentialist homepage
- 1 2 Bridges BA, Foster PL, Timms AR (2001). «Effect of endogenous carotenoids on "adaptive" mutation in Escherichia coli FC40». Mutat. Res. 473 (1): 109–19. Bibcode:2001MRFMM.473..109B. PMC 2929247
 . PMID 11166030. doi:10.1016/s0027-5107(00)00144-5
. PMID 11166030. doi:10.1016/s0027-5107(00)00144-5 - ↑ Samorodnitsky, Dan (5 de junho de 2024). «Most Life on Earth is Dormant, After Pulling an 'Emergency Brake'». Quanta Magazine (em inglês). Consultado em 12 de junho de 2024
- ↑ Novick A (1955). «Growth of Bacteria». Annual Review of Microbiology. 9: 97–110. PMID 13259461. doi:10.1146/annurev.mi.09.100155.000525
- ↑ Anagnostopoulos C, Spizizen J (1961). «Requirements for Transformation in Bacillus Subtilis». J. Bacteriol. 81 (5): 741–6. Bibcode:1961JBact..81..741A. PMC 279084
 . PMID 16561900. doi:10.1128/JB.81.5.741-746.1961
. PMID 16561900. doi:10.1128/JB.81.5.741-746.1961 - ↑ Monod, Jacques (1941). Recherches sur la crescimento des cultures bactériennes (em francês). Paris: Hermann
- ↑ Monod, Jacques (1945). «Sur la nature du fenômeno de diauxie». Annales de l'Institut Pasteur (em francês). 71: 37–40
- ↑ Mockaitis, Gustavo (2026). «Mono- and Polyauxic Growth Kinetics: A Semi-Mechanistic Framework for Complex Biological Dynamics». Bulletin of Mathematical Biology. 88. 55 páginas. arXiv:2507.05960
 . doi:10.1007/s11538-026-01621-7
. doi:10.1007/s11538-026-01621-7
- ↑ Mockaitis, Gustavo (2026). «Polyauxic Modeling Platform v1.0.0 (Streamlit)». doi:10.5281/zenodo.18025828
- ↑ Steinhaus EA, Birkeland JM (setembro de 1939). «Studies on the Life and Death of Bacteria: I. The Senescent Phase in Aging Cultures and the Probable Mechanisms Involved». Journal of Bacteriology. 38 (3): 249–261. PMC 374517
 . PMID 16560248. doi:10.1128/jb.38.3.249-261.1939
. PMID 16560248. doi:10.1128/jb.38.3.249-261.1939 - ↑ Finkel SE, Kolter R (março de 1999). «Evolution of microbial diversity during prolonged starvation». Proceedings of the National Academy of Sciences of the United States of America. 96 (7): 4023–4027. Bibcode:1999PNAS...96.4023F. PMC 22413
 . PMID 10097156. doi:10.1073/pnas.96.7.4023
. PMID 10097156. doi:10.1073/pnas.96.7.4023
- ↑ Finkel SE (fevereiro de 2006). «Long-term survival during stationary phase: evolution and the GASP phenotype». Nature Reviews. Microbiology. 4 (2): 113–120. PMID 16415927. doi:10.1038/nrmicro1340
- ↑ Feller, Georges; Gerday, Charles (dezembro de 2003). «Psychrophilic enzymes: hot topics in cold adaptation». Nature Reviews Microbiology (em inglês). 1 (3): 200–208. ISSN 1740-1534. doi:10.1038/nrmicro773 Verifique o valor de
|url-access=subscription(ajuda) - ↑ Somayaji, Adithi; Dhanjal, Chetan Roger; Lingamsetty, Rathnamegha; Vinayagam, Ramesh; Selvaraj, Raja; Varadavenkatesan, Thivaharan; Govarthanan, Muthusamy (1 de outubro de 2022). «An insight into the mechanisms of homeostasis in extremophiles». Microbiological Research. 263. ISSN 0944-5013. PMID 35868258. doi:10.1016/j.micres.2022.127115 Verifique o valor de
|url-access=subscription(ajuda) - ↑ Blamire J. «Effect of pH on Growth Rate». Brooklyn College. Consultado em 8 de outubro de 2016
- ↑ Cruz-Paredes, Carla; Tájmel, Dániel; Rousk, Johannes (1 de maio de 2021). «Can moisture affect temperature dependences of microbial growth and respiration?». Soil Biology and Biochemistry. 156. Bibcode:2021SBiBi.15608223C. ISSN 0038-0717. doi:10.1016/j.soilbio.2021.108223

- ↑ Merchant, Sabeeha S.; Helmann, John D. (2012), «Elemental Economy», ISBN 978-0-12-398264-3, Elsevier, Advances in Microbial Physiology (em inglês), 60, pp. 91–210, PMC 4100946
 , doi:10.1016/b978-0-12-398264-3.00002-4
, doi:10.1016/b978-0-12-398264-3.00002-4