Pasireotide
Pasireotide
| |||||||||
|---|---|---|---|---|---|---|---|---|---|
 | |||||||||
| Nomes | |||||||||
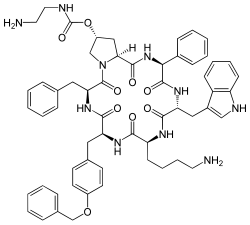
| Nome IUPAC | [(3S,6S,9S,12R,15S,18S,20R)-9-(4-aminobutyl)-3-benzyl-12-(1H-indol-3-ylmethyl)-2,5,8,11,14,17-hexaoxo-15-phenyl-6-[(4-phenylmethoxyphenyl)methyl]-1,4,7,10,13,16-hexazabicyclo[16.3.0]henicosan-20-yl] N-(2-aminoethyl)carbamate | ||||||||
| Outros nomes | SOM230 | ||||||||
| |||||||||
| |||||||||
| |||||||||
| Página de dados suplementares | |||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||
Pasireotide é um fármaco da Novartis de marca comercial Signifor. Foi aprovado para ser utilizado no tratamento da doença de Cushing pelo FDA em dezembro de 2012.[1] Nos estudos clínicos de fase III mostrou que a maioria dos pacientes testados conseguiu reduzir os níveis de cortisol na urina.[2]
Notas e referências
- ↑ UOL. Fármaco da Novartis Signifor® obtém aprovação da FDA como primeiro medicamento para trata síndrome de Cushing, distúrbio endócrino grave. Acesso em 18 de dezembro de 2012.
- ↑ RCM Pharma. «Fármaco experimental para a Novartis revela-se eficaz na doença de Cushing». Consultado em 22 de setembro de 2010