Fenacetina
Fenacetina
| |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||
| Nomes | |||||||||||||
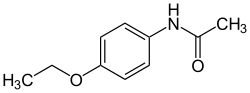
| Nome IUPAC | N-(4-etoxifenil)etanamida | ||||||||||||
| Outros nomes | 1-Acetamino-4-etoxibenzeno p-Etoxiacetanilida Acetofenetidina | ||||||||||||
| |||||||||||||
| |||||||||||||
| |||||||||||||
| |||||||||||||
| |||||||||||||
| Página de dados suplementares | |||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||
A fenacetina (acetofetidin, N-(4-etoxifenil)acetamida[2]) é um medicamento aliviador da dor e redutor da febre, que foi amplamente usado após sua introdução em 1887. Foi retirada do uso medicinal como perigosa a partir da década de 1970 (por exemplo, retirada no Canadá em 1973,[3] e pela Agência de Administração de Alimentos e Medicamentos dos Estados Unidos em 1983[4]).
História
A fenacetina foi introduzida em 1887 em Elberfeld, Alemanha pela empresa alemã Bayer, e foi usada principalmente como analgésico; foi um dos primeiros redutores sintéticos da febre a chegar ao mercado. É também historicamente conhecida por ser um dos primeiros analgésicos não-opioides sem propriedades anti-inflamatórias. Embora o paracetamol (acetaminofeno) tenha sido produzido anteriormente, um acidente histórico fez com que fosse ignorado após a avaliação de Joseph von Mering em 1893.[5]
Antes da Primeira Guerra Mundial, a Grã-Bretanha importava fenacetina da Alemanha.[6] Durante a guerra, uma equipe incluindo Jocelyn Field Thorpe e Martha Annie Whiteley desenvolveu uma síntese na Grã-Bretanha.[6]
Mecanismo de ação conhecido
Os efeitos analgésicos da fenacetina são devidos às suas ações nos tratos sensoriais da medula espinhal. Além disso, a fenacetina tem uma ação depressora no coração, onde atua como um inótropo negativo. É um antipirético, atuando no cérebro para diminuir o ponto de ajuste da temperatura. É também usada para tratar artrite reumatoide (tipo subaguda) e neuralgia intercostal.
In vivo, uma de duas reações ocorre. Usualmente o éter da fenacetina é clivado para deixar paracetamol (acetaminofeno), que é o analgésico clinicamente relevante. Uma minoria das vezes o grupo acetil é removido da amina, produzindo p-fenetidina carcinogênica. Esta reação é bastante rara, no entanto, como evidenciado pelo fato de que o medicamento esteve no mercado por quase 100 anos antes que uma ligação estatística fosse estabelecida, quando o Canadá, seguido pelos Estados Unidos, a retirou do mercado.
Preparação
A primeira síntese foi relatada em 1878 por Harmon Northrop Morse. O artigo citado de Morse descreve a síntese do paracetamol a partir do 4-aminofenol e ácido acético.[7]
A fenacetina pode ser sintetizada como um exemplo da síntese do éter de Williamson: iodeto de etila, paracetamol, e carbonato de potássio anidro são aquecidos em 2-butanona para dar o produto bruto, que é recristalizado a partir da água.[8]
Usos
Médico
A fenacetina foi amplamente usada até o terceiro quarto do século vinte, muitas vezes na forma de um A.P.C., ou composto analgésico "aspirina-fenacetina-cafeína", como um remédio para febre e dor. Uma formulação inicial (1919) foi o APC de Vincent na Austrália.
Nos Estados Unidos, a Agência de Administração de Alimentos e Medicamentos ordenou a retirada de medicamentos contendo fenacetina em novembro de 1983, devido às suas propriedades carcinogênicas e danosas aos rins.[9] Foi também banida na Índia.[10] Como resultado, algumas preparações de marca, e previamente baseadas em fenacetina, continuaram a ser vendidas, mas com a fenacetina substituída por alternativas mais seguras. Uma marca popular de fenacetina era Saridon da Roche, que foi reformulada em 1983 para conter propilfenazona, paracetamol e cafeína. Coricidin foi também reformulada sem fenacetina. O paracetamol é um metabólito da fenacetina com efeitos analgésicos e antipiréticos similares, mas a nova formulação não foi encontrada como tendo a carcinogenicidade da fenacetina.
Outros
A fenacetina tem sido usada como um agente de corte para adulterar cocaína no Reino Unido e Canadá, devido às propriedades físicas similares.[11] Lá, recebeu o apelido de "mágica".
Devido ao seu baixo custo, a fenacetina é usada para pesquisa sobre as propriedades físicas e refrativas de cristais. É um composto ideal para este tipo de pesquisa.[2][12]
No Canadá, a fenacetina é usada como um reagente de laboratório, e em algumas preparações de tintura de cabelo (como um estabilizador para peróxido de hidrogênio). Embora seja considerada um medicamento de prescrição, nenhum medicamento comercializado contém fenacetina.[13]
Segurança
A fenacetina, e produtos contendo fenacetina, têm sido mostrados em um modelo animal como tendo o efeito colateral e pós-efeito de carcinogênese. Em humanos, muitos relatos de casos implicaram produtos contendo fenacetina em neoplasmas uroteliais, especialmente carcinoma urotelial da pelve renal. A fenacetina é classificada pela Agência Internacional para Pesquisa do Câncer (IARC) como carcinogênica para humanos.[2] Em uma série prospectiva, a fenacetina foi associada com um risco aumentado de morte devido a doenças urológicas ou renais, morte devido a cânceres, and morte devido a doenças cardiovasculares.[14] Além disso, pessoas com deficiência de glicose-6-fosfato desidrogenase podem experimentar hemólise aguda, ou dissolução de células sanguíneas, enquanto tomam este medicamento. A hemólise aguda é possível no caso de pacientes que desenvolvem uma resposta IgM à fenacetina levando a complexos imunes que se ligam aos eritrócitos no sangue. Os eritrócitos são então lisados quando os complexos ativam o sistema complemento.
O uso crônico da fenacetina é conhecido por levar à nefropatia analgésica caracterizada por necrose papilar renal.[15][16][17] Esta é uma condição que resulta na destruição de algumas ou todas as papilas renais nos rins. Acredita-se que o metabólito p-fenetidina seja pelo menos parcialmente responsável por esses efeitos.[18]
Uma morte notável que pode possivelmente ser atribuída ao uso desta droga foi a do pioneiro da aviação Howard Hughes. Ele havia estado usando fenacetina extensivamente para o tratamento de dor crônica; foi declarado durante sua autópsia que o uso de fenacetina pode ter sido a causa de sua insuficiência renal.[19]
Askit Powders, uma cura para dor de cabeça anteriormente popular no mercado do Reino Unido, foram associados com insuficiência renal em usuários crônicos devido ao conteúdo de fenacetina até 1966, quando foram reformulados para removê-la.[20]
Na cultura popular
Um episódio de 1974 da série da Yorkshire Television Justice, "Duty of Care", apresenta um caso judicial que resultou de uma mulher morrer de envenenamento por fenacetina, como resultado de tomar A.P.C. por cinco anos. Isso explicou que a fenacetina causou necrose papilar renal.[21]
No livro Zen and the Art of Motorcycle Maintenance capítulo 4, "APCs for headaches" está incluído em uma lista de coisas valiosas para levar em viagens de motocicleta.[22]
Veja também
Referências
- ↑ Registo de Phenacetin na Base de Dados de Substâncias GESTIS do IFA.
- ↑ a b c Gralak B, Enoch S, Tayeb G (junho de 2000). «Anomalous refractive properties of photonic crystals». Journal of the Optical Society of America A. 17 (6): 1012–1020. Bibcode:2000JOSAA..17.1012G. CiteSeerX 10.1.1.462.8012
 . PMID 10850471. doi:10.1364/JOSAA.17.001012
. PMID 10850471. doi:10.1364/JOSAA.17.001012
- ↑ «Phenacetin». DrugBank. Consultado em 28 de abril de 2020
- ↑ «Drugs withdrawn from the market containing phenacetin» (PDF). Department of Health and Human Services - FDA. 5 de outubro de 1983
- ↑ Sneader W (2005). Drug Discovery: A History. Hoboken, NJ: Wiley. p. 439. ISBN 978-0471899808.
The eminent clinical pharmacologist Joseph von Mering collaborated with the Bayer Company in a trial of paracetamol in 1893. He found it to be an effective antipyretic and analgesic, but claimed it had a slight tendency to produce metemoglobinemia. This could conceivably have been caused by the contamination of his paracetamol with the 4-aminophenol from which it was synthesised.
- ↑ a b Creese MR (1997). «Martha Annie Whiteley (1866-1956): Chemist and Editor» (PDF). Bulletin for the History of Chemistry. 8 (20): 42–45. doi:10.70359/bhc1997n20p042
- ↑ Morse HN (1878). «Ueber eine neue Darstellungsmethode der Acetylamidophenole». Berichte der deutschen chemischen Gesellschaft. 11 (1): 232–233. doi:10.1002/cber.18780110151
- ↑ «Conversion of Acetaminophen into Phenacetin». Chemistry Department Master Experiment Archive. California State University Stanislaus
- ↑ Federal Register de 5 de outubro de 1983 (48 FR 45466)
- ↑ «Drugs banned in India». Central Drugs Standard Control Organization, Dte.GHS, Ministry of Health and Family Welfare, Government of India. Consultado em 17 de setembro de 2013
- ↑ «Cancer chemical in street cocaine». BBC News. 23 de novembro de 2006
- ↑ Studenikin PA, Zagumennyi AI, Zavartsev YD, Popov PA, Shcherbakov IA (1995). «GdVO4as a new medium for solid-state lasers: Some optical and thermal properties of crystals doped with Cd3+, Tm3+, and Er3+ions». Quantum Electronics. 25 (12): 1162–1165. doi:10.1070/QE1995v025n12ABEH000556
- ↑ «Health - Product safety - Chemical substances - Phenacetin information sheet». Government of Canada -. 18 de abril de 2017. Consultado em 29 de abril de 2020
- ↑ Dubach UC, Rosner B, Stürmer T (janeiro de 1991). «An epidemiologic study of abuse of analgesic drugs. Effects of phenacetin and salicylate on mortality and cardiovascular morbidity (1968 to 1987)». The New England Journal of Medicine. 324 (3): 155–160. PMID 1984193. doi:10.1056/NEJM199101173240304

- ↑ Cochran AJ, Lawson DH, Linton AL (julho de 1967). «Renal papillary necrosis following phenacetin excess». Scottish Medical Journal. 12 (7): 246–250. PMID 6036245. doi:10.1177/003693306701200702
- ↑ Tan GH, Rabbino MD, Hopper J (agosto de 1964). «Is Phenacetin a Nephrotoxin?: A Report on Twenty-three Users of the Drug». California Medicine. 101 (2): 73–77. PMC 1515485
 . PMID 14180501
. PMID 14180501
- ↑ Brix AE (2002). «Renal papillary necrosis». Toxicologic Pathology. 30 (6): 672–674. PMID 12512867. doi:10.1080/01926230290166760

- ↑ Kankuri E, Solatunturi E, Vapaatalo H (junho de 2003). «Effects of phenacetin and its metabolite p-phenetidine on COX-1 and COX-2 activities and expression in vitro». Thrombosis Research. 110 (5–6): 299–303. PMID 14592552. doi:10.1016/S0049-3848(03)00416-X
- ↑ Tennant F (julho–agosto de 2007). «Howard Hughes & Pseudoaddiction» (PDF). Practical Pain Management. 7 (6): 20. Consultado em 2 de novembro de 2015.
The phenacetin in the codeine compound produced, over time, kidney failure and death.
- ↑ «Taggart star's Askit questions over mother's death». BBC News. 9 de janeiro de 2018
- ↑ Duty of Care. Justice. Yorkshire Television. 31 May 1974.
- ↑ Pirsig, Robert M. (1985). Zen and the Art of Motorcycle Maintenance 82ª impressão ed. [S.l.]: Bantam. p. 35
Ligações externas
- Relatório de carcinógeno do NIH
- Relatório IARC
- Dados de segurança (MSDS) para fenacetina Arquivado em 2006-09-24 no Wayback Machine