Epilepsia pós-traumática
| Epilepsia pós-traumática | |
|---|---|
| Especialidade | Neurologia |
| Classificação e recursos externos | |
| eMedicine | 1184178 |
| MeSH | D004834 |
Epilepsia pós-traumática (EPT) é uma forma de epilepsia adquirida que resulta de lesão cerebral causada por trauma físico ao cérebro (traumatismo cranioencefálico, abreviado TCE).[1] Uma pessoa com EPT sofre crises crises pós-traumáticas (CPT, crises resultantes de TCE) recorrentes mais de uma semana após a lesão inicial.[2] Estima-se que a EPT constitua 5% de todos os casos de epilepsia e mais de 20% dos casos de epilepsia adquirida[3][4][1] (em que as crises são causadas por uma condição cerebral orgânica identificável).[5]
Não se sabe quem desenvolverá epilepsia após um TCE e quem não desenvolverá.[6] No entanto, a probabilidade de uma pessoa desenvolver EPT é influenciada pela gravidade e tipo da lesão; por exemplo, traumas penetrantes [en] e aquelas que envolvem sangramento intracerebral apresentam maior risco. O início da EPT pode ocorrer logo após o trauma físico que a causa, ou meses, até anos depois.[3] Indivíduos com trauma craniano podem permanecer em maior risco de crises pós-traumáticas do que a população geral mesmo décadas após a lesão.[7] A EPT pode ser desencadeada por diversos processos bioquímicos que ocorrem no cérebro após o trauma, incluindo a sobreexcitação de neurônios e danos aos tecidos cerebrais por radicais livres.[8]
Medidas diagnósticas incluem eletroencefalografia (EEG) e técnicas de imagem cerebral, como ressonância magnética, embora estas não sejam totalmente confiáveis. Medicamentos antiepilépticos não previnem o desenvolvimento de EPT após lesão craniana, mas podem ser usados para tratar a condição se ela ocorrer. Quando a medicação não controla as crises, pode ser necessária cirurgia.[9] Técnicas cirúrgicas modernas para EPT têm origem no século XIX, mas a trepanação (corte no crânio para criar um orifício) pode ter sido usada para a condição em culturas antigas.[10]
Classificação
Crises podem ocorrer após um traumatismo cranioencefálico; estas são conhecidas como crises pós-traumáticas (CPT). No entanto, nem todos que têm crises pós-traumáticas continuarão a ter epilepsia pós-traumática, pois esta é uma condição crônica. Ainda assim, os termos CPT e EPT são usados indistintamente na literatura médica.[11][12] As crises devido à epilepsia pós-traumática diferenciam-se das crises pós-traumáticas não epilépticas com base em sua causa e tempo após o trauma. Uma pessoa com EPT tem crises tardias, aquelas que ocorrem mais de uma semana após o trauma inicial.[13] Crises tardias são consideradas não provocadas, enquanto crises precoces (que ocorrem dentro de uma semana do trauma) são vistas como resultado direto dos efeitos da lesão. Uma crise provocada resulta de uma causa excepcional e não recorrente, como os efeitos imediatos do trauma, e não de um defeito no cérebro; ela não indica epilepsia.[14] Assim, para um diagnóstico de EPT, as crises devem ser não provocadas.
Há discordância sobre se a EPT deve ser definida como a ocorrência de uma ou mais crises tardias não provocadas, ou se o diagnóstico deve ser restrito a pessoas com duas ou mais crises.[15] Fontes médicas geralmente consideram a EPT presente se ocorrer ao menos uma crise não provocada, mas recentemente tornou-se aceito restringir a definição de todos os tipos de epilepsia a condições em que ocorrem mais de uma crise.[11] Exigir mais de uma crise para o diagnóstico de EPT alinha-se mais com a definição moderna de epilepsia, mas exclui pessoas cujas crises são controladas por medicação após a primeira ocorrência.[11]
Como em outras formas de epilepsia, os tipos de crises na EPT podem ser focais (afetando apenas parte de um hemisfério cerebral) ou generalizadas (afetando ambos os hemisférios e associadas à perda de consciência).[16] Em cerca de um terço dos casos, pessoas com EPT têm crises parciais; estas podem ser simples ou complexas.[17] Em crises parciais simples, o nível de consciência não é alterado, enquanto em crises parciais complexas a consciência é prejudicada.[14] Quando ocorrem crises generalizadas, elas podem começar como crises parciais e depois se espalhar, tornando-se generalizadas.[17]
Causas
Não está claro por que alguns pacientes desenvolvem EPT enquanto outros com lesões muito semelhantes não desenvolvem.[11] Contudo, possíveis fatores de risco foram identificados, incluindo gravidade e tipo de lesão, presença de crises precoces e fatores genéticos.
Genética
A genética pode desempenhar um papel no risco de uma pessoa desenvolver EPT; indivíduos com o alelo ApoE-ε4 podem ter maior risco de EPT.[7] O alelo haptoglobina Hp2-2 pode ser outro fator de risco genético, possivelmente porque se liga mal à hemoglobina, permitindo que mais ferro escape e danifique os tecidos.[7] No entanto, a maioria dos estudos concluiu que ter familiares com epilepsia não aumenta significativamente o risco de CPT,[11] sugerindo que a genética não é um fator de risco forte.
Gravidade do trauma
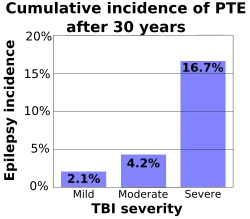
Quanto mais grave o trauma cerebral, maior a probabilidade de uma pessoa ter EPT tardia.[19] Evidências sugerem que lesões cranianas leves não aumentam o risco de desenvolver EPT, enquanto tipos mais graves aumentam.[20] Em TCE leve simples, o risco de EPT é cerca de 1,5 vez maior que na população não lesionada.[18] Algumas estimativas indicam que até metade dos indivíduos com trauma cerebral grave sofre EPT;[19] outras estimativas colocam o risco em 5% para todos os pacientes com TCE e 15–20% para TCE grave.[21] Um estudo descobriu que o risco em 30 anos de desenvolver EPT foi de 2,1% para TCE leve, 4,2% para moderada e 16,7% para lesões graves, conforme mostrado no gráfico à direita.[18][22]
Natureza do trauma
A natureza do trauma craniano também influencia o risco de EPT. Pessoas com fratura de crânio deprimida [en], trauma craniano penetrante [en], CPT precoces e hematomas intracerebrais e subdurais devido à TCE são especialmente propensas a ter EPT, que ocorre em mais de 30% das pessoas com qualquer um desses achados.[19] Cerca de 50% dos pacientes com trauma craniano penetrante desenvolvem EPT,[8][20] e lesões por mísseis e perda de volume cerebral estão associadas a uma probabilidade particularmente alta de desenvolver a condição.[23] Lesões que ocorrem em ambientes militares apresentam risco acima do usual para EPT, provavelmente porque envolvem mais comumente lesões cerebrais penetrantes e danos cerebrais mais disseminados.[7] Hematomas intracranianos, em que o sangue se acumula dentro do crânio, são um dos fatores de risco mais importantes para EPT.[24] Hematomas subdurais conferem um risco maior de EPT do que hematomas epidurais, possivelmente porque causam mais danos ao tecido cerebral.[8] Cirurgias intracranianas repetidas conferem alto risco para EPT tardia, possivelmente porque pessoas que precisam de mais cirurgias têm maior probabilidade de apresentar fatores associados a traumas cerebrais graves, como hematomas grandes ou edema cerebral.[8] Além disso, as chances de desenvolver EPT variam conforme a localização da lesão cerebral: uma contusão cerebral em um dos lobos frontais tem risco de 20% para EPT, enquanto uma contusão em um dos lobos parietais tem risco de 19% e em um lobo temporal, 16%.[22] Quando ocorrem contusões em ambos os hemisférios, o risco é de 26% para os lobos frontais, 66% para os parietais e 31% para os temporais.[22]
Crises pós-traumáticas
O risco de uma pessoa desenvolver EPT é aumentado, mas não garantido, se ocorrerem CPTs.[20] Como muitos dos fatores de risco para EPT e CPT precoces são os mesmos, não se sabe se a ocorrência de CPT é um fator de risco por si só.[7] No entanto, mesmo independentemente de outros fatores de risco comuns, CPT precoces aumentam o risco de EPT para mais de 25% na maioria dos estudos.[4] Uma pessoa que tem uma crise tardia está em risco ainda maior de ter outra do que alguém com CPT precoce; a epilepsia ocorre em 80% das pessoas que têm uma crise tardia.[25] O estado de mal epiléptico, uma crise contínua ou múltiplas crises em rápida sucessão, é especialmente correlacionado com o desenvolvimento de EPT; crises de estado ocorrem em 6% de todos os TCEs, mas estão associadas a EPT em 42% dos casos, e interromper rapidamente uma crise de estado reduz as chances de desenvolvimento de EPT.[22]
Fisiopatologia
Por razões desconhecidas, o trauma pode causar mudanças no cérebro que levam à epilepsia.[3][26] Existem vários mecanismos propostos pelos quais o TCE causa EPT, podendo mais de um estar presente em uma mesma pessoa.[8] No período entre uma lesão cerebral e o início da epilepsia, as células cerebrais podem formar novas sinapses e axônios, sofrer apoptose ou necrose e experimentar alterações na expressão gênica.[25] Além disso, danos a áreas particularmente vulneráveis do córtex, como o hipocampo, podem originar EPT.[4]
Sangue que se acumula no cérebro após uma lesão pode danificar o tecido cerebral e, assim, causar epilepsia.[8] Produtos resultantes da degradação da hemoglobina do sangue podem ser tóxicos ao tecido cerebral.[8] A "hipótese do ferro" sugere que a EPT é devido a danos por radicais livres de oxigênio, cuja formação é catalisada pelo ferro do sangue.[19] Experimentos com ratos mostraram que crises epilépticas podem ser produzidas injetando ferro no cérebro.[8] O ferro catalisa a formação de radicais hidroxila pela reação de Haber-Weiss;[8] esses radicais livres danificam as células cerebrais por peroxidação de lipídios em suas membranas.[27] O ferro do sangue também reduz a atividade de uma enzima chamada óxido nítrico sintase, outro fator pensado para contribuir com a EPT.[19]
Após o TCE, existem anormalidades na liberação de neurotransmissores, substâncias químicas usadas pelas células cerebrais para se comunicarem; essas anormalidades podem desempenhar um papel no desenvolvimento da EPT.[8] A TCE pode levar à liberação excessiva de glutamato e outros neurotransmissores excitatórios (aqueles que estimulam as células cerebrais e aumentam a probabilidade de que elas disparem). Essa liberação excessiva de glutamato pode levar à excitotoxicidade, dano às células cerebrais por superativação dos receptores bioquímicos que se ligam e respondem a neurotransmissores excitatórios. A superativação de receptores de glutamato danifica neurônios; por exemplo, leva à formação de radicais livres.[8] A excitotoxicidade é um possível fator no desenvolvimento da EPT;[13] ela pode levar à formação de um foco epileptogênico crônico.[8] Um foco epiléptico é a parte do cérebro de onde originam-se as descargas epilépticas.[28]
Além de mudanças químicas nas células, mudanças estruturais que levam à epilepsia podem ocorrer no cérebro.[3] Crises que ocorrem logo após o TCE podem reorganizar redes neurais e causar crises recorrentes e espontâneas posteriormente.[4] A hipótese do kindling sugere que novas conexões neurais são formadas no cérebro e causam um aumento na excitabilidade.[19] A palavra kindling é uma metáfora: a maneira como a resposta do cérebro a estímulos aumenta com exposições repetidas é semelhante ao modo como pequenos gravetos em chamas podem produzir um grande fogo.[29] Essa reorganização de redes neurais pode torná-las mais excitáveis.[4] Neurônios em um estado hiperexcitável devido ao trauma podem criar um foco epiléptico no cérebro que leva a crises.[12] Além disso, um aumento na excitabilidade dos neurônios pode acompanhar a perda de neurônios inibitórios que normalmente reduzem a probabilidade de outros neurônios dispararem; essas mudanças também podem produzir EPT.[4]
Diagnóstico
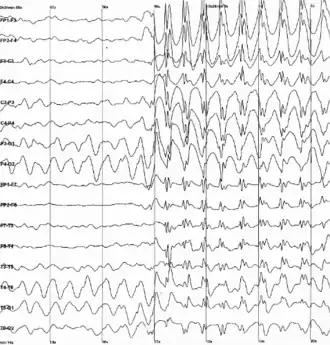
Para ser diagnosticado com EPT, uma pessoa deve ter histórico de trauma craniano e nenhum histórico de crises antes da lesão.[30] Testemunhar uma crise é a maneira mais eficaz de diagnosticar EPT.[12] A eletroencefalografia (EEG) é uma ferramenta usada para diagnosticar um transtorno convulsivo, mas uma grande porção de pessoas com EPT pode não apresentar os achados "epileptiformes" anormais indicativos de epilepsia.[12] Em um estudo, cerca de um quinto das pessoas que tiveram EEGs normais três meses após uma lesão desenvolveram EPT posteriormente. No entanto, embora o EEG não seja útil para prever quem desenvolverá EPT, ele pode ser útil para localizar o foco epiléptico, determinar a gravidade e prever se uma pessoa terá mais crises se parar de tomar medicamentos antiepilépticos.[8]
A ressonância magnética (RM) é realizada em pessoas com EPT, e a tomografia computadorizada pode ser usada para detectar lesões cerebrais se a RM não estiver disponível.[8] Contudo, frequentemente não é possível detectar o foco epiléptico usando neuroimagem.[31]
Para um diagnóstico de EPT, as crises não devem ser atribuíveis a outra causa óbvia.[4] Crises que ocorrem após lesão craniana não são necessariamente devido à epilepsia ou mesmo ao trauma craniano.[11] Como qualquer pessoa, sobreviventes de TCE podem ter crises devido a fatores como desequilíbrios de fluidos ou eletrólitos, epilepsia de outras causas, hipóxia (oxigênio insuficiente) e isquemia (fluxo sanguíneo insuficiente ao cérebro).[11] A retirada de álcool é outra causa poptencial de crises.[32] Assim, esses fatores devem ser descartados como causas de crises em pessoas com lesão craniana antes que um diagnóstico de EPT possa ser feito.
Prevenção
A prevenção da EPT envolve prevenir o trauma cerebral em geral; medidas de proteção incluem capacetes de bicicleta e assentos de segurança infantil.[8] Não existe tratamento específico para prevenir o desenvolvimento de epilepsia após a ocorrência de TCE.[3] No passado, medicamentos antiepilépticos foram usados com a intenção de prevenir o desenvolvimento de EPT.[3] No entanto, embora os antiepilépticos possam prevenir CPT precoces, estudos clínicos falharam em mostrar que o uso profilático de antiepilépticos previne o desenvolvimento de EPT.[2][3][7][33] Não está claro por que os antiepilépticos em ensaios clínicos falharam em impedir o desenvolvimento de EPT, mas várias explicações foram oferecidas.[7] Os medicamentos podem simplesmente não ser capazes de prevenir a epilepsia, ou os ensaios podem ter sido configurados de forma que não permitiu encontrar um benefício dos medicamentos (por exemplo, os medicamentos podem ter sido administrados tarde demais ou em doses inadequadas).[7] Estudos em animais também falharam em mostrar efeito protetor significativo dos medicamentos anticonvulsivantes mais comumente usados em ensaios de EPT, como fenitoína e carbamazepina.[7] Medicamentos antiepilépticos são recomendados para prevenir crises tardias apenas para pessoas em quem a EPT já foi diagnosticada, não como medida preventiva.[34] Com base nos estudos mencionados, nenhum tratamento é amplamente aceito para prevenir o desenvolvimento de epilepsia.[19] No entanto, foi proposto que existe uma janela estreita de cerca de uma hora após o TCE durante a qual a administração de antiepilépticos poderia prevenir a epileptogênese (o desenvolvimento de epilepsia).[9] Não há evidências que apoiem ou contraindiquem o uso de antiepilépticos para profilaxia de EPT tardia.[35]
Corticosteroides também foram investigados para a prevenção de EPT, mas ensaios clínicos revelaram que os medicamentos não reduziram as CPT tardias e foram, na verdade, associados a um aumento no número de CPT precoces.[3]
Tratamento
Medicamentos antiepilépticos podem ser administrados para prevenir novas crises; esses medicamentos eliminam crises em cerca de 35% das pessoas com EPT.[22] No entanto, os antiepilépticos previnem crises apenas enquanto estão sendo tomados; eles não reduzem a ocorrência uma vez que o paciente para de tomá-los.[2] A medicação pode ser interrompida após as crises estarem controladas por dois anos.[4] A EPT é comumente difícil de tratar com terapia medicamentosa,[3][36] e os antiepilépticos podem estar associados a efeitos colaterais.[34] Os antiepilépticos carbamazepina e valproato são os medicamentos mais comuns usados para tratar EPT; a fenitoína também pode ser usada, mas pode aumentar o risco de efeitos colaterais cognitivos, como pensamento prejudicado.[9] Outros medicamentos comumente usados para tratar EPT incluem clonazepam, fenobarbital, primidona, gabapentina e etossuximida.[12] Entre os antiepilépticos testados para prevenção de crises após TCE (fenitoína, ácido valproico, carbamazepina, fenobarbital), não há evidências de ensaios clínicos randomizados que mostrem superioridade de um sobre outro.[8]
Pessoas cuja EPT não responde à medicação podem passar por cirurgia para remover o foco epileptogênico, a parte do cérebro que está causando as crises.[9] No entanto, a cirurgia para EPT pode ser mais difícil do que para epilepsia de outras causas,[9] e é menos provável que seja útil na EPT do que em outras formas de epilepsia.[8] Pode ser particularmente difícil na EPT localizar o foco epiléptico, em parte porque o TCE pode afetar áreas difusas do cérebro.[31] A dificuldade em localizar o foco convulsivo é vista como um obstáculo à cirurgia.[4] No entanto, para pessoas com esclerose no lobo temporal mesial (na parte interna do lobo temporal), que compõem cerca de um terço das pessoas com EPT intratável, a cirurgia provavelmente terá um bom resultado.[4] Quando há múltiplos focos epilépticos ou o foco não pode ser localizado, e a terapia medicamentosa não é eficaz, a estimulação do nervo vago é outra opção para tratar EPT.[31]
Pessoas com EPT têm visitas de acompanhamento, nas quais os profissionais de saúde monitoram a função neurológica e neuropsicológica e avaliam a eficácia e os efeitos colaterais dos medicamentos.[8] Como em outros tipos de epilepsia, indivíduos com EPT são aconselhados a ter cautela ao realizar atividades nas quais crises poderiam ser particularmente arriscadas, como escalada em rocha.[9]
Prognóstico
O prognóstico para epilepsia devido a trauma é pior do que para epilepsia de causa indeterminada.[20] Pensa-se que pessoas com EPT tenham expectativa de vida mais curta do que pessoas com lesão cerebral sem crises.[12] Comparadas a pessoas com lesões cerebrais estruturais semelhantes, mas sem EPT, as pessoas com EPT levam mais tempo para se recuperar da lesão, têm mais problemas cognitivos e motores e desempenham pior em tarefas cotidianas.[12] Essa descoberta pode sugerir que a EPT é um indicador de uma lesão cerebral mais grave, em vez de uma complicação que por si só piora o resultado.[12] Também foi constatado que a EPT está associada a piores resultados sociais e funcionais, mas não prejudica a reabilitação dos pacientes ou sua capacidade de retornar ao trabalho.[8] No entanto, pessoas com EPT podem ter dificuldade em encontrar emprego se admitirem ter crises, especialmente se o trabalho envolver operar máquinas pesadas.[37]
O período entre uma lesão e o desenvolvimento de epilepsia varia, e não é incomum que uma lesão seja seguida por um período latente sem crises recorrentes.[25] Quanto mais tempo uma pessoa passa sem desenvolver crises, menores são as chances de que a epilepsia se desenvolva.[4] Pelo menos 80–90% das pessoas com EPT têm sua primeira crise dentro de dois anos do TCE.[8] Pessoas sem crises dentro de três anos da lesão têm apenas 5% de chance de desenvolver epilepsia.[38] No entanto, um estudo descobriu que sobreviventes de trauma craniano estão em risco aumentado de EPT até 10 anos após TCE moderado e mais de 20 anos após TCE grave.[7] Como o trauma craniano é bastante comum e a epilepsia pode ocorrer tardiamente após a lesão, pode ser difícil determinar se um caso de epilepsia resultou de um trauma craniano passado ou se o trauma foi incidental.[31]
A questão de por quanto tempo uma pessoa com EPT permanece em maior risco de crises do que a população geral é controversa.[7] Cerca de metade dos casos de EPT entra em remissão, mas casos que ocorrem mais tardiamente podem ter menor chance de fazê-lo.[20]
Epidemiologia
Estudos descobriram que a incidência de EPT varia entre 1,9 e mais de 30% dos indivíduos com TCE, variando conforme a gravidade da lesão e o tempo após o TCE pelo qual os estudos acompanharam os sujeitos.[7]
O trauma cerebral é um dos fatores predisponentes mais fortes para o desenvolvimento de epilepsia e é um fator especialmente importante em adultos jovens.[22] Adultos jovens, que estão em maior risco de lesão craniana, também têm a maior taxa de EPT,[8] que é a maior causa de casos de epilepsia de início recente em jovens.[39] Crianças têm um risco menor de desenvolver epilepsia; 10% das crianças com TCE grave e 16–20% dos adultos com lesões semelhantes desenvolvem EPT.[22] Ter mais de 65 anos também é um fator preditivo no desenvolvimento de epilepsia após trauma cerebral.[25] Um estudo descobriu que a EPT é mais comum em sobreviventes de TCE do sexo masculino do que em mulheres.[12]
História
Registros de EPT existem desde 3000 a.C.[37] A trepanação, na qual um orifício é cortado no crânio, pode ter sido usada para tratar EPT em culturas antigas.[10] No início do século XIX, os cirurgiões Baron Larrey e WC Wells relataram cada um ter realizado a operação para EPT.[10] O cirurgião americano de origem francesa Benjamin Winslow Dudley (1785–1870) realizou seis trepanações para EPT entre 1819 e 1832 em Kentucky e obteve bons resultados apesar da indisponibilidade de antissepsia.[40] A cirurgia envolvia abrir o crânio no local da lesão, debridar tecido lesionado e, às vezes, drenar sangue ou fluido de sob a dura-máter.[40] O trabalho de Dudley foi a maior série do tipo realizada até aquele momento e incentivou outros cirurgiões a usar a trepanação para crises pós-traumáticas.[40] Seus relatórios sobre as operações vieram antes de ser aceito que a cirurgia para aliviar a pressão excessiva dentro do crânio era eficaz no tratamento da epilepsia, mas ajudaram a estabelecer a trepanação para EPT como prática comum.[40] O procedimento tornou-se mais aceito no final do século XIX, quando a antissepsia estava disponível e a especialização funcional era um conceito familiar.[40] No entanto, em 1890, o proeminente médico alemão Ernst von Bergmann criticou o procedimento; ele questionou sua eficácia (exceto em circunstâncias particulares) e sugeriu que as operações foram declaradas bem-sucedidas cedo demais após os procedimentos para saber se conferiam um benefício a longo prazo.[10] O final do século XIX viu o advento da cirurgia intracraniana, operando lesões cerebrais consideradas causadoras de crises, um passo além da cirurgia craniana, que envolvia apenas o crânio e as meninges.[10] Até 1893, pelo menos 42 operações intracranianas haviam sido realizadas para EPT nos EUA, com sucesso limitado.[10]
A cirurgia foi o tratamento padrão para EPT até os anos após a Segunda Guerra Mundial, quando a condição recebeu mais atenção à medida que soldados que sobreviveram a traumas cranianos a desenvolveram.[19] A necessidade crescente de medicamentos para tratar EPT levou a ensaios com antiepilépticos; esses ensaios iniciais sugeriram que os medicamentos poderiam prevenir a epileptogênese (o desenvolvimento da epilepsia).[19] Ainda se pensava na década de 1970 que os antiepilépticos poderiam prevenir a epileptogênese;[27] em 1973, 60% dos médicos pesquisados os usavam para prevenir EPT.[33] No entanto, os ensaios clínicos que apoiaram um efeito protetor dos antiepilépticos não foram controlados; em ensaios controlados posteriores, os medicamentos falharam em demonstrar um efeito antiepileptogênico.[41] Estudos mostraram que os antiepilépticos preveniam crises que ocorriam dentro de uma semana após a lesão, e em 1995 a força-tarefa da Brain Trauma Foundation publicou uma recomendação sugerindo seu uso para proteger contra crises precoces após o trauma.[33] No entanto, recomendações foram publicadas contra o uso profilático de antiepilépticos por mais de uma semana após a lesão pelo Brain Injury Special Interest Group da American Academy of Physical Medicine and Rehabilitation em 1998 e pela American Association of Neurological Surgeons em 2000.[12]
Pesquisa
Como a epilepsia se desenvolve após uma lesão cerebral não é totalmente compreendido, e ganhar tal entendimento pode ajudar os pesquisadores a encontrar maneiras de preveni-la, torná-la menos grave ou mais fácil de tratar.[22] Pesquisadores esperam identificar biomarcadores, indicações biológicas de que a epileptogênese está ocorrendo, como meio de encontrar medicamentos que possam atingir vias pelas quais a epilepsia se desenvolve.[25] Por exemplo, medicamentos poderiam ser desenvolvidos para interferir com lesão cerebral secundária (lesão que não ocorre no momento do trauma, mas resulta de processos iniciados por ele), bloqueando vias como danos por radicais livres ao tecido cerebral.[31] Um aumento no entendimento das diferenças de idade no desenvolvimento da epilepsia após trauma também pode ajudar os pesquisadores a encontrar biomarcadores de epileptogênese.[25] Há também interesse em encontrar mais medicamentos antiepilépticos, com potencial para interferir na epileptogênese.[42] Alguns novos antiepilépticos, como topiramato, gabapentina e lamotrigina, já foram desenvolvidos e mostraram promessa no tratamento da EPT.[8] Nenhum modelo animal tem todas as características da epileptogênese em humanos, então os esforços de pesquisa visam identificar um.[22][25] Tal modelo pode ajudar os pesquisadores a encontrar novos tratamentos e identificar os processos envolvidos na epileptogênese.[7] No entanto, os modelos mecânicos mais comuns de lesão cerebral traumática, como lesão por percussão de fluido, impacto cortical controlado e modelos de queda de peso, exibem epileptogênese em pontos de tempo crônicos com crises eletroencefalográficas e comportamentais remotas documentadas e aumento da suscetibilidade a crises.[43] Foi relatado que a EPT também pode ocorrer em peixes-zebra, resultando em respostas fisiopatológicas semelhantes as do TCE humano.[44]
Referências
- ↑ a b Brady, Rhys D.; Casillas-Espinosa, Pablo M.; Agoston, Denes V.; Bertram, Edward H.; Kamnaksh, Alaa; Semple, Bridgette D.; Shultz, Sandy R. (março de 2019). «Modelling traumatic brain injury and posttraumatic epilepsy in rodents». Neurobiology of Disease (em inglês). 123: 8–19. PMC 6348144
 . PMID 30121231. doi:10.1016/j.nbd.2018.08.007
. PMID 30121231. doi:10.1016/j.nbd.2018.08.007
- ↑ a b c Pagni CA, Zenga F (2005). «Posttraumatic epilepsy with special emphasis on prophylaxis and prevention». Acta Neurochirurgica. Acta Neurochirurgica Supplementum (em inglês). 93: 27–34. ISBN 978-3-211-24150-9. PMID 15986723. doi:10.1007/3-211-27577-0_3
- ↑ a b c d e f g h i
Garga N, Lowenstein DH (2006). «Posttraumatic Epilepsy: A Major Problem in Desperate Need of Major Advances». Epilepsy Currents (em inglês). 6 (1): 1–5. PMC 1363374
 . PMID 16477313. doi:10.1111/j.1535-7511.2005.00083.x
. PMID 16477313. doi:10.1111/j.1535-7511.2005.00083.x
- ↑ a b c d e f g h i j k Mani J, Barry E (2006). «Posttraumatic epilepsy». In: Wyllie E, Gupta A, Lachhwani DK. The Treatment of Epilepsy: Principles and Practice (em inglês). Hagerstown, MD: Lippincott Williams & Wilkins. pp. 521–524. ISBN 0-7817-4995-6
- ↑ Scheffer, Ingrid E.; Berkovic, Samuel; Capovilla, Giuseppe; Connolly, Mary B.; French, Jacqueline; Guilhoto, Laura; Hirsch, Edouard; Jain, Satish; Mathern, Gary W. (abril de 2017). «ILAE classification of the epilepsies: Position paper of the ILAE Commission for Classification and Terminology». Epilepsia (em inglês). 58 (4): 512–521. PMC 5386840
 . PMID 28276062. doi:10.1111/epi.13709
. PMID 28276062. doi:10.1111/epi.13709
- ↑
Pitkänen A, Kharatishvili I, Karhunen H, et al. (2007). «Epileptogenesis in experimental models». Epilepsia (em inglês). 48 (Supplement 2): 13–20. PMID 17571349. doi:10.1111/j.1528-1167.2007.01063.x

- ↑ a b c d e f g h i j k l m
D'Ambrosio R, Perucca E (2004). «Epilepsy after head injury». Current Opinion in Neurology (em inglês). 17 (6): 731–735. PMC 2672045
 . PMID 15542983. doi:10.1097/00019052-200412000-00014
. PMID 15542983. doi:10.1097/00019052-200412000-00014
- ↑ a b c d e f g h i j k l m n o p q r s t u v Agrawal A, Timothy J, Pandit L, Manju M (2006). «Post-traumatic epilepsy: An overview». Clinical Neurology and Neurosurgery (em inglês). 108 (5): 433–439. PMID 16225987. doi:10.1016/j.clineuro.2005.09.001
- ↑ a b c d e f Posner E, Lorenzo N (11 de outubro de 2006). "Posttraumatic epilepsy". Emedicine.com. Acessado em 2008-07-30.
- ↑ a b c d e f Eadie MJ, Bladin PF (2001). A Disease Once Sacred: A History of the Medical Understanding of Epilepsy (em inglês). London: John Libbey. pp. 215–216. ISBN 0-86196-607-4
- ↑ a b c d e f g
Frey LC (2003). «Epidemiology of posttraumatic epilepsy: A critical review». Epilepsia (em inglês). 44 (Supplement 10): 11–17. PMID 14511389. doi:10.1046/j.1528-1157.44.s10.4.x

- ↑ a b c d e f g h i j Tucker GJ (2005). «Seizures». In: Silver JM, McAllister TW, Yudofsky SC. Textbook Of Traumatic Brain Injury (em inglês). [S.l.]: American Psychiatric Pub., Inc. pp. 309–321. ISBN 1-58562-105-6
- ↑ a b Gupta YK, Gupta M (2006). «Post traumatic epilepsy: A review of scientific evidence» (PDF). Indian Journal of Physiology and Pharmacology (em inglês). 50 (1): 7–16. PMID 16850898. Consultado em 31 de julho de 2008. Arquivado do original (PDF) em 13 de julho de 2011
- ↑ a b Ayd FJ (2000). Lexicon of Psychiatry, Neurology, and the Neurosciences (em inglês). Philadelphia, Pa: Lippincott-Williams & Wilkins. pp. 888–890. ISBN 0-7817-2468-6
- ↑ Statler KD (2006). «Pediatric posttraumatic seizures: Epidemiology, putative mechanisms of epileptogenesis and promising investigational progress». Dev. Neurosci. (em inglês). 28 (4–5): 354–363. PMID 16943659. doi:10.1159/000094162
- ↑ Cuccurullo S (2004). Physical Medicine and Rehabilitation Board Review (em inglês). [S.l.]: Demos Medical Publishing. pp. 68–71. ISBN 1-888799-45-5
- ↑ a b Parent JM, Aminoff MJ (2004). «Treatment of epilepsy in general medical conditions». In: Dodson WE, Avanzini G, Shorvon SD, Fish DR, Perucca E. The Treatment of Epilepsy (em inglês). Oxford: Blackwell Science. 244 páginas. ISBN 0-632-06046-8
- ↑ a b c
Annegers JF, Hauser WA, Coan SP, Rocca WA (janeiro de 1998). «A population-based study of seizures after traumatic brain injuries». New England Journal of Medicine (em inglês). 338 (1): 20–4. PMID 9414327. doi:10.1056/NEJM199801013380104

- ↑ a b c d e f g h i Iudice A, Murri L (2000). «Pharmacological prophylaxis of post-traumatic epilepsy». Drugs (em inglês). 59 (5): 1091–9. PMID 10852641. doi:10.2165/00003495-200059050-00005
- ↑ a b c d e JW Sander, MC Walker e JE Smalls (2007). «Chapter 12: Adult onset epilepsies, DW Chadwick» (PDF). Epilepsy: From Cell to Community – A Practical Guide to Epilepsy (PDF) (em inglês). [S.l.]: National Society for Epilepsy. pp. 127–132. ISBN 978-0-9519552-4-6. Consultado em 26 de julho de 2008
- ↑ Oliveros-Juste A, Bertol V, Oliveros-Cid A (2002). «Preventive prophylactic treatment in posttraumatic epilepsy». Revista de Neurología (em inglês). 34 (5): 448–459. PMID 12040514. doi:10.33588/rn.3405.2001439
- ↑ a b c d e f g h i Pitkänen A, McIntosh TK (2006). «Animal models of post-traumatic epilepsy». Journal of Neurotrauma (em inglês). 23 (2): 241–261. PMID 16503807. doi:10.1089/neu.2006.23.241
- ↑ Beghi E (2004). «Aetiology of epilepsy». In: Dodson WE, Avanzini G, Shorvon SD, Fish DR, Perucca E. The Treatment of Epilepsy (em inglês). Oxford: Blackwell Science. 61 páginas. ISBN 0-632-06046-8
- ↑ de la Peña P, Porta-Etessam J (1998). «Post-traumatic epilepsy». Revista de Neurología (em espanhol). 26 (150): 256–261. PMID 9580443. doi:10.33588/rn.26150.981066
- ↑ a b c d e f g Herman ST (2002). «Epilepsy after brain insult: Targeting epileptogenesis». Neurology (em inglês). 59 (9 Suppl 5): S21–S26. PMID 12428028. doi:10.1212/wnl.59.9_suppl_5.s21
- ↑
Mazarati A (2006). «Is Posttraumatic Epilepsy the Best Model of Posttraumatic Epilepsy?». Epilepsy Currents (em inglês). 6 (6): 213–214. PMC 1783489
 . PMID 17260063. doi:10.1111/j.1535-7511.2006.00149.x
. PMID 17260063. doi:10.1111/j.1535-7511.2006.00149.x
- ↑ a b Willmore LJ (1990). «Post-traumatic epilepsy: Cellular mechanisms and implications for treatment». Epilepsia (em inglês). 31 (Supplement 3): S67–73. PMID 2226373. doi:10.1111/j.1528-1157.1990.tb05861.x
- ↑ Morimoto K, Fahnestock M, Racine RJ (maio de 2004). «Kindling and status epilepticus models of epilepsy: Rewiring the brain». Prog. Neurobiol. (em inglês). 73 (1): 1–60. PMID 15193778. doi:10.1016/j.pneurobio.2004.03.009
- ↑ Abel MS, McCandless DW (1992). «The kindling model of epilepsy». In: Adams RN, Baker GB, Baker JM, Bateson AN, Boisvert DP, Boulton AA, et al. Neuromethods: Animal Models of Neurological Disease (em inglês). Totowa, NJ: Humana Press. pp. 153–155. ISBN 0-89603-211-6
- ↑ Menkes JH, Sarnat HB, Maria BL (2005). Child Neurology (em inglês). Hagerstown, MD: Lippincott Williams & Wilkins. pp. 683–684. ISBN 0-7817-5104-7
- ↑ a b c d e Firlik KS, Spencer DD (2004). «Surgery of post-traumatic epilepsy». In: Dodson WE, Avanzini G, Shorvon SD, Fish DR, Perucca E. The Treatment of Epilepsy (em inglês). Oxford: Blackwell Science. pp. 775–778. ISBN 0-632-06046-8
- ↑
Barry E, Bergey GK, Krumholz A, et al. (1997). «Posttraumatic seizure types vary with the interval after head injury». Epilepsia (em inglês). 38 (Supplement 8): 49S–50S. doi:10.1111/j.1528-1157.1997.tb01495.x

- ↑ a b c Schierhout G, Roberts I (2008) [2001]. Schierhout, Gillian, ed. «Anti-epileptic drugs for preventing seizures following acute traumatic brain injury». Cochrane Database of Systematic Reviews (em inglês) (4): CD000173. PMID 11687070. doi:10.1002/14651858.CD000173
- ↑ a b
Beghi E (2003). «Overview of studies to prevent posttraumatic epilepsy». Epilepsia (em inglês). 44 (Supplement 10): 21–26. PMID 14511391. doi:10.1046/j.1528-1157.44.s10.1.x

- ↑ Szaflarski JP, Nazzal Y, Dreer LE (2014). «Post-traumatic epilepsy: current and emerging treatment options». Neuropsychiatric Disease and Treatment (em inglês). 10: 1469–77. PMC 4136984
 . PMID 25143737. doi:10.2147/NDT.S50421
. PMID 25143737. doi:10.2147/NDT.S50421
- ↑
Aroniadou-Anderjaska V, Fritsch B, Qashu F, Braga MF (fevereiro de 2008). «Pathology and Pathophysiology of the Amygdala in Epileptogenesis and Epilepsy». Epilepsy Res. (em inglês). 78 (2–3): 102–16. PMC 2272535
 . PMID 18226499. doi:10.1016/j.eplepsyres.2007.11.011
. PMID 18226499. doi:10.1016/j.eplepsyres.2007.11.011
- ↑ a b Young B (1992). «Post-traumatic epilepsy». In: Barrow DL. Complications and Sequelae of Head Injury (em inglês). Park Ridge, Ill: American Association of Neurological Surgeons. pp. 127–132. ISBN 1-879284-00-6
- ↑ Swash M (1998). Outcomes in Neurological and Neurosurgical Disorders (em inglês). Cambridge, UK: Cambridge University Press. pp. 172–173. ISBN 0-521-44327-X
- ↑
Diaz-Arrastia R, Agostini MA, Frol AB, et al. (novembro de 2000). «Neurophysiologic and neuroradiologic features of intractable epilepsy after traumatic brain injury in adults». Archives of Neurology (em inglês). 57 (11): 1611–1616. PMID 11074793. doi:10.1001/archneur.57.11.1611

- ↑ a b c d e Jensen RL, Stone JL (1997). «Benjamin Winslow Dudley and early American trephination for posttraumatic epilepsy». Neurosurgery (em inglês). 41 (1): 263–268. PMID 9218316. doi:10.1097/00006123-199707000-00045
- ↑ Willmore LJ (dezembro de 2005). «Antiepileptic drugs and neuroprotection: Current status and future roles». Epilepsy & Behavior (em inglês). 7 (Supplement 3): S25–S28. PMID 16239127. doi:10.1016/j.yebeh.2005.08.006
- ↑ Chang BS, Lowenstein DH (2003). «Practice parameter: Antiepileptic drug prophylaxis in severe traumatic brain injury: Report of the Quality Standards Subcommittee of the American Academy of Neurology». Neurology (em inglês). 60 (1): 10–16. PMID 12525711. doi:10.1212/01.wnl.0000031432.05543.14
- ↑ Glushakov, Alexander V.; Glushakova, Olena Y.; Doré, Sylvain; Carney, Paul R.; Hayes, Ronald L. (2016). «Animal Models of Posttraumatic Seizures and Epilepsy». Injury Models of the Central Nervous System. Col: Methods in Molecular Biology (em inglês). 1462. [S.l.: s.n.] pp. 481–519. ISBN 978-1-4939-3814-8. ISSN 1940-6029. PMC 6036905
 . PMID 27604735. doi:10.1007/978-1-4939-3816-2_27
. PMID 27604735. doi:10.1007/978-1-4939-3816-2_27
- ↑ Cho, Sung-Joon; Park, Eugene; Telliyan, Tamar; Baker, Andrew; Reid, Aylin Y. (agosto de 2020). «Zebrafish model of posttraumatic epilepsy». Epilepsia (em inglês). 61 (8): 1774–1785. ISSN 0013-9580. PMID 32592416. doi:10.1111/epi.16589