Molécula biatómica
Uma Molécula diatômica (português brasileiro) ou molécula diatómica (português europeu) ou molécula biatómica (Língua grega: di-, «dois»)? são moléculas compostas por apenas dois átomos, do mesmo ou de diferentes elementos químicos. Se uma molécula diatómica consiste em dois átomos do mesmo elemento, como o hidrogénio (H
2) ou o oxigénio (O
2), diz-se que é homonuclear. Caso contrário, se uma molécula diatómica consistir em dois átomos diferentes, como o monóxido de carbono (CO) ou o óxido nítrico (NO), a molécula é dita heteronuclear. A ligação numa molécula diatómica homonuclear é não polar.
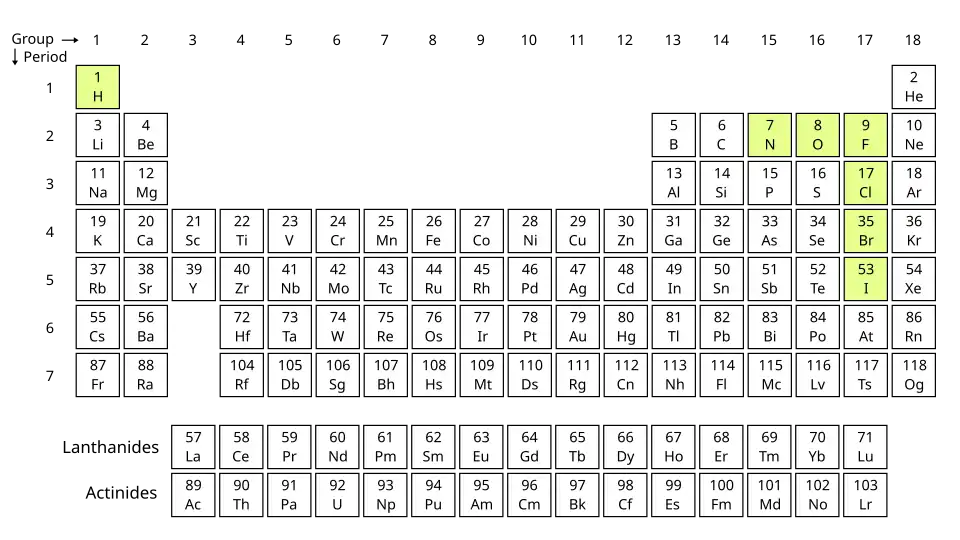
Os únicos elementos químicos que formam moléculas diatómicas homonucleares estáveis à temperatura e pressão padrão (STP) (ou em condições laboratoriais típicas de 1 bar e 25 °C) são os gases hidrogénio (H
2), azoto (N
2), oxigénio (O
2), flúor (F
2) e cloro (Cl
2), e o líquido bromo (Br
2).[1]
Os gases nobres (hélio, néon, árgon, cripton, xénon e radon) também são gases em STP, mas são monatómicos. Os gases diatómicos homonucleares e os gases nobres juntos são chamados de "gases elementares" ou "gases moleculares", para os distinguir de outros gases que são compostos químicos.[2]
A temperaturas ligeiramente elevadas, os halogéneos bromo (Br
2) e iodo (I
2) também formam gases diatómicos.[3] Todos os halogéneos foram observados como moléculas diatómicas, exceto o astato e o tenesso, que são incertos.
Outros elementos formam moléculas diatómicas quando evaporados, mas estas espécies diatómicas repolimerizam quando arrefecidas. O aquecimento ("cracking") do fósforo produz difósforo (P
2). O vapor de enxofre é maioritariamente dienxofre (S
2). O dilítio (Li
2) e o dissódio (Na
2)[4] são conhecidos na fase gasosa. O ditungsténio (W
2) e o dimolibdénio (Mo
2) formam-se com ligações sêxtuplas na fase gasosa. O dirubídio (Rb
2) é diatómico.
Moléculas heteronucleares
Todas as outras moléculas diatómicas são compostos químicos de dois elementos diferentes. Muitos elementos podem combinar-se para formar moléculas diatómicas heteronucleares, dependendo da temperatura e pressão.
Exemplos são os gases monóxido de carbono (CO), óxido nítrico (NO) e cloreto de hidrogénio (HCl).
Muitos compostos binários 1:1 não são normalmente considerados diatómicos porque são poliméricos à temperatura ambiente, mas formam moléculas diatómicas quando evaporados, por exemplo, o MgO gasoso, o SiO e muitos outros.
Ocorrência
Centenas de moléculas diatómicas foram identificadas[5] no ambiente da Terra, no laboratório e no espaço interestelar. Cerca de 99% da atmosfera da Terra é composta por duas espécies de moléculas diatómicas: azoto (78%) e oxigénio (21%). A abundância natural de hidrogénio (H2) na atmosfera terrestre é apenas da ordem de partes por milhão, mas o H2 é a molécula diatómica mais abundante no universo. O meio interestelar é dominado por átomos de hidrogénio.
Geometria molecular
Todas as moléculas diatómicas são lineares e caracterizadas por um único parâmetro que é o comprimento de ligação ou distância entre os dois átomos. O azoto diatómico tem uma ligação tripla, o oxigénio diatómico tem uma ligação dupla, e o hidrogénio, flúor, cloro, iodo e bromo diatómicos têm todos ligações simples.[6]
Significado histórico
Os elementos diatómicos desempenharam um papel importante na elucidação dos conceitos de elemento, átomo e molécula no século XIX, porque alguns dos elementos mais comuns, como o hidrogénio, o oxigénio e o azoto, ocorrem como moléculas diatómicas. A hipótese atómica original de John Dalton assumia que todos os elementos eram monatómicos e que os átomos nos compostos teriam normalmente as razões atómicas mais simples entre si. Por exemplo, Dalton assumiu que a fórmula da água seria HO, dando o peso atómico do oxigénio como oito vezes o do hidrogénio,[7] em vez do valor moderno de cerca de 16. Como consequência, existiu confusão em relação aos pesos atómicos e fórmulas moleculares durante cerca de meio século.
Já em 1805, Gay-Lussac e von Humboldt mostraram que a água é formada por dois volumes de hidrogénio e um volume de oxigénio, e em 1811 Amedeo Avogadro chegou à interpretação correta da composição da água, baseada no que hoje é chamado de Lei de Avogadro e na suposição de moléculas elementares diatómicas. No entanto, estes resultados foram maioritariamente ignorados até 1860, em parte devido à crença de que átomos de um elemento não teriam afinidade química com átomos do mesmo elemento, e também em parte devido a aparentes exceções à lei de Avogadro que não foram explicadas até mais tarde em termos de moléculas dissociativas.
No Congresso de Karlsruhe de 1860 sobre pesos atómicos, Cannizzaro ressuscitou as ideias de Avogadro e utilizou-as para produzir uma tabela consistente de pesos atómicos, que concorda maioritariamente com os valores modernos. Estes pesos foram um pré-requisito importante para a descoberta da lei periódica por Dmitri Mendeleev e Lothar Meyer.[8]
Estados eletrónicos excitados
As moléculas diatómicas estão normalmente no seu estado mais baixo ou fundamental, que convencionalmente também é conhecido como o estado . Quando um gás de moléculas diatómicas é bombardeado por eletrões energéticos, algumas das moléculas podem ser excitadas para estados eletrónicos superiores, como ocorre, por exemplo, na aurora natural; explosões nucleares de alta altitude; e experiências com canhões de eletrões transportados por foguetes.[9] Tal excitação também pode ocorrer quando o gás absorve luz ou outra radiação eletromagnética. Os estados excitados são instáveis e relaxam naturalmente de volta ao estado fundamental. Ao longo de várias escalas de tempo curtas após a excitação (tipicamente uma fração de segundo, ou por vezes mais de um segundo se o estado excitado for metaestável), ocorrem transições de estados eletrónicos superiores para inferiores e, finalmente, para o estado fundamental, e em cada transição resulta a emissão de um fotão. Esta emissão é conhecida como fluorescência. Estados eletrónicos sucessivamente superiores são convencionalmente nomeados , , , etc. (mas esta convenção nem sempre é seguida, e por vezes são usadas letras minúsculas e letras fora de sequência alfabética, como no exemplo abaixo). A energia de excitação deve ser maior ou igual à energia do estado eletrónico para que a excitação ocorra.
Na teoria quântica, um estado eletrónico de uma molécula diatómica é representado pelo símbolo de termo molecular onde é o número quântico de spin eletrónico total, é o número quântico de momento angular eletrónico total ao longo do eixo internuclear, e é o número quântico vibracional. assume os valores 0, 1, 2, ..., que são representados pelos símbolos de estado eletrónico , , , ... Por exemplo, a tabela seguinte lista os estados eletrónicos comuns (sem números quânticos vibracionais) juntamente com a energia do nível vibracional mais baixo () do azoto diatómico (N2), o gás mais abundante na atmosfera da Terra.[10]
Os subscritos e sobrescritos após fornecem detalhes mecânicos quânticos adicionais sobre o estado eletrónico. O sobrescrito ou determina se a reflexão num plano que contém o eixo internuclear introduz uma mudança de sinal na função de onda. O subscrito ou aplica-se a moléculas de átomos idênticos, e ao refletir o estado ao longo de um plano perpendicular ao eixo molecular, estados que não mudam são rotulados como (gerade), e estados que mudam de sinal são rotulados como (ungerade).
| Estado | Energia[a] (, cm−1) |
|---|---|
| 0.0 | |
| 49754.8 | |
| 59306.8 | |
| 59380.2 | |
| 65851.3 | |
| 67739.3 | |
| 68951.2 | |
| 71698.4 |
A referida fluorescência ocorre em regiões distintas do espectro eletromagnético, chamadas "bandas de emissão": cada banda corresponde a uma transição particular de um estado eletrónico e nível vibracional superior para um estado eletrónico e nível vibracional inferior (tipicamente, muitos níveis vibracionais estão envolvidos num gás excitado de moléculas diatómicas). Por exemplo, as bandas de emissão N2 - (também conhecidas como bandas de Vegard-Kaplan) estão presentes na faixa espectral de 0,14 a 1,45 μm (micrómetros).[9] Uma dada banda pode ser espalhada por vários nanómetros no espaço de comprimento de onda eletromagnético, devido às várias transições que ocorrem no número quântico rotacional da molécula, . Estas são classificadas em ramos de sub-bandas distintos, dependendo da mudança em .[11] O ramo corresponde a , o ramo a , e o ramo a . As bandas são espalhadas ainda mais pela resolução espectral limitada do espectrómetro usado para medir o espectro. A resolução espectral depende da função de dispersão de ponto do instrumento.
Níveis de energia
O símbolo de termo molecular é uma expressão abreviada dos momentos angulares que caracterizam os estados quânticos eletrónicos de uma molécula diatómica, que também são autoestados do Hamiltoniano molecular eletrónico. Também é conveniente, e comum, representar uma molécula diatómica como duas massas pontuais ligadas por uma mola sem massa. As energias envolvidas nos vários movimentos da molécula podem então ser divididas em três categorias: as energias translacional, rotacional e vibracional. O estudo teórico dos níveis de energia rotacional das moléculas diatómicas pode ser descrito usando a descrição abaixo dos níveis de energia rotacional. Enquanto o estudo do nível de energia vibracional das moléculas diatómicas pode ser descrito usando a aproximação do oscilador harmónico ou usando potenciais de interação vibracional quântica.[12][13] Estes potenciais fornecem níveis de energia mais precisos porque levam em conta múltiplos efeitos vibracionais.
Em relação à história, o primeiro tratamento de moléculas diatómicas com mecânica quântica foi feito por Lucy Mensing em 1926.[14]
Energias translacionais
A energia translacional da molécula é dada pela expressão da energia cinética: onde é a massa da molécula e é a sua velocidade.
Energias rotacionais
Classicamente, a energia cinética de rotação é onde
- é o momento angular
- é o momento de inércia da molécula
Para sistemas microscópicos de nível atómico como uma molécula, o momento angular só pode ter valores discretos específicos dados por onde é um número inteiro não negativo e é a constante de Planck reduzida.
Além disso, para uma molécula diatómica, o momento de inércia é onde
- é a massa reduzida da molécula e
- é a distância média entre os centros dos dois átomos na molécula.
Assim, substituindo o momento angular e o momento de inércia em Erot, os níveis de energia rotacional de uma molécula diatómica são dados por:
Energias vibracionais
Outro tipo de movimento de uma molécula diatómica é para cada átomo oscilar — ou vibrar — ao longo da linha que liga os dois átomos. A energia vibracional é aproximadamente a de um oscilador harmónico quântico: onde
- é um número inteiro
- é a constante de Planck reduzida e
- é a frequência angular da vibração.
Comparação entre os espaçamentos das energias rotacional e vibracional
O espaçamento, e a energia de uma transição espectroscópica típica, entre os níveis de energia vibracional é cerca de 100 vezes maior do que o de uma transição típica entre os níveis de energia rotacional.
Casos de Hund
Os bons números quânticos para uma molécula diatómica, bem como boas aproximações dos níveis de energia rotacional, podem ser obtidos modelando a molécula usando os Casos de Hund.
Mnemónicas
As mnemónicas BrINClHOF, pronunciado "Brinklehof",[15] HONClBrIF, pronunciado "Honkelbrif",[16] “HOBrFINCl”, pronunciado “Hoberfinkel”, e HOFBrINCl, pronunciado "Hofbrinkle", foram cunhadas para ajudar a recordar a lista de elementos diatómicos. Outro método, para falantes de inglês, é a frase: "Never Have Fear of Ice Cold Beer" como uma representação de Azoto (Nitrogen), Hidrogénio, Flúor, Oxigénio, Iodo, Cloro, Bromo.
Ver também
- Simetria de moléculas diatómicas
- Método AXE
- Ligação covalente
- Gás industrial
Notas
- ↑ As unidades de "energia" aqui são, na verdade, o recíproco do comprimento de onda de um fotão emitido numa transição para o estado de energia mais baixa. A energia real pode ser encontrada multiplicando a estatística dada pelo produto de c (a velocidade da luz) e h (a constante de Planck); i.e., cerca de 1,99 × 10−25 joule-metros, e depois multiplicando por um fator adicional de 100 para converter de cm−1 para m−1.
Referências
- ↑ Hammond, C.R. (2012). «Section 4: Properties of the Elements and Inorganic Compounds» (PDF). Handbook of Chemistry and Physics. [S.l.: s.n.] Cópia arquivada (PDF) em 11 de novembro de 2011
- ↑ Emsley, J. (1989). The Elements. Oxford: Clarendon Press. pp. 22–23. ISBN 9780198555681
- ↑ Whitten, Kenneth W.; Davis, Raymond E.; Peck, M. Larry; Stanley, George G. (2010). Chemistry 9th ed. [S.l.]: Brooks/Cole, Cengage Learning. pp. 337–338. ISBN 9780495391630
- ↑ Lu, Z.W.; Wang, Q.; He, W.M.; Ma, Z.G. (Julho 1996). «New parametric emissions in diatomic sodium molecules». Applied Physics B. 63 (1): 43–46. Bibcode:1996ApPhB..63...43L. doi:10.1007/BF01112836
- ↑ Huber, K. P.; Herzberg, G. (1979). Molecular Spectra and Molecular Structure IV. Constants of Diatomic Molecules. [S.l.]: New York: Van Nostrand: Reinhold. ISBN 978-0-442-23394-5
- ↑ Brown, Catrin; Ford, Mike (2014). Standard Level Chemistry 2nd ed. [S.l.]: Prentice Hall. pp. 123–125. ISBN 9781447959069
- ↑ Langford, Cooper Harold; Beebe, Ralph Alonzo (1 de janeiro de 1995). The Development of Chemical Principles (em inglês). [S.l.]: Courier Corporation. ISBN 9780486683591
- ↑ Ihde, Aaron J. (1961). «The Karlsruhe Congress: A centennial retrospective». Journal of Chemical Education. 38 (2): 83–86. Bibcode:1961JChEd..38...83I. doi:10.1021/ed038p83. Consultado em 24 de agosto de 2007. Cópia arquivada em 28 de setembro de 2007 Verifique o valor de
|url-access=subscription(ajuda) - 1 2
Gilmore, Forrest R.; Laher, Russ R.; Espy, Patrick J. (1992). «Franck-Condon Factors, r-Centroids, Electronic Transition Moments, and Einstein Coefficients for Many Nitrogen and Oxygen Band Systems». Journal of Physical and Chemical Reference Data. 21 (5): 1005–1107. Bibcode:1992JPCRD..21.1005G. doi:10.1063/1.555910. Cópia arquivada em 9 de julho de 2017 Verifique o valor de
|url-access=subscription(ajuda) - ↑
Laher, Russ R.; Gilmore, Forrest R. (1991). «Improved Fits for the Vibrational and Rotational Constants of Many States of Nitrogen and Oxygen». Journal of Physical and Chemical Reference Data. 20 (4): 685–712. Bibcode:1991JPCRD..20..685L. doi:10.1063/1.555892. Cópia arquivada em 2 de junho de 2018 Verifique o valor de
|url-access=subscription(ajuda) - ↑ Levine, Ira N. (1975), Molecular Spectroscopy, ISBN 0-471-53128-6, John Wiley & Sons, pp. 508–9
- ↑ Mishra, Swati (2022). «Temperature guided behavioral transitions in confined helium: Gas-wall interaction effects on dynamics and transport in the cryogenic limit». Chemical Thermodynamics and Thermal Analysis. 7 (August). doi:10.1016/j.ctta.2022.100073
- ↑ Al-Raeei, Marwan (2022). «Morse potential specific bond volume: a simple formula with applications to dimers and soft–hard slab slider». Journal of Physics: Condensed Matter. 34 (28). 284001 páginas. Bibcode:2022JPCM...34B4001A. PMID 35544352. doi:10.1088/1361-648X/ac6a9b
- ↑ Mensing, Lucy (1 de novembro de 1926). «Die Rotations-Schwingungsbanden nach der Quantenmechanik». Zeitschrift für Physik (em alemão). 36 (11): 814–823. Bibcode:1926ZPhy...36..814M. ISSN 0044-3328. doi:10.1007/BF01400216
- ↑ «Mnemonic BrINClHOF (pronounced Brinklehoff) in Chemistry» (em inglês). Consultado em 1 de junho de 2019
- ↑ Sherman, Alan (1992). Chemistry and Our Changing World. [S.l.]: Prentice Hall. p. 82. ISBN 9780131315419
Leitura adicional
- Huber, K. P.; Herzberg, G. (1979). Molecular Spectra and Molecular Structure IV. Constants of Diatomic Molecules. [S.l.]: New York: Van Nostrand: Reinhold
- Tipler, Paul (1998). Physics For Scientists and Engineers: Vol. 1 4th ed. [S.l.]: W. H. Freeman. ISBN 1-57259-491-8
Ligações externas
- Hyperphysics – Espectros Rotacionais de Moléculas de Rotor Rígido
- Hyperphysics – Oscilador Harmónico Quântico
- IUMSC – Centro de Estrutura Molecular da Universidade de Indiana
Predefinição:MolecularGeometry Predefinição:Diatomicelements Predefinição:Molecules detected in outer space