Hidrazona
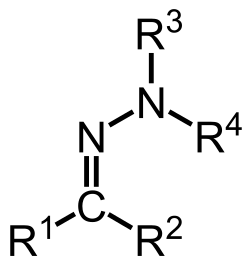
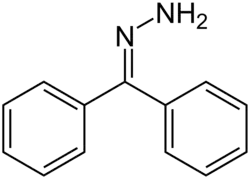
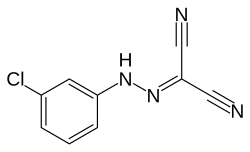
Uma hidrazona é uma classe de compostos orgânicos com a estrutura R2C=NNR2 [1]. Estes compostos são derivados funcionais de cetonas e aldeídos formados pela substituição do átomo de oxigênio do grupo carbonila(C=O) pelo grupo funcional hidrazonico NNH2[1]. A Síntese ocorre tipicamnete através da condensação de uma hidrazina (Ou seus derivados) com um composto carbonílico,liberando uma molécula de água como subproduto.
Princípios Físicos e Mecanismo de Formação
A formação de uma hidrazona segue um mecanismo de adição nucleofílica seguido de eliminação (desidratação). O par de elétrons do nitrogênio terminal da hidrazina ataca o carbono eletrofílico da carbonila, formando um intermediário conhecido como carbinolamina. Sob catálise ácida moderada, a hidroxila desse intermediário é protonada e eliminada na forma de água, estabelecendo a ligação dupla carbono-nitrogênio (C=N). Este processo é reversível em meio aquoso ácido, o que permite que as hidrazonas sejam hidrolisadas de volta aos seus precursores originais. A estabilidade da hidrazona formada depende fortemente da natureza dos grupos
- grupos aromáticos tendem a estabilizar a estrutura por ressonância.
Isomerismo e Configuração Molecular
Devido à presença da ligação dupla C= as hidrazonas apresentam isomerismo geométrico (ou isomerismo cis-trans), frequentemente designado pelas letras E (entgegen) e Z (zusammen)
Configuração E/Z: A barreira de rotação em torno da ligação dupla é alta o suficiente para que os isômeros possam ser distinguidos. O isômero E é geralmente o mais estável termodinamicamente devido à menor repulsão estérica entre os substituintes volumosos.
Tautomerismo: Em certas condições, hidrazonas que possuem hidrogênios no carbono alfa podem exibir tautomerismo azo-hidrazona, onde o próton migra do nitrogênio para o carbono, alterando a posição da ligação dupla.
Quiralidade: Se os grupos R
ligados ao carbono ou ao nitrogênio forem diferentes e contiverem centros assimétricos, a molécula exibirá atividade óptica, sendo um campo vasto de estudo na síntese assimétrica.
Ocorrência e Derivados Importantes
Embora raramente encontradas de forma livre em sistemas biológicos simples, as hidrazonas são blocos de construção essenciais em química orgânica:
Fenil-hidrazonas: Historicamente importantes na identificação de açúcares (osazonas), técnica desenvolvida por Emil Fischer.
2,4-Dinitrofenil-hidrazonas (2,4-DNP): Sólidos cristalinos de cores vibrantes (amarelo a vermelho) usados como derivados para caracterizar aldeídos e cetonas desconhecidos em análises qualitativas.
N-acil-hidrazonas: Uma subfamília que apresenta propriedades farmacológicas promissoras, especialmente em estudos de novos candidatos a fármacos anti-inflamatórios e analgésicos.
Aplicações Industriais e Laboratoriais
As hidrazonas são intermediários versáteis com diversas utilidades:
Redução de Wolff-Kishner: Uma das aplicações mais famosas, onde a hidrazona é tratada com uma base forte em alta temperatura para converter o grupo carbonila original em um grupo metileno (-CH2-)
Redução de Wolff-Kishner: Uma das aplicações mais famosas, onde a hidrazona é tratada com uma base forte em alta temperatura para converter o grupo carbonila original em um grupo metileno.
Síntese de Indol de Fischer: Utiliza fenil-hidrazonas como reagentes de partida para a criação de anéis indólicos, estruturas fundamentais em muitos alcaloides e medicamentos. Sensores Químicos: Devido às suas propriedades fluorescentes e capacidade de coordenar metais, são usadas no desenvolvimento de quimiossensores para detectar íons específicos em soluções ambientais.
Farmacologia: Muitas hidrazonas demonstram atividades biológicas, incluindo propriedades antibacterianas, antifúngicas e antitumorais
Vantagens e Desafios Sintéticos
A principal vantagem das hidrazonas é a facilidade de sua síntese e a cristalinização eficiente, o que facilita a purificação de compostos orgânicos complexos. No entanto, o manuseio de seus precursores (hidrazinas) exige cautela rigorosa, pois muitos são compostos altamente tóxicos, voláteis e potencialmente carcinogênicos. Além disso, o controle da seletividade E/Z durante a síntese pode ser um desafio em reações que exigem estereoquímica precisa para aplicações biomédicas.
Ver também
Referências
- 1 2 Victor Gold, IUPAC Gold Book, hydrazones