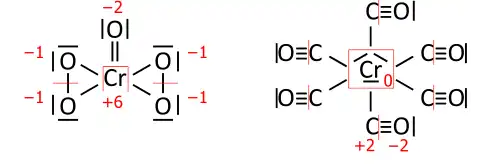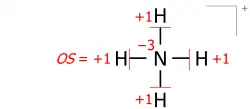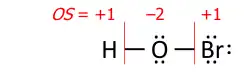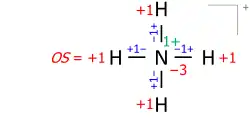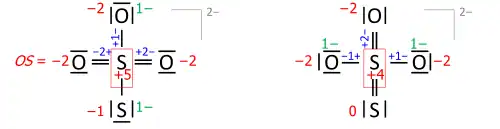Estado de oxidação
O estado de oxidação, também chamado de número de oxidação (nox), é uma abordagem para atribuir o valor da carga que um átomo em uma substância possui. O estado de oxidação contribui para a compreensão do grau de oxidação de um átomo a partir da consideração de que todas as ligações químicas existentes sejam iônicas, muito embora isso não seja necessariamente verdadeiro.[1] O termo oxidação foi usado pela primeira vez por Antoine Lavoisier para significar a reação de uma substância com o oxigênio.[2]
Em uma reação de oxirredução, o aumento do número de oxidação no produto em relação ao reagente significa que aquele átomo perdeu elétrons e foi oxidado; a diminuição do número de oxidação no produto em relação ao reagente significa que aquele átomo ganhou elétrons e foi reduzido.
Na química, o estado de oxidação é sempre relatado no nome químico de um composto. Os estados de oxidação desempenham um papel tão importante nos fundamentos da química que alguns argumentaram que deveriam ser representados como a terceira dimensão da tabela periódica. Um bom exemplo é o cromo: no estado de oxidação III é essencial ao corpo humano; no estado de oxidação IV, é extremamente tóxico.[3]
O estado de oxidação é a carga hipotética de um átomo se todas as suas ligações com outros átomos fossem totalmente iónicas. Descreve o grau de oxidação (perda de eletrões) de um átomo num composto químico. Conceptualmente, o estado de oxidação pode ser positivo, negativo ou zero. Além da ligação iónica quase pura, muitas ligações covalentes exibem uma forte ionicidade, tornando o estado de oxidação um preditor útil de carga.
O estado de oxidação de um átomo não representa a carga "real" nesse átomo, ou qualquer outra propriedade atómica real. Isto é particularmente verdadeiro para estados de oxidação elevados, onde a energia de ionização necessária para produzir um ião multipositivo é muito superior às energias disponíveis em reações químicas. Além disso, os estados de oxidação dos átomos num determinado composto podem variar dependendo da escolha da escala de eletronegatividade utilizada no seu cálculo. Assim, o estado de oxidação de um átomo num composto é puramente um formalismo. No entanto, é importante para compreender as convenções de nomenclatura de compostos inorgânicos. Além disso, várias observações relativas a reações químicas podem ser explicadas a um nível básico em termos de estados de oxidação.
Os estados de oxidação são tipicamente representados por números inteiros que podem ser positivos, zero ou negativos. Em alguns casos, o estado de oxidação médio de um elemento é uma fração, como 8/3 para o ferro na magnetite Fe
3O
4 (veja abaixo). O estado de oxidação mais elevado conhecido é relatado como sendo +9, exibido pelo irídio no catião tetroxoirídio(IX) (IrO+
4).[4] Prevê-se que até um estado de oxidação +10 possa ser alcançado pela platina no tetroxoplatina(X), PtO2+
4.[5] O estado de oxidação mais baixo é −5, como no boro em Al
3BC[6] e no gálio no digaleto de pentamagnésio (Mg
5Ga
2).
Na nomenclatura de Stock, que é comummente utilizada para compostos inorgânicos, o estado de oxidação é representado por um número romano colocado após o nome do elemento entre parênteses, ex: Óxido de ferro(III), ou como um sobrescrito após o símbolo do elemento, ex: FeIII2O3. O termo oxidação foi utilizado pela primeira vez por Antoine Lavoisier para significar a reação de uma substância com o oxigénio. Muito mais tarde, percebeu-se que a substância, ao ser oxidada, perde eletrões, e o significado foi alargado para incluir outras reações nas quais os eletrões são perdidos, independentemente de o oxigénio estar envolvido. O aumento do estado de oxidação de um átomo, através de uma reação química, é conhecido como oxidação; uma diminuição no estado de oxidação é conhecida como uma redução. Tais reações envolvem a transferência formal de eletrões: um ganho líquido de eletrões sendo uma redução, e uma perda líquida de eletrões sendo oxidação. Para elementos puros, o estado de oxidação é zero.
Visão Geral
Os números de oxidação são atribuídos aos elementos numa molécula de tal forma que a soma global é zero numa molécula neutra. O número indica o grau de oxidação de cada elemento causado pela ligação molecular. Em compostos iónicos, os números de oxidação são os mesmos que a carga iónica do elemento. Assim, para o KCl, ao potássio é atribuído +1 e ao cloro é atribuído −1.[7] O conjunto completo de regras para a atribuição de números de oxidação é discutido nas secções seguintes.
Os números de oxidação são fundamentais para a nomenclatura química de compostos iónicos. Por exemplo, os compostos de Cu com estado de oxidação +2 são chamados cúpricos e aqueles com estado +1 são cuprosos.[7]:172 Os números de oxidação dos elementos permitem previsões de fórmulas químicas e reações, especialmente reações de oxidação-redução. Os números de oxidação dos compostos químicos mais estáveis seguem tendências na tabela periódica.[8]:140
Definição da IUPAC
A União Internacional de Química Pura e Aplicada (IUPAC) publicou uma "Definição abrangente de estado de oxidação (Recomendações IUPAC 2016)".[9] É uma destilação de um relatório técnico da IUPAC: "Rumo a uma definição abrangente de estado de oxidação".[10] De acordo com o Gold Book da IUPAC: "O estado de oxidação de um átomo é a carga deste átomo após a aproximação iónica das suas ligações heteronucleares."[11] O termo número de oxidação é quase sinónimo.[12]
A aproximação iónica significa extrapolar as ligações para iónicas. Vários critérios[13] foram considerados para a aproximação iónica:
- Extrapolação da polaridade da ligação;
- a partir da diferença de eletronegatividade,
- a partir do momento de dipolo, e
- a partir de cálculos de química quântica de cargas.
- Atribuição de eletrões de acordo com a contribuição do átomo para a ligação de Orbital Molecular (MO)[13][14] ou a fidelidade do eletrão num modelo LCAO–MO.[15]
Numa ligação entre dois elementos diferentes, os eletrões da ligação são atribuídos ao seu principal contribuinte atómico, tipicamente de maior eletronegatividade; numa ligação entre dois átomos do mesmo elemento, os eletrões são divididos igualmente. A maioria das escalas de eletronegatividade depende do estado de ligação do átomo, o que torna a atribuição do estado de oxidação um argumento algo circular. Por exemplo, algumas escalas podem resultar em estados de oxidação invulgares, como −6 para a platina em PtH2–
4, para as escalas de Pauling e Mulliken.[10] Os momentos de dipolo também resultariam por vezes em números de oxidação anormais, como no CO e NO, que estão orientados com a sua extremidade positiva em direção ao oxigénio. Portanto, isto deixa a contribuição do átomo para a MO de ligação, a energia da orbital atómica e os cálculos de cargas da química quântica como os únicos critérios viáveis com valores convincentes para a aproximação iónica. No entanto, para uma estimativa simples para a aproximação iónica, podemos usar as eletronegatividades de Allen,[10] pois apenas essa escala de eletronegatividade é verdadeiramente independente do estado de oxidação, uma vez que se relaciona com a energia média dos eletrões de valência do átomo livre:
| Grupo → | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ↓ Período | ||||||||||||||||||
| 1 | H 2.300 |
He 4.160 | ||||||||||||||||
| 2 | Li 0.912 |
Be 1.576 |
B 2.051 |
C 2.544 |
N 3.066 |
O 3.610 |
F 4.193 |
Ne 4.787 | ||||||||||
| 3 | Na 0.869 |
Mg 1.293 |
Al 1.613 |
Si 1.916 |
P 2.253 |
S 2.589 |
Cl 2.869 |
Ar 3.242 | ||||||||||
| 4 | K 0.734 |
Ca 1.034 |
Sc 1.19 |
Ti 1.38 |
V 1.53 |
Cr 1.65 |
Mn 1.75 |
Fe 1.80 |
Co 1.84 |
Ni 1.88 |
Cu 1.85 |
Zn 1.588 |
Ga 1.756 |
Ge 1.994 |
As 2.211 |
Se 2.424 |
Br 2.685 |
Kr 2.966 |
| 5 | Rb 0.706 |
Sr 0.963 |
Y 1.12 |
Zr 1.32 |
Nb 1.41 |
Mo 1.47 |
Tc 1.51 |
Ru 1.54 |
Rh 1.56 |
Pd 1.58 |
Ag 1.87 |
Cd 1.521 |
In 1.656 |
Sn 1.824 |
Sb 1.984 |
Te 2.158 |
I 2.359 |
Xe 2.582 |
| 6 | Cs 0.659 |
Ba 0.881 |
Lu 1.09 |
Hf 1.16 |
Ta 1.34 |
W 1.47 |
Re 1.60 |
Os 1.65 |
Ir 1.68 |
Pt 1.72 |
Au 1.92 |
Hg 1.765 |
Tl 1.789 |
Pb 1.854 |
Bi 2.01 |
Po 2.19 |
At 2.39 |
Rn 2.60 |
| 7 | Fr 0.67 |
Ra 0.89 | ||||||||||||||||
| Ver também: Anexo:Tabela de eletronegatividades dos elementos químicos (página de dados) | ||||||||||||||||||
Determinação
Embora os níveis introdutórios do ensino da química utilizem estados de oxidação postulados, a recomendação da IUPAC[9] e a entrada do Gold Book[11] listam dois algoritmos inteiramente gerais para o cálculo dos estados de oxidação de elementos em compostos químicos.
Abordagem simples sem considerações de ligação
A química introdutória utiliza postulados: o estado de oxidação de um elemento numa fórmula química é calculado a partir da carga global e dos estados de oxidação postulados para todos os outros átomos.
Um exemplo simples baseia-se em dois postulados:
- EO = +1 para o hidrogénio
- EO = −2 para o oxigénio
onde EO significa estado de oxidação. Esta abordagem produz estados de oxidação corretos em óxidos e hidróxidos de qualquer elemento único, e em ácidos como o ácido sulfúrico (H
2SO
4) ou o ácido dicrómico (H
2Cr
2O
7). A sua cobertura pode ser alargada por uma lista de exceções ou atribuindo prioridade aos postulados. Este último funciona para o peróxido de hidrogénio (H
2O
2), onde a prioridade da regra 1 deixa ambos os oxigénios com estado de oxidação −1.
Postulados adicionais e a sua classificação podem expandir a gama de compostos para se adequarem ao âmbito de um livro didático. Como exemplo, um algoritmo de postulados de entre muitos possíveis, numa sequência de prioridade decrescente:
- Um elemento na forma livre tem EO = 0.
- Num composto ou ião, a soma dos estados de oxidação é igual à carga total do composto ou ião.
- O Flúor em compostos tem EO = −1; isto estende-se ao cloro e bromo apenas quando não ligados a um halogéneo mais leve, oxigénio ou nitrogénio.
- Os metais do Grupo 1 e grupo 2 em compostos têm EO = +1 e +2, respetivamente.
- O hidrogénio tem EO = +1, mas adota −1 quando ligado como um hidreto a metais ou metaloides.
- O oxigénio em compostos tem EO = −2, mas apenas quando não ligado ao oxigénio (ex: em peróxidos) ou flúor.
Este conjunto de postulados cobre estados de oxidação de fluoretos, cloretos, brometos, óxidos, hidróxidos e hidretos de qualquer elemento único. Cobre todos os oxoácidos de qualquer átomo central (e todos os seus parentes flúor-, cloro- e bromo-), bem como sais de tais ácidos com metais dos grupos 1 e 2. Também cobre iodetos, sulfuretos e sais simples semelhantes destes metais.
Algoritmo de atribuição de ligações
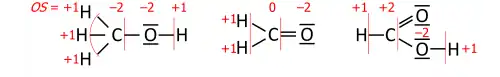
Este algoritmo é realizado numa Estrutura de Lewis (um diagrama que mostra todos os eletrões de valência). O estado de oxidação é igual à carga de um átomo após cada uma das suas ligações heteronucleares ter sido atribuída ao parceiro mais eletronegativo da ligação (exceto quando esse parceiro é um ligante de ácido de Lewis ligado reversivelmente) e as ligações homonucleares terem sido divididas igualmente:
onde cada "—" representa um par de eletrões (partilhado entre dois átomos ou apenas num átomo), e "EO" é o estado de oxidação como uma variável numérica.
Após os eletrões terem sido atribuídos de acordo com as linhas vermelhas verticais na fórmula, o número total de eletrões de valência que agora "pertencem" a cada átomo é subtraído do número N de eletrões de valência do átomo neutro (como 5 para o nitrogénio no grupo 15) para produzir o estado de oxidação desse átomo.
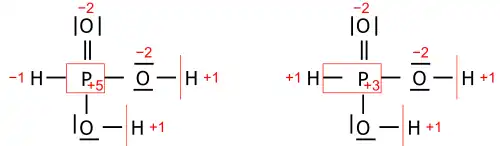
Este exemplo mostra a importância de descrever a ligação. A sua fórmula sumária, HNO
3, corresponde a dois isómeros estruturais; o ácido peroxonitroso na figura acima e o mais estável ácido nítrico. Com a fórmula HNO
3, a abordagem simples sem considerações de ligação produz −2 para os três oxigénios e +5 para o nitrogénio, o que está correto para o ácido nítrico. Para o ácido peroxonitroso, no entanto, ambos os oxigénios na ligação O–O têm EO = −1, e o nitrogénio tem EO = +3, o que requer uma estrutura para compreender.
Os compostos orgânicos são tratados de forma semelhante; exemplificados aqui nos grupos funcionais que ocorrem entre o metano (CH
4) e o dióxido de carbono (CO
2):
Analogamente para compostos de metal de transição; CrO(O
2)
2 à esquerda tem um total de 36 eletrões de valência (18 pares para serem distribuídos), e o hexacarbonilcrómio (Cr(CO)
6) à direita tem 66 eletrões de valência (33 pares):
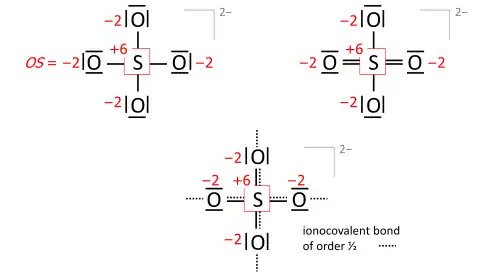
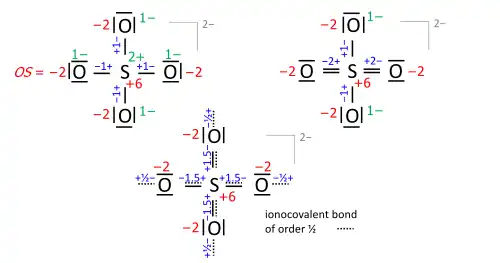
Um passo fundamental é desenhar a estrutura de Lewis da molécula (neutra, catiónica, aniónica): Os símbolos dos átomos são organizados de modo que pares de átomos possam ser unidos por ligações simples de dois eletrões como na molécula (uma espécie de estrutura "esquelética"), e os restantes eletrões de valência são distribuídos de modo que os átomos sp obtenham um octeto (dueto para o hidrogénio) com uma prioridade que aumenta proporcionalmente com a eletronegatividade. Em alguns casos, isto leva a fórmulas alternativas que diferem nas ordens de ligação (o conjunto completo das quais é chamado de fórmulas de ressonância). Considere o anião sulfato (SO2–
4) com 32 eletrões de valência; 24 dos oxigénios, 6 do enxofre, 2 da carga do anião obtida do catião implícito. As ordens de ligação para os oxigénios terminais não afetam o estado de oxidação desde que os oxigénios tenham octetos. Já a estrutura esquelética, no canto superior esquerdo, produz os estados de oxidação corretos, tal como a estrutura de Lewis, no canto superior direito (uma das fórmulas de ressonância):
A fórmula de ordem de ligação na parte inferior é a mais próxima da realidade de quatro oxigénios equivalentes, cada um tendo uma ordem de ligação total de 2. Esse total inclui a ligação de ordem 1/2 ao catião implícito e segue a regra 8 − N[10] exigindo que o total da ordem de ligação do átomo do grupo principal seja igual a 8 − N eletrões de valência do átomo neutro, aplicada com uma prioridade que aumenta proporcionalmente com a eletronegatividade.
Este algoritmo funciona igualmente para catiões moleculares compostos por vários átomos. Um exemplo é o catião amónio de 8 eletrões de valência (5 do nitrogénio, 4 dos hidrogénios, menos 1 eletrão para a carga positiva do catião):
Desenhar estruturas de Lewis com pares de eletrões como traços enfatiza a equivalência essencial de pares de ligação e pares solitários ao contar eletrões e mover ligações para os átomos. Estruturas desenhadas com pares de pontos de eletrões são, obviamente, idênticas em todos os aspetos:
A ressalva do algoritmo
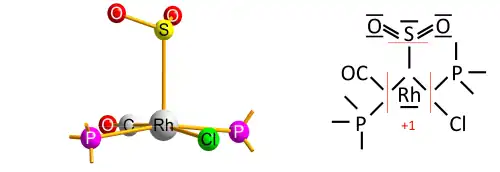
O algoritmo contém uma ressalva, que diz respeito a casos raros de complexos de metal de transição com um tipo de ligante que está ligado reversivelmente como um ácido de Lewis (como um aceitador do par de eletrões do metal de transição); denominado um ligante "tipo Z" no método de classificação de ligação covalente de Green. A ressalva origina-se do uso simplificador da eletronegatividade em vez da fidelidade do eletrão baseada em MO para decidir o sinal iónico.[9] Um exemplo inicial é o complexo O
2S–RhCl(CO)(PPh
3)
2''";[16] com dióxido de enxofre (SO
2) como o ligante aceitador ligado reversivelmente (libertado após aquecimento). A ligação Rh−S é, portanto, extrapolada como iónica contra as eletronegatividades de Allen do ródio e do enxofre, resultando no estado de oxidação +1 para o ródio:
Algoritmo de soma das ordens de ligação
Este algoritmo funciona em estruturas de Lewis e gráficos de ligação de sólidos estendidos (não moleculares):
O estado de oxidação é obtido somando as ordens de ligação heteronuclear no átomo como positivas se esse átomo for o parceiro eletropositivo numa ligação particular e como negativas se não for, e a carga formal do átomo (se houver) é adicionada a essa soma. Aplica-se a mesma ressalva acima.
Aplicado a uma estrutura de Lewis
Um exemplo de uma estrutura de Lewis sem carga formal,
ilustra que, neste algoritmo, as ligações homonucleares são simplesmente ignoradas (as ordens de ligação estão em azul).
O monóxido de carbono exemplifica uma estrutura de Lewis com cargas formais:
Para obter os estados de oxidação, as cargas formais são somadas com o valor da ordem de ligação tomado positivamente no carbono e negativamente no oxigénio.
Aplicado a iões moleculares, este algoritmo considera a localização real da carga formal (iónica), conforme desenhado na estrutura de Lewis. Como exemplo, a soma das ordens de ligação no catião amónio resulta em −4 no nitrogénio de carga formal +1, com os dois números somando-se para o estado de oxidação de −3:
A soma dos estados de oxidação no ião é igual à sua carga (tal como é igual a zero para uma molécula neutra).
Também nos aniões, as cargas formais (iónicas) devem ser consideradas quando não nulas. Para o sulfato, isto é exemplificado com as estruturas esquelética ou de Lewis (topo), comparadas com a fórmula de ordem de ligação de todos os oxigénios equivalentes e cumprindo as regras do octeto e 8 − N (fundo):
Aplicado ao gráfico de ligação
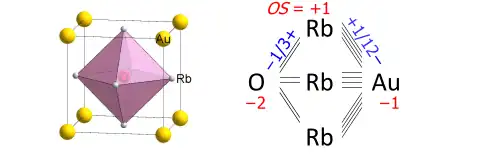
Um gráfico de ligação na química do estado sólido é uma fórmula química de uma estrutura estendida, na qual as conectividades de ligação direta são mostradas. Um exemplo é a perovskita AuORb
3, cuja célula unitária é desenhada à esquerda e o gráfico de ligação (com valores numéricos adicionados) à direita:
Vemos que o átomo de oxigénio se liga aos seis catiões de rubídio mais próximos, cada um dos quais tem 4 ligações com o anião aurieto. O gráfico de ligação resume estas conectividades. As ordens de ligação (também chamadas valências de ligação) somam-se aos estados de oxidação de acordo com o sinal anexo da aproximação iónica da ligação (não há cargas formais nos gráficos de ligação).
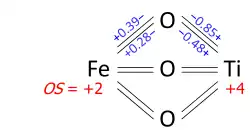
A determinação dos estados de oxidação a partir de um gráfico de ligação pode ser ilustrada na ilmenite, FeTiO
3. Podemos perguntar se o mineral contém Fe2+ e Ti4+, ou Fe3+ e Ti3+. A sua estrutura cristalina tem cada átomo de metal ligado a seis oxigénios e cada um dos oxigénios equivalentes ligado a dois ferros e dois titânios, como no gráfico de ligação abaixo. Os dados experimentais mostram que três ligações metal-oxigénio no octaedro são curtas e três são longas (os metais estão fora do centro). As ordens de ligação (valências), obtidas a partir dos comprimentos de ligação pelo método de valência de ligação, somam 2,01 no Fe e 3,99 no Ti; que podem ser arredondados para os estados de oxidação +2 e +4, respetivamente:
Equilíbrio de redox
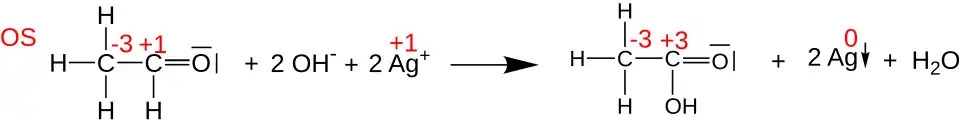
Os estados de oxidação podem ser úteis para equilibrar equações químicas de reações de oxidação-redução (ou redox), porque as mudanças nos átomos oxidados têm de ser equilibradas pelas mudanças nos átomos reduzidos. Por exemplo, na reação do acetaldeído com o reagente de Tollens para formar ácido acético (mostrada abaixo), o átomo de carbono da carbonila muda o seu estado de oxidação de +1 para +3 (perde dois eletrões). Esta oxidação é equilibrada reduzindo dois catiões Ag+
a Ag0
(ganhando dois eletrões no total).
Um exemplo inorgânico é a reação de Bettendorf usando dicloreto de estanho (SnCl
2) para provar a presença de iões arsenito num extrato concentrado de HCl. Quando o arsénio(III) está presente, aparece uma coloração castanha formando um precipitado escuro de arsénio, de acordo com a seguinte reação simplificada:
- 2 As3+
+ 3 Sn2+
→ 2 As0
+ 3 Sn4+
Aqui, três átomos de estanho são oxidados do estado de oxidação +2 para +4, produzindo seis eletrões que reduzem dois átomos de arsénio do estado de oxidação +3 para 0. O equilíbrio simples de uma linha funciona da seguinte forma: os dois pares redox são escritos conforme reagem;
- As3+
+ Sn2+
⇌ As0
+ Sn4+
Um estanho é oxidado do estado de oxidação +2 para +4, um passo de dois eletrões, logo escreve-se 2 à frente dos dois parceiros de arsénio. Um arsénio é reduzido de +3 para 0, um passo de três eletrões, logo 3 vai à frente dos dois parceiros de estanho. Um procedimento alternativo de três linhas consiste em escrever separadamente as semirreações de oxidação e redução, cada uma equilibrada com eletrões, e depois somá-las de modo que os eletrões se anulem. Em geral, estes equilíbrios redox (o equilíbrio de uma linha ou cada semirreação) precisam de ser verificados para que as somas das cargas iónicas e eletrónicas em ambos os lados da equação sejam de facto iguais. Se não forem iguais, iões adequados são adicionados para equilibrar as cargas e o equilíbrio elementar não-redox.
Aparências
Estados de oxidação nominais
Um estado de oxidação nominal é um termo geral com duas definições diferentes:
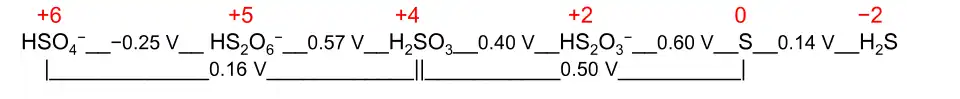
- O estado de oxidação eletroquímico[10]:1060 representa uma molécula ou ião no Diagrama de Latimer ou Diagrama de Frost para o seu elemento redox-ativo. Um exemplo é o diagrama de Latimer para o enxofre a pH 0, onde o estado de oxidação eletroquímico +2 para o enxofre coloca o HS
2O–
3 entre S e o H
2SO
3:
- O estado de oxidação sistemático é escolhido entre alternativas próximas como uma descrição pedagógica. Um exemplo é o estado de oxidação do fósforo no H
3PO
3 (estruturalmente diprótico HPO(OH)
2) tomado nominalmente como +3, enquanto as eletronegatividades de Allen do fósforo e do hidrogénio sugerem +5 por uma margem estreita que torna as duas alternativas quase equivalentes:
- Ambos os números de oxidação alternativos para o fósforo fazem sentido químico, dependendo de qual propriedade química ou reação é enfatizada. Por contraste, uma alternativa calculada, como a média (+4), não faz.
Estados de oxidação ambíguos
As fórmulas de Lewis são aproximações baseadas em regras da realidade química, tal como são as eletronegatividades de Allen. Ainda assim, os estados de oxidação podem parecer ambíguos quando a sua determinação não é direta. Se apenas uma experiência pode determinar o estado de oxidação, a determinação baseada em regras é ambígua (insuficiente). Existem também valores verdadeiramente dicotómicos que são decididos arbitrariamente.
Determinação do estado de oxidação a partir de fórmulas de ressonância
Estados de oxidação aparentemente ambíguos são derivados de um conjunto de fórmulas de ressonância de pesos iguais para uma molécula com ligações heteronucleares onde a conectividade atómica não corresponde ao número de ligações de dois eletrões ditado pela regra 8 − N.[10]:1027 Um exemplo é o S
2N
2, onde quatro fórmulas de ressonância com uma ligação dupla S=N têm estados de oxidação +2 e +4 para os dois átomos de enxofre, que fazem uma média de +3 porque os dois átomos de enxofre são equivalentes nesta molécula de forma quadrada.
Uma medição física é necessária para determinar o estado de oxidação
- quando um ligante não-inocente está presente, de propriedades redox ocultas ou inesperadas que poderiam, de outra forma, ser atribuídas ao átomo central. Um exemplo é o complexo de nquel ditiolato, Ni(S
2C
2H
2)2–
2.[10]:1056–1057 - quando a ambiguidade redox de um átomo central e ligante produz estados de oxidação dicotómicos de estabilidade próxima, pode resultar em tautomerismo termicamente induzido, como exemplificado pelo catecolato de manganês, Mn(C
6H
4O
2)
3.[10]:1057–1058 A atribuição de tais estados de oxidação requer dados espectroscópicos,[17] magnéticos ou estruturais. - quando a ordem de ligação tem de ser apurada juntamente com um tandem isolado de uma ligação heteronuclear e uma homonuclear. Um exemplo é o tiossulfato S
2O2–
3 tendo dois estados de oxidação possíveis (as ordens de ligação estão em azul e as cargas formais em verde):
- A medição da distância S–S no tiossulfato é necessária para revelar que esta ordem de ligação é muito próxima de 1, como na fórmula à esquerda.
Estados de oxidação ambíguos/arbitrários
- quando a diferença de eletronegatividade entre dois átomos ligados é muito pequena (como no H
3PO
3). Dois pares quase equivalentes de estados de oxidação, escolhidos arbitrariamente, são obtidos para estes átomos. - quando um átomo eletronegativo do bloco p forma apenas ligações homonucleares, cujo número difere do número de ligações de dois eletrões sugerido pelas regras. Exemplos são cadeias finitas homonucleares como o N–
3 (o nitrogénio central liga dois átomos com quatro ligações de dois eletrões, enquanto apenas três ligações de dois eletrões[18] são exigidas pela regra 8 − N[10]:1027) ou o I
3 (o iodo central liga dois átomos com duas ligações de dois eletrões, enquanto apenas uma ligação de dois eletrões cumpre a regra 8 − N). Uma abordagem sensata é distribuir a carga iónica pelos dois átomos externos.[10] Tal colocação de cargas num polissulfureto S
n2– (onde todos os enxofres internos formam duas ligações, cumprindo a regra 8 − N) segue-se já da sua estrutura de Lewis.[10] - quando o tandem isolado de uma ligação heteronuclear e uma homonuclear leva a um compromisso de ligação entre duas estruturas de Lewis de ordens de ligação limitantes. Um exemplo é o N
2O:
- O estado de oxidação típico do nitrogénio no N
2O é +1, o que também se obtém para ambos os nitrogénios por uma abordagem de orbital molecular.[13] As cargas formais à direita cumprem as eletronegatividades, o que implica uma contribuição de ligação iónica adicionada. De facto, as ordens de ligação N−N e N−O estimadas são 2,76 e 1,9, respetivamente,[10] aproximando-se da fórmula de ordens de ligação inteiras que incluiria a contribuição iónica explicitamente como uma ligação (em verde):
- Inversamente, cargas formais contra as eletronegatividades numa estrutura de Lewis diminuem a ordem de ligação da ligação correspondente. Um exemplo é o monóxido de carbono com uma estimativa de ordem de ligação de 2,6.[19]
Regras para atribuição do nox
Existem algumas regras práticas para a determinação do estado de oxidação:[20]
- Para um átomo em uma substância simples, seu estado de oxidação é sempre zero. Como os átomos são os mesmos e, portanto, apresentam a mesma eletronegatividade, se ocorresse o rompimento da ligação, nenhum deles doaria ou receberia elétrons. Exemplos: H2, O2, O3, P4, S8.
- Para um íon monoatômico, o número de oxidação é igual à sua carga. Exemplos: Na+ (nox = +1), Ca2+ (nox = +2), Cl- (nox = -1), S2- (nox = -2).
- Os íons dos metais alcalinos (grupo 1A) possuem sempre carga 1+ e portanto número de oxidação igual a +1.
- Exemplos: átomo de sódio no NaCl, átomo de potássio no KNO3.
- Os íons dos metais alcalino-terrosos (grupo 2A) possuem sempre carga 2+ e portanto número de oxidação igual a +2.
- Exemplos: átomo de cálcio no CaCO3, átomo de magnésio no MgCl2.
- O alumínio (Al) possui sempre carga 3+ e portanto número de oxidação igual a +3.
- Exemplo: átomo de alumínio no KAl(SO4)2.
- Para um não-metal, os estados de oxidação são negativos na maioria dos casos.
- O número de oxidação do oxigênio é usualmente -2, tanto em compostos iônicos quanto moleculares. São exceções peróxidos (O22-, os quais possuem nox igual a -1, como no caso do H2O2) e superóxidos (O2-, nox = - 1/2).
- O número de oxidação do hidrogênio é usualmente +1 quando ligado a não-metais (exemplo: HCl) e -1 quando ligado em metais (exemplo: NaH).
- O número de oxidação do flúor é -1 em todos os compostos. Demais halogênios possuem número de oxidação igual a -1 em quase todos os compostos binários (2 elementos). Exemplos: KBr, CaCl2 , CF4. Entretanto, quando combinados com oxigênio, apresentam estados de oxidação positivos, como no caso do NaOCl (nox = +1).
- A soma dos números de oxidação de todos os átomos em um composto neutro é zero. A soma dos números de oxidação de todos os átomos em um íon poliatômico é igual a carga do próprio íon.
- Exemplos: no cloreto de sódio (NaCl), o átomo de cloro possui número de oxidação igual a -1 e o sódio possui número de oxidação igual a +1, totalizando zero;
no íon hidrônio (H3O+), cada um dos átomos de hidrogênio possui número de oxidação igual a +1 e o átomo de oxigênio possui número de oxidação igual a -2, totalizando 1+.
Exemplo prático
Qual o estado de oxidação do átomo de fósforo na molécula de H3PO4?
Por se tratar de uma molécula neutra, a soma dos números de oxidação de cada átomo deve ser igual a zero. São 4 átomos de oxigênio, 3 de hidrogênio e 1 de fósforo. Cada átomo de oxigênio possui nox igual a -2. Cada átomo de hidrogênio possui nox igual a +1. Isso totaliza 4*(-2) + 3*(+1) = -8 + 3 = -5. Portanto, o átomo de fósforo precisa ter carga igual a 5+ para contrabalancear e fazer com que a soma seja zero, tendo nox = +5.
Ver também
Referências
- ↑ IUPAC, Compêndio de Terminologia Química, 2ª ed. ("Gold Book"). Compilado por A. D. McNaught e A. Wilkinson. Blackwell Scientific Publications, Oxford (1997). Versão online: "oxidation state" (2006–) criado por M. Nic, J. Jirat, B. Kosata; atualizações compiladas por A. Jenkins. ISBN 0-9678550-9-8.
- ↑ «Antoine Laurent Lavoisier (1743 – 1794)». GPET Física. Consultado em 12 de julho de 2021
- ↑ EPFL (11 de julho de 2021). «Machine Learning Using Collective Knowledge to Crack the Oxidation States of Crystal Structures». SciTechDaily (em inglês). Consultado em 12 de julho de 2021
- ↑ Wang, G.; Zhou, M.; Goettel, G. T.; Schrobilgen, G. J.; Su, J.; Li, J.; Schlöder, T.; Riedel, S. (2014). «Identification of an iridium-containing compound with a formal oxidation state of IX». Nature. 514 (7523): 475–477. Bibcode:2014Natur.514..475W. PMID 25341786. doi:10.1038/nature13795
- ↑ Yu, Haoyu S.; Truhlar, Donald G. (2016). «Oxidation State 10 Exists». Angewandte Chemie International Edition. 55 (31): 9004–9006. Bibcode:2016ACIE...55.9004Y. PMID 27273799. doi:10.1002/anie.201604670
- ↑ Schroeder, Melanie, Eigenschaften von borreichen Boriden und Scandium-Aluminium-Oxid-Carbiden (em alemão), p. 139, consultado em 24 de fevereiro de 2020, cópia arquivada em 6 de agosto de 2020
- 1 2 Siebring, B. R., Schaff, M. E. (1980). General Chemistry. United States: Wadsworth Publishing Company.
- ↑ Gray, H. B., Haight, G. P. (1967). Basic Principles of Chemistry. Netherlands: W. A. Benjamin.
- 1 2 3 Karen, P.; McArdle, P.; Takats, J. (2016). «Comprehensive definition of oxidation state (IUPAC Recommendations 2016)». Pure Appl. Chem. 88 (8): 831–839. doi:10.1515/pac-2015-1204. hdl:10852/59520
- 1 2 3 4 5 6 7 8 9 10 11 12 Karen, P.; McArdle, P.; Takats, J. (2014). «Toward a comprehensive definition of oxidation state (IUPAC Technical Report)». Pure Appl. Chem. 86 (6): 1017–1081. doi:10.1515/pac-2013-0505
- 1 2 IUPAC, Compêndio de Terminologia Química, 2ª ed. ("Gold Book"). Compilado por A. D. McNaught e A. Wilkinson. Blackwell Scientific Publications, Oxford (1997). Versão online: "{{{título}}}" (2006–) criado por M. Nic, J. Jirat, B. Kosata; atualizações compiladas por A. Jenkins. ISBN 0-9678550-9-8.
- ↑ IUPAC, Compêndio de Terminologia Química, 2ª ed. ("Gold Book"). Compilado por A. D. McNaught e A. Wilkinson. Blackwell Scientific Publications, Oxford (1997). Versão online: "{{{título}}}" (2006–) criado por M. Nic, J. Jirat, B. Kosata; atualizações compiladas por A. Jenkins. ISBN 0-9678550-9-8.
- 1 2 3 Karen, Pavel (2015). «Oxidation State, A Long-Standing Issue!». Angewandte Chemie International Edition. 54 (16): 4716–4726. Bibcode:2015ACIE...54.4716K. PMC 4506524
 . PMID 25757151. doi:10.1002/anie.201407561
. PMID 25757151. doi:10.1002/anie.201407561 - ↑ Hooydonk, G. Van (1 de maio de 1974). «O n an Ionic Approximation to Chemical Bonding». Zeitschrift für Naturforschung A. 29 (5): 763–767. Bibcode:1974ZNatA..29..763H. ISSN 1865-7109. doi:10.1515/zna-1974-0517
- ↑ «Oxidation state». The IUPAC Compendium of Chemical Terminology: The Gold Book. [S.l.: s.n.] 2009. ISBN 978-0-9678550-9-7. doi:10.1351/goldbook.O04365
- ↑ Muir, K. W.; Ibers, J. A. (1969). «The structure of chlorocarbonyl(sulfur dioxide)bis(triphenylphosphine)rhodium, (RhCl(CO)(SO2)(P(C6H5)3 2)». Inorg. Chem. 8 (9): 1921–1928. doi:10.1021/ic50079a024
- ↑ Jørgensen, C. K. (1966). «Electric Polarizability, Innocent Ligands and Spectroscopic Oxidation States». Structure and Bonding. 1. Berlin: Springer-Verlag. pp. 234–248
- ↑ «The Two-Electron Bond». Chemistry LibreTexts. June 25, 2016. Consultado em September 1, 2020. Cópia arquivada em February 9, 2021 Verifique data em:
|acessodata=, |arquivodata=, |data=(ajuda) - ↑ Martinie, R. J.; Bultema, J. J.; Wal, M. N. V.; Burkhart, B. J.; Griend, D. A. V.; DeCock, R. L. (2011). «Bond order and chemical properties of BF, CO, and N2». J. Chem. Educ. 88 (8): 1094–1097. Bibcode:2011JChEd..88.1094M. doi:10.1021/ed100758t
- ↑ Brown, Theodore L. Chemistry, The Central Science 11 ed. [S.l.]: Prentice Hall. p. 137