Polimerização por abertura de anel
Em química de polímeros, polimerização por abertura de anel (PAA) é uma forma de polimerização por crescimento de cadeia, em que a extremidade terminal de um polímero funciona como um centro reativo, em que os monómeros cíclicos adicionais juntam-se para formar uma cadeia maior de polímero por meio de propagação iônica ou radicalar. O tratamento de alguns compostos cíclicos com catalisadores provoca a clivagem do anel, seguido por polimerização para produzir polímeros de alto peso molecular.[1]
A abertura de aneis de monômeros cíclicos é frequentemente levada pelo alívio da tensão causada pelos ângulos de ligação. Portanto, como é o caso para os outros tipos de polimerização, a mudança de entalpia na abertura do anel é negativa. [2]
Monômeros
Vários monômeros cíclicos são sujeitos a PAA.[3]. Isto inclui epóxidos [4][5], trisiloxanos cíclicos, algumas lactonas [4][6] e lactidas [6], anidridos cíclicos [5], carbonatos cíclicos/ésteres de carbonato [7] e aminoácidos N-carboxianidrido. [8][9]. Vários cicloalcenos tensionados, como o norborneno, são monômeros apropriados para a Polimerização por metátese de abertura de anel. Até mesmo aneis de cicloalcanos altamente tensionados, como derivados de ciclopropano[10] e ciclobutano[11] podem sofrer PAA.
História
Polimerização por abertura de anel tem sido praticada desde o início do século XI para produzir polímeros. A síntese de polipeptídeos, que apresenta o histórico mais velho de PAA, foi apresentada no trabalho de Leuchs em 1906.[12] Subsequentemente, a PAA de açúcares anidros deram origem a polissacarídeos como o dextrano, a goma xantana, goma Welan, goma gellan, goma diutan e pululano. Os mecanismos e termodinâmica da polimerização por abertura de anel foram estabelecidos por volta de 1950. [13][14] Os primeiros polímeros de alta massa molecular (Mn de até 105) com uma única unidade repetitiva foram preparados por PAA tão cedo quanto em 1976. [15][16]
Novas pesquisas mostram que a PAA pode ser realizada em ésteres cíclicos com pouco ou sequer o uso de solventes através da utilização de mistura por ressonância acústica.[17]
Uma aplicação industrial é a produção de nylon 6 a partir de caprolactama.
Mecanismos
A PAA pode ser dada através de polimerização radical, aniônica ou catiônica como descrito abaixo.[18] Adicionalmente, a PAA radicalar é útil na produção de polímeros com grupos funcionais incorporados na estrutura principal que não poderiam ser sintetizados através da polimerização em massa de monômeros vinílicos. Como exemplo, a PAA pode produzir polímeros com éteres, ésteres, amidas e carbonatos como grupos funcionais ao longo da cadeia principal.[18][19]
Polimerização aniônica por abertura de anel
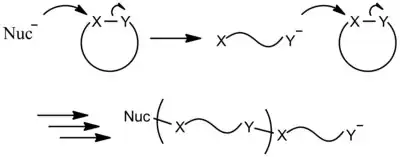
A polimerização aniônica por abertura de anel requer reagentes nucleofílicos como iniciadores. Monômeros com anel de três membros como epóxidos sofrem polimerização aniônica por abertura de anel.[19]
Um exemplo típico de polimerização aniônica por abertura de anel é a polimerização da ε-caprolactona, iniciada por um alcóxido.[19]
Polimerização catiônica por abertura de anel
Iniciadores e intermediários catiônicos caracterizam a polimerização catiônica por abertura de anel. Exemplos de monômeros cíclicos que polimerizam por este mecanismo incluem lactonas, lactamas, aminas e éteres.[20] A polimerização catiônica por abertura de anel pode prosseguir através de uma propagação e crescimento de cadeia do tipo SN1 ou SN2.[18] O mecanismo é afetado pela estabilidade da espécie catiônica formada. Por exemplo, se o átomo com a carga positiva é estabilizado por um grupo doador de elétrons, a polimerização irá prosseguir pelo mecanismo SN1.[19] A espécie catiônica é um heteroátomo e a cadeia cresce pela adição de monômeros cíclicos e, consequentemente, abrindo o sistema de anéis.
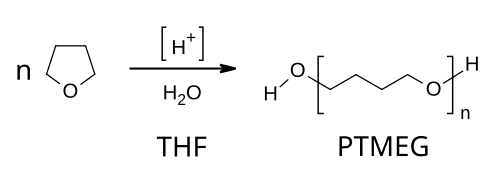
Os monômeros podem ser ativados por ácidos de Brønsted, ions carbênium, íons ônio e cátions metálicos.[18]
A polimerização catiônica por abertura de anel pode ser uma Polimerização Viva e pode ser terminada por reagentes nucleofílicos como ânions fenóxi, fosfinas ou poliânions.[18] Quando a quantidade de monômero se esgota, a terminação pode ocorrer intra ou intermolecularmente. O terminal propagante pode se ligar ao próprio "rabo" da cadeia, formando um macrociclo. Transferências de cadeia alquila também são possíveis, em que o terminal propagante é extinguido pela transferência da cadeia alquílica para outro polímero.
Polimerização por metátese de abertura de anel
A polimerização por métatese de abertura de anel produz polímeros insaturados a partir de cicloalcenos ou bicicloalcenos. A mesma requer catálise organometálica.[18]
O mecanismo para essa via segue caminhos similares às metáteses de olefinas. O processo de iniciação envolve a coordenação do cicloalceno ao complexo metal-alquilideno, seguido de uma cicloadição de tipo [2+2] para formar o intermediário metalociclobutano que ciclicamente reverte para formar uma nova espécie alquilideno.[22][23]
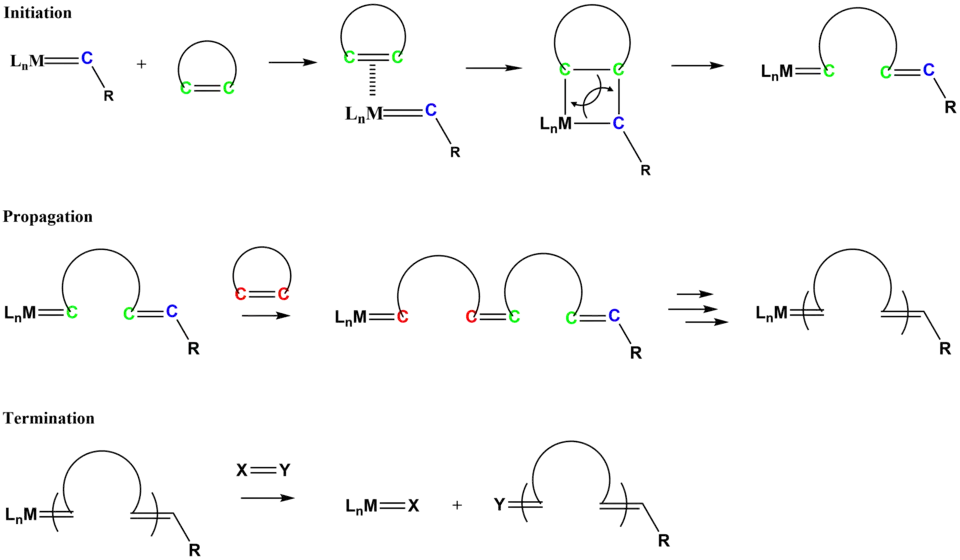
Polímeros insaturados comercialmente relevantes sintetizados através desta técnica incluem polinorborneno, policicloocteno e policiclopentadieno.[24]
Termodinâmica de reação e propagação
O critério termodinâmico formal do potencial de polimerização de um monômero é relacionado ao sinal da entalpia livre (Energia livre de Gibbs) da polimerização: onde:
- x e y indicam os estados do monômero e polímero, respectivamente (x e/ou y = l (líquido), g (gasoso), c (sólido amorfo), c' (sólido cristalino), s (solução));
- ΔHp(xy) é a entalpia de polimerização (Unidade do SI: joule por kelvin);
- ΔSp(xy) é a entropia de polimerização (Unidade do SI: joule);
- T é a temperatura absoluta (Unidade do SI: kelvin).
A entalpia livre de polimerização (ΔGp) pode ser expressada através da soma de entalpia padrão de polimerização (ΔGp°) e um termo relacionado a concentrações instantâneas de moléculas de monômero e macromoléculas em crescimento: em que:
- R é a constante universal dos gases perfeitos;
- M é o monômero;
- (m)i é o monômero em um estado inicial;
- m* é o monômero ativo/espécie propagante.
Seguindo a teoria de solução de Flory-Huggins que consta que a reatividade de um centro ativo localizado em uma macromolécula de uma cadeia macromolecular suficientemente longa não depende do seu grau de polimerização (DPi). Levando em conta que ΔGp° = ΔHp° − TΔSp° (onde ΔHp° e ΔSp° indicam a entropia e entalpia padrões de polimerização, respectivamente), nós obtemos que:
No equilíbrio (ΔGp = 0), quando a polimerização é completa, a concentração de monômero ([M]eq) assume um valor determinado por parâmetros de polimerização padrão (ΔHp° e ΔSp°) e temperatura de polimerização: Por exemplo, tetraidrofurano (THF) não é capaz de polimerizar acima de Tc = 84 °C, assim como o alótropo de enxofre S8 abaixo de Tf = 159 °C.[25][26][27][28] No entanto, para vários monômeros, as temperaturas de polimerização em massa Tc e Tf estão muito acima ou abaixo das temperaturas operáveis de polimerização, respectivamente. A polimerização de uma grande maioria de monômeros é acompanhada por uma redução na entropia devido majoritariamente à perda de graus de liberdade translacionais. Nesta situação, polimerização é termodinamicamente permitida apenas quando a contribuição entálpica em ΔGp prevalece (como consequência, quando ΔHp° < 0 e ΔSp° < 0, a desigualdade |ΔHp| > −TΔSp é um requisito). Portanto, quanto maior a tensão do anel, menor será a concentração resultante de monômero no equilíbrio.
Referências
- ↑ GLOSSAIRE DES TERMES DE BASE EN SCIENCE DES POLYMERES (Recommandations 1996) - www.gfp.asso.fr
- ↑ Young, Robert J. (2011). Introduction to Polymers. Boca Raton: CRC Press. ISBN 978-0-8493-3929-5
- ↑ Nuyken, Oskar; Pask, Stephen (2013). «Ring-Opening Polymerization—An Introductory Review». Polymers. 5 (2): 361–403. doi:10.3390/polym5020361
- ↑ a b Yann Sarazin; Jean-François Carpentier (2015). «Discrete Cationic Complexes for Ring-Opening Polymerization Catalysis of Cyclic Esters and Epoxides». Chemical Reviews. 115 (9): 3564–3614. PMID 25897976. doi:10.1021/acs.chemrev.5b00033
- ↑ a b Longo, Julie M.; Sanford, Maria J.; Coates, Geoffrey W. (2016). «Ring-Opening Copolymerization of Epoxides and Cyclic Anhydrides with Discrete Metal Complexes: Structure–Property Relationships». Chemical Reviews. 116 (24): 15167–15197. PMID 27936619. doi:10.1021/acs.chemrev.6b00553
- ↑ a b JEROME, C; LECOMTE, P (10 de junho de 2008). «Recent advances in the synthesis of aliphatic polyesters by ring-opening polymerization☆». Advanced Drug Delivery Reviews. 60 (9): 1056–1076. ISSN 0169-409X. PMID 18403043. doi:10.1016/j.addr.2008.02.008. hdl:2268/3723
- ↑ Matsumura, Shuichi; Tsukada, Keisuke; Toshima, Kazunobu (May 1997). «Enzyme-Catalyzed Ring-Opening Polymerization of 1,3-Dioxan-2-one to Poly(trimethylene carbonate)». Macromolecules. 30 (10): 3122–3124. Bibcode:1997MaMol..30.3122M. doi:10.1021/ma961862g Verifique data em:
|data=(ajuda) - ↑ Kricheldorf, H. R. (2006). «Polypeptides and 100 Years of Chemistry of α-Amino Acid N-Carboxyanhydrides». Angewandte Chemie International Edition. 45 (35): 5752–5784. PMID 16948174. doi:10.1002/anie.200600693
- ↑ Nikos Hadjichristidis; Hermis Iatrou; Marinos Pitsikalis; Georgios Sakellariou (2009). «Synthesis of Well-Defined Polypeptide-Based Materials via the Ring-Opening Polymerization of α-Amino Acid N-Carboxyanhydrides». Chemical Reviews. 109 (11): 5528–5578. PMID 19691359. doi:10.1021/cr900049t
- ↑ Scott, R. J.; Gunning, H. E. (1952). «The Polymerization of Cyclopropane». J. Phys. Chem. 56 (1): 156–160. doi:10.1021/j150493a031
- ↑ Yokozawa, Tsutomu; Tsuruta, Ei-ichi (1996). «Ring-Opening Polymerization of the Cyclobutane Adduct of Methyl Tricyanoethylenecarboxylate and Ethyl Vinyl Ether». Macromolecules. 29 (25): 8053–8056. Bibcode:1996MaMol..29.8053Y. doi:10.1021/ma9608535
- ↑ Leuchs, H. (1906). «Glycine-carbonic acid». Berichte der Deutschen Chemischen Gesellschaft. 39: 857. doi:10.1002/cber.190603901133
- ↑ Dainton, F. S.; Devlin, T. R. E.; Small, P. A. (1955). «The thermodynamics of polymerization of cyclic compounds by ring opening». Transactions of the Faraday Society. 51: 1710. doi:10.1039/TF9555101710
- ↑ Conix, André; Smets, G. (January 1955). «Ring opening in lactam polymers». Journal of Polymer Science. 15 (79): 221–229. Bibcode:1955JPoSc..15..221C. doi:10.1002/pol.1955.120157918 Verifique data em:
|data=(ajuda) - ↑ Kałuz̀ynski, Krzysztof; Libiszowski, Jan; Penczek, Stanisław (1977). «Poly(2-hydro-2-oxo-1,3,2-dioxaphosphorinane). Preparation and NMR spectra». Die Makromolekulare Chemie. 178 (10): 2943–2947. ISSN 0025-116X. doi:10.1002/macp.1977.021781017
- ↑ Libiszowski, Jan; Kałużynski, Krzysztof; Penczek, Stanisław (June 1978). «Polymerization of cyclic esters of phosphoric acid. VI. Poly(alkyl ethylene phosphates). Polymerization of 2-alkoxy-2-oxo-1,3,2-dioxaphospholans and structure of polymers». Journal of Polymer Science: Polymer Chemistry Edition. 16 (6): 1275–1283. Bibcode:1978JPoSA..16.1275L. doi:10.1002/pol.1978.170160610 Verifique data em:
|data=(ajuda) - ↑ Fowler, Harriet R.; O’Shea, Riley; Sefton, Joseph; Howard, Shaun C.; Muir, Benjamin W.; Stockman, Robert A.; Taresco, Vincenzo; Irvine, Derek J. (10 de fevereiro de 2025). «Rapid, Highly Sustainable Ring-Opening Polymerization via Resonant Acoustic Mixing». ACS Sustainable Chemistry & Engineering. 13 (5): 1916–1926. PMC 11816011
 . PMID 39950108. doi:10.1021/acssuschemeng.4c06330
. PMID 39950108. doi:10.1021/acssuschemeng.4c06330
- ↑ a b c d e f Nuyken, Oskar; Stephen D. Pask (25 April 2013). «Ring-Opening Polymerization—An Introductory Review». Polymers. 5 (2): 361–403. doi:10.3390/polym5020361
 Verifique data em:
Verifique data em: |data=(ajuda) - ↑ a b c d e Dubois, Philippe (2008). Handbook of ring-opening polymerization 1. Aufl. ed. Weinheim: Wiley-VCH. ISBN 978-3-527-31953-4
- ↑ Cowie, John McKenzie Grant (2008). Polymers: Chemistry and Physics of Modern Materials. Boca Raton, Florida: CRC Press. pp. 105–107. ISBN 978-0-8493-9813-1
- ↑ Pruckmayr, Gerfried; Dreyfuss, P.; Dreyfuss, M. P. (1996). «Polyethers, Tetrahydrofuran and Oxetane Polymers». Kirk‑Othmer Encyclopedia of Chemical Technology. John Wiley & Sons
- ↑ Sutthasupa, Sutthira; Shiotsuki, Masashi; Sanda, Fumio (13 October 2010). «Recent advances in ring-opening metathesis polymerization, and application to synthesis of functional materials». Polymer Journal. 42 (12): 905–915. doi:10.1038/pj.2010.94
 Verifique data em:
Verifique data em: |data=(ajuda) - ↑ Hartwig, John F. (2010). Organotransition metal chemistry: from bonding to catalysis. Sausalito, California: University Science Books. ISBN 978-1-891389-53-5
- ↑ Walsh, Dylan J.; Lau, Sii Hong; Hyatt, Michael G.; Guironnet, Damien (25 de setembro de 2017). «Kinetic Study of Living Ring-Opening Metathesis Polymerization with Third-Generation Grubbs Catalysts». Journal of the American Chemical Society (em inglês). 139 (39): 13644–13647. Bibcode:2017JAChS.13913644W. ISSN 0002-7863. PMID 28944665. doi:10.1021/jacs.7b08010
- ↑ Tobolsky, A. V. (July 1957). «Equilibrium polymerization in the presence of an ionic initiator». Journal of Polymer Science. 25 (109): 220–221. Bibcode:1957JPoSc..25..220T. doi:10.1002/pol.1957.1202510909 Verifique data em:
|data=(ajuda) - ↑ Tobolsky, A. V. (August 1958). «Equilibrium polymerization in the presence of an ionic initiator». Journal of Polymer Science. 31 (122): 126. Bibcode:1958JPoSc..31..126T. doi:10.1002/pol.1958.1203112214
 Verifique data em:
Verifique data em: |data=(ajuda) - ↑ Tobolsky, Arthur V.; Eisenberg, Adi (May 1959). «Equilibrium Polymerization of Sulfur». Journal of the American Chemical Society. 81 (4): 780–782. Bibcode:1959JAChS..81..780T. doi:10.1021/ja01513a004 Verifique data em:
|data=(ajuda) - ↑ Tobolsky, A. V.; Eisenberg, A. (January 1960). «A General Treatment of Equilibrium Polymerization». Journal of the American Chemical Society. 82 (2): 289–293. Bibcode:1960JAChS..82..289T. doi:10.1021/ja01487a009 Verifique data em:
|data=(ajuda)