Variabilichromis moorii
Variabilichromis moorii
| |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||
| Estado de conservação | |||||||||||||||||||
 Pouco preocupante (IUCN 3.1) [1] | |||||||||||||||||||
| Classificação científica | |||||||||||||||||||
| |||||||||||||||||||
| Nome binomial | |||||||||||||||||||
| Variabilichromis moorii (Boulenger, 1898) | |||||||||||||||||||
| Sinónimos | |||||||||||||||||||
| |||||||||||||||||||
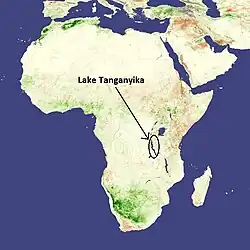
Variabilichromis moorii não tem nome comum e é uma espécie de peixe ciclídeo de água doce endêmico do lago Tanganica, na África oriental. É um peixe pequeno de corpo ovalado, nomeado em homenagem a um dos primeiros coletores de peixes do lago, John Edmund Sharrock Moore [en] (1870–1947), que era citologista, zoólogo, liderou uma expedição ao lago Tanganica e descobriu esta espécie.[2] Os juvenis são geralmente amarelos, e os adultos são de cor marrom-escura a preta.[3] Atinge um comprimento total [en] de 10,3 cm. Atualmente, é o único membro de seu gênero. V. moorii alimenta-se de algas, zooplâncton e invertebrados bentônicos. Também é encontrado no comércio de aquários.[4]
Taxonomia
Variabilichromis moorii é o único membro do gênero Varibilichromis, bem como um membro da tribo Lamprologini [en]. Anteriormente, esteve no gênero Neolamprologus, mas em 1985, Colombé & Allgayer criaram o novo gênero monotípico Variabilichromis para levar em conta uma estrutura óssea supraorbital mais ancestral. Isso foi rejeitado pela classificação de Poll (1986), mas apoiado por Stiassny (1997).[5] A classificação de Stiassny manteve o gênero monotípico devido à estrutura óssea mencionada, bem como à existência de duas outras características que são raras na tribo Lamprilogini: sua dieta inclui algas filamentosas e as fêmeas têm dois ovários funcionais.[6]
Morfologia e coloração

V. moorii exibe dimorfismo sexual, pois as fêmeas adultas tendem a ser maiores que os machos adultos.[3] Os machos adultos muitas vezes têm nadadeiras pélvicas [en], dorsais [en] e anais mais longas do que as fêmeas.[7]

Os adultos são pretos com bordas azuis elétricas em suas nadadeiras caudal, peitorais e dorsais, enquanto os juvenis são amarelos.[6] Geograficamente, eles mostram pouca variação na cor.
Distribuição e habitat
V. moorii é encontrado apenas nas partes do sul do lago Tanganica, na África. Eles são encontrados em áreas rochosas e relativamente rasas na zona litorânea do lago (menos de 10 metros de profundidade).[6] É uma das espécies mais abundantes nesta região do lago.[8]
Reprodução e acasalamento

V. moorii é um reprodutor de substrato, com um casal de macho e fêmea fornecendo cuidado biparental aos seus ovos e aos filhotes após a eclosão.[5] Esta espécie exibe monogamia serial, onde um macho e uma fêmea são monogâmicos por pelo menos um ciclo de desova.[9] Uma fêmea põe de 200 a 500 ovos por ninhada, geralmente sob uma rocha saliente ou dentro de uma fenda de rocha.[5][10] Os ovos levam pelo menos 3 dias para eclodir e as larvas recém-eclodidas têm aproximadamente 3,62 mm de comprimento. Elas permanecem no estágio larval por 4 a 5 dias, presas ao substrato por suas glândulas cefálicas. Elas então se desenvolvem em alevinos de natação livre e nadam em um cardume compacto perto do local de desova. Os pais podem defender a ninhada por até 100 dias, que é quando os alevinos atingem cerca de 3,3 cm de comprimeto.[11]
Sincronicidade lunar na desova
Os ciclos de desova em V. moorii correspondem ao ciclo lunar, com a postura dos ovos ocorrendo pouco antes da lua cheia. Esta periodicidade reprodutiva relacionada à lua é rara em organismos de água doce e muito mais comum em organismos em ambientes marinhos. Esta periodicidade provavelmente evoluiu para diminuir o risco de predação quando os alevinos estão em seus estágios mais vulneráveis (como ovos e larvas), já que a lua está mais brilhante e os pais podem defender melhor contra peixes noturnos comedores de alevinos. Tais predadores noturnos também tendem a evitar ou se afastar da luz e, portanto, caçam menos durante a lua cheia. Esta sincronicidade lunar confere maior benefício a V. moorii em comparação com outras espécies de peixes de água doce devido à localização de V. moorii na zona tropical, onde o luar é mais intenso (já que é mais perpendicular à superfície) e V. moorii tende a viver em águas rasas que são facilmente penetradas pelo luar.[11]
Desova parasitária e paternidade múltipla
V. moorii mostra monogamia social, mas não genética. Os adultos reprodutores desovam de acordo com o ciclo lunar e, portanto, desovam sincronicamente [en] (ver Sincronicidade lunar na desova). Isso permite que os machos desovem em ovos que não pertencem à fêmea com a qual estão acasalados (também conhecido como desova parasitária).[12] Todos os descendentes dentro de uma única ninhada compartilham a mesma mãe, mas não o mesmo pai. Um estudo descobriu que as ninhadas são quase sempre geradas por múltiplos machos (pelo menos dois, mas às vezes mais de dez), uma taxa que é excepcionalmente alta em comparação com outros peixes de acasalamento múltiplo. O macho acasalado com a mãe da ninhada investirá recursos significativos para proteger o território e a ninhada, mesmo que não tenha gerado a maioria dos alevinos. A fêmea está relacionada a toda a ninhada e o macho está relacionado apenas a uma fração da ninhada, então seria esperado que a fêmea fornecesse mais cuidados do que o macho. No entanto, não há grande diferença no cuidado parental masculino e no cuidado parental feminino.[12]
Defesa de território
V. moorii tem territórios individuais para alimentação e territórios compartilhados com um parceiro ao desovar e criar seus filhotes.
Territórios de alimentação
Os territórios individuais de V. moorii são defendidos por seus recursos alimentares e os proprietários do território defenderão mais agressivamente contra indivíduos de espécies com dietas semelhantes, incluindo coespecíficos. Os territórios de alimentação de V. moorii em áreas mais profundas são maiores do que os em áreas rasas. A densidade populacional diminui com o aumento da profundidade, de modo que um grande território em uma área profunda pode ser defendido mais facilmente dos concorrentes do que um território de tamanho semelhante em uma área rasa. Há também menor produtividade de algas em maiores profundidades, porque menos luz está disponível para a fotossíntese, o que também contribui para territórios maiores com o aumento da profundidade.[13]
Territórios de reprodução
Os pais de V. moorii têm um território total defendido que é várias vezes maior do que a área central (que é a área onde os pais passam a maior parte do tempo e onde a ninhada está localizada). O macho e a fêmea dividem o território total em subterritórios aproximadamente iguais, sem muita sobreposição, com a ninhada localizada entre esses dois subterritórios. As fronteiras do subterritório não são fixas e mudam ao longo do dia, dependendo da presença de intrusos. Ao ver um intruso, um dos pais sairá rapidamente do território central para afugentar o intruso.[14] Os pais atacarão coespecíficos, bem como outras espécies de peixes que entrarem no território. Heteroespecíficos são atacados com muito mais frequência do que coespecíficos, e incluem tanto predadores (como Lepidiolamprologus elongatus e Neolamprologus fasciatus) quanto não predadores (como Ophthalmotilapia ventralis e Tropheus moorii, que competem com Variabilichromis moorii por alimento).[14] V. moorii ataca peixes comedores de alevinos que entram em seu território com mais frequência se sua ninhada for maior. Isso é razoável porque os pais têm uma taxa de retorno maior do investimento parental em uma ninhada grande em comparação com uma pequena. Os pais de V. moorii atacam peixes comedores de alevinos com mais frequência do que outros tipos de peixes, o que significa que eles podem concentrar seus esforços defensivos nos peixes mais perigosos para seus alevinos. As taxas de ataque não diminuem significativamente mesmo quando os alevinos envelhecem e crescem, porque o ambiente tem alta pressão de predação e até mesmo alevinos mais velhos serão rapidamente comidos sem a defesa dos pais.[15]
Exploração por Neolamprologus mustax
Os pais de V. moorii tipicamente afugentam outros peixes que entram em seu território, mas são menos agressivos com os membros da espécie de ciclídeo Neolamprologus mustax, que são de cor amarela, assemelhando-se aos alevinos de Variabilichromis moorii. Neolamprologus mustax é o único outro ciclídeo no habitat de Variabilichromis moorii que é amarelo. Experimentos mostraram que V. moorii é mais agressivo com peixes pretos em comparação com peixes amarelos do mesmo tamanho e forma.[16] Neolamprologus mustax alimenta-se de invertebrados bentônicos e prefere se alimentar em territórios de Variabilichromis moorii, onde os invertebrados bentônicos são muito mais abundantes. Isso se deve ao fato de os pais de V. moorii afastarem outras espécies de peixes zoobentívoros, que muitas vezes também predam os alevinos de V. moorii.[17] Ao contrário de outros peixes zoobentívoros, Neolamprologus mustax não preda os alevinos de Variabilichromis moorii; se o fizessem, certamente seriam afugentados.[16]
Referências
- ↑ Bigirimana, C. (2006). «Neolamprologus moorii». Lista Vermelha de Espécies Ameaçadas. 2006. doi:10.2305/IUCN.UK.2006.RLTS.T60613A12384127.en

- ↑ Christopher Scharpf; Kenneth J. Lazara (25 de setembro de 2018). «Order CICHLIFORMES: Family CICHLIDAE: Subfamily PSEUDOCRENILABRINAE (p-y)». The ETYFish Project Fish Name Etymology Database. Christopher Scharpf and Kenneth J. Lazara. Consultado em 2 de fevereiro de 2019
- ↑ a b Borstein, Sam. «Variabilichromis moori (Boulenger, 1898)». Sam Borstein's Cichlids. Consultado em 20 de novembro de 2013
- ↑ Konings, Ad (1996). Back to Nature: Guide to Tanganyika Cichlids. Jonsered, Suécia: Back to Nature. pp. 77, 78. ISBN 978-3-928457-37-8
- ↑ a b c Sturmbauer, Christian; Corinna Fuchs; Georg Harb; Elisabeth Damm; Nina Duftner; Michaela Maderbacher; Martin Koch; Stephan Koblmüller (2008). «Abundance, distribution, and territory areas of rock-dwelling Lake Tanganyika cichlid fish species». Patterns and Processes of Speciation in Ancient Lakes. 615. [S.l.: s.n.] pp. 57–68. ISBN 978-1-4020-9581-8. doi:10.1007/978-1-4020-9582-5_5
- ↑ a b c Borstein, Rick (11 de agosto de 2011). «Variabilochromis moorii». Greater Chicago Cichlid Association. Consultado em 20 de novembro de 2013
- ↑ «Variabilichromis moorii». Seriously Fish. Consultado em 21 de novembro de 2013
- ↑ Takeuchi, Y.; Ochi, H.; Kohda, M.; Sinyinza, D.; Hori, M. (2010). «A 20-year census of a rocky littoral fish community in Lake Tanganyika». Ecology of Freshwater Fish. 19 (2): 239–248. Bibcode:2010EcoFF..19..239T. doi:10.1111/j.1600-0633.2010.00408.x
- ↑ Ota, Kazutaka; Michio Hori; Masanori Kohda (2012). «Testes Investment along a Vertical Depth Gradient in an Herbivorous Fish». Ethology. 118 (7): 683–693. Bibcode:2012Ethol.118..683O. doi:10.1111/j.1439-0310.2012.02056.x
- ↑ Sturmbauer, Christian; Erik Verheyen; Axel Meyer (1994). «Mitochondrial Phylogeny of the Lamprologini, the Major Substrate Spawning Lineage of Cichild Fishes from Lake Tanganyika in Eastern Africa». Molecular Biology and Evolution. 11 (4): 691–703. PMID 8078408. doi:10.1093/oxfordjournals.molbev.a040148

- ↑ a b Rossiter, A (abril de 1991). «Lunar spawning synchroneity in a freshwater fish». Naturwissenschaften. 78 (4): 182–184. Bibcode:1991NW.....78..182R. doi:10.1007/BF01136210
- ↑ a b Sefc, Kristina M.; Karin Mattersdorfer; Christian Sturmbauer; Stephan Koblmüller (2008). «High Frequency of Multiple Paternity in Broods of a Socially Monogamous Cichlid Fish with Biparental Nest Defence». Molecular Ecology. 17 (10): 2531–2543. Bibcode:2008MolEc..17.2531S. PMID 18430146. doi:10.1111/j.1365-294X.2008.03763.x
- ↑ Karino, Kenji (1998). «Depth-related Differences in Territory Size and Defense in the Herbivorous Cichlid, Neolamprologus moorii, in Lake Tanganyika». Ichthyological Research. 45 (1): 89–94. Bibcode:1998IchtR..45...89K. doi:10.1007/BF02678579
- ↑ a b Sturmbauer, Christian; Christoph Hahn; Stephan Koblmüller; Lisbeth Postl; Danny Sinyinza; Kristina M. Sefc (2008). «Variation of territory size and defense behavior in breeding pairs of the endemic Lake Tanganyika cichlid fish Variabilichromis moorii». Patterns and Processes of Speciation in Ancient Lakes. 615. [S.l.: s.n.] pp. 49–56. ISBN 978-1-4020-9581-8. doi:10.1007/978-1-4020-9582-5_4
- ↑ Karino, Kenji (1997). «Influence of Brood Size and Offspring Size on Parental Investment in a Biparental Cichlid Fish, Neolamprologus moorii». Journal of Ethology. 15 (1): 39–43. doi:10.1007/BF02767324
- ↑ a b Ochi, Haruki; Satoshi Awata (2009). «Resembling the Juvenile Colour of Host Cichlid Facilitates Access of the Guest Cichlid to Host Territory». Behaviour. 146 (6): 741–56. doi:10.1163/156853909X446181
- ↑ Ochi, Haruki; Satoshi Awata; Masanori Kohda (2012). «Differential Attack by a Cichlid Fish on Resident and Non-resident Fish of Another Cichlid Species». Behaviour. 149 (1): 99–109. doi:10.1163/156853912X629139