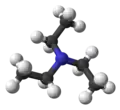
Trietilamina
Trietilamina
| |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||
| Nomes | |||||||||||||
| Nome IUPAC | Triethylamine | ||||||||||||
| Outros nomes | N,N-dietiletanamina TEA TEN N,N,N-Trietilamina | ||||||||||||
| |||||||||||||
| |||||||||||||
| |||||||||||||
| |||||||||||||
| Página de dados suplementares | |||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||
Trietilamina é o composto químico com a fórmula N(CH2CH3)3, comumente abreviada Et3N. É comumente encontrado em síntese orgânica provavelmente porque é a mais simples amina simetricamente trisubstituída, i.e. uma amina terciária, que é líquida a temperatura ambiente. Possui um forte cheiro de peixe reminiscente de amônia. Diisopropiletilamina (base de Hünig, CAS # 7087-68-5) é um relacionado largamente utilizado de trietilamina. Trietilamina é também a doadora do odor das plantas do gênero Crataegus, e do sêmen, entre outros[1]
Trietilamina é comumente empregada em síntese orgânica como uma base, mais frequentemente na preparação de ésteres e amidas de cloretos de acila.[2] Tais reações conduzem à produção de cloreto de hidrogênio o qual combina-se com trietilamina para formar o sal hidrocloreto de trietilamina, comumente chamado cloreto de trietilamônio. Esta reação remove o cloreto de hidrogênio da mistura reacional, o qual é requerido por estas reações para proceder-se a complementação (R, R' = alquila, arila):
- R2NH + R'C(O)Cl + Et3N → R'C(O)NR2 + Et3NH+Cl-
Como outras aminas terciárias, catalisa a formação de espumas de uretano e resinas epóxi. É também útil em reações de deidrohalogenação e oxidações de Swern.
Trietilamina é facilmente alquilada para dar o correspondente sal de quaternário de amônio:
- RI + Et3N → Et3NR+I-
Referências
cscsca\csacasc scacx
Ligações externas
- US EPA - Air Toxics Website (em inglês)