Tricloreto de fósforo
Tricloreto de fósforo
| |||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
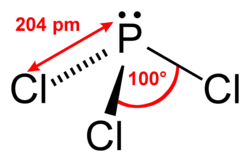 | |||||||||||||||||||||
 | |||||||||||||||||||||
| Nomes | |||||||||||||||||||||
| Nome IUPAC | Phosphorus trichloride | ||||||||||||||||||||
| Outros nomes | Cloreto de fósforo (III) Cloreto de fósforo Tricloreto de monofósforo | ||||||||||||||||||||
| |||||||||||||||||||||
| |||||||||||||||||||||
| |||||||||||||||||||||
| |||||||||||||||||||||
| |||||||||||||||||||||
| Página de dados suplementares | |||||||||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||||||||
Tricloreto de fósforo (fórmula PCl3) é o mais importante dos três cloretos de fósforo. É um importante produto químico industrial, sendo usado para a fabricação de compostos organofosforados para uma grande variedade de aplicações.
propriedades químicas
O fósforo no PCl3 é frequentemente considerado como tendo o estado de oxidação +3 e os átomos de cloro são considerados como estando no estado de oxidação -1. Muito de sua reatividade é consistente com esta descrição.
Reações redox
PCl3 é um precursor para outros compostos de fósforo, através de oxidação a e.g. pentacloreto de fósforo (PCl5), cloreto de tiofosforila (PSCl3), ou oxicloreto de fósforo (POCl3).
Se uma descarga elétrica é passada através de uma mistura de vapor de PCl3 e gás hidrogênio, um raro cloreto de fósforo é formado, tetracloreto de difósforo (P2Cl4).
PCl3 como um eletrófilo
Tricloreto de fósforo é o precursor a compostos organofosforosos que contém um ou mais átomos (P3+), mais notavelmente fosfitos e fosfonatos. Estes compostos normalmente não contém os átomos encontrados no PCl3.
PCl3 reage rápida e exotermicamente com água para formar ácido fosforoso, H3PO3 e HCl. Um grande número de reações de substituição similares são conhecidas, a mais importante das quais é a formação de ésteres fosfitos por reação com álcoois ou fenóis. Por exemplo, com fenol, fosfito de trifenilo é formado:
- 3 PhOH + PCl3 → P(OPh)3 + 3 HCl
onde "Ph" representa o grupo fenil, -C6H5. álcoois tais como o etanol reagem similarmente na presença de uma base tal como:[1]
- PCl3 + 3 EtOH + 3 R3N → P(OEt)3 + 3 R3NH+Cl-
De muitos compostos realcionados que podem ser preparados similarmente, fosfito de triisopropila é um exemplo (p.e. 43.5 °C/1.0 mm; número CAS 116-17-6).
Na ausência de base, entretanto, a reação conduz a um fosfanato de dialquila e um cloreto de alquila, de acordo com a seguinte estequiometria:
- PCl3 + 3 C2H5OH → (C2H5O)2P(=O)H + C2H5Cl + 2 HCl
Aminas, R2NH, formam P(NR2)3, e tióis (RSH) formam P(SR)3. Uma reação industrialmente relevante de PCl3 com aminas é a fosfonometilação, as quais empregam formaldeído:
- R2NH + PCl3 + CH2O → (HO)2P(O)CH2NR2 + 3 HCl
Aminofosfonates são largamente usados como sequentrantes e agentes antiescala em tratamento de água. Um herbicida de grande volume glifosato é também produzido por este meio. A reação de PCl3 com reagentes de Grignard e reagentes organolítios é um método útil para a preparação de fosfinas orgânicas com a fórmula R3P (algumas vezes chamadas fosfanas) tais como trifenilfosfina, Ph3P.
- 3 PhMgBr + PCl3 → Ph3P + 3 MgBrCl
Sob condições controladas PCl3 pode ser usado para preparar PhPCl2 e Ph2PCl.
PCl3 como um nucleófilo
Tricloreto de fósforo tem um "par solitário" (par de elétrons, e conseqüentemente pode atuar como uma base de Lewis, por exemplo com ácidos de Lewis BBr3[2] ele forma um 1:1 aduto, Br3B−−+PCl3. Complexos metálicos tais como Ni(PCl3)4 são conhecidos. Esta bacidade de Lewis é explicada em uma útil rota a compostos organofosforados:
O produto (RPCl3)+ pode então ser decomposto com água para produzir um dicloreto alquilfosfônico RP(=O)Cl2.
Preparação
A produção mundial excede um terço de milhão de toneladas.[3] Tricloreto de fósforo é preparado industrialmente pela reação de cloro com uma solução em refluxo de fósforo branco em tricloreto de fósforo, com contínua remoção de PCl3 à medida que é formado.
A produção industrial de tricloreto de fósforo é controlada sob a Chemical Weapons Convention, onde é listado na schedule 3. Em laboratório pode ser mais conveniente o uso do menos tóxico fósforo vermelho.[4] É suficientemente barato para não ser necessariamente sintetizado para ser uso em laboratório.
O Tricloreto de fósforo é um gás extramente tóxico. Uma pessoas exposta a uma concentração acima de 13Ppm pode morrer. O Tricloreto de fosfóro causa endema pulmonar, parada cardiáca e danos ao sistema sensorial nervoso.
- ↑ «A. H. Ford-Moore and B. J. Perry (1963). "Triethyl Phosphite". Org. Synth.; Coll. Vol. 4: 955.»
- ↑ R. R. Holmes, Journal of Inorganic and Nuclear Chemistry 12, 266-275 (1960).
- ↑ N. N. Greenwood, A. Earnshaw, Chemistry of the Elements, 2nd ed., Butterworth-Heinemann, Oxford, UK, 1997.
- ↑ M. C. Forbes, C. A. Roswell, R. N. Maxson, Inorganic Syntheses, Vol. II, 145-7 (1946).
