Tolerância periférica
Em imunologia, tolerância periférica é o segundo ramo da tolerância imunológica, após a tolerância central. Ela ocorre na periferia imune (depois que as células T e B saem dos órgãos linfoides primários). Seu principal objetivo é garantir que células T e B autorreativas que escaparam da tolerância central não causem doença autoimune.[1] A tolerância periférica também pode servir para prevenir uma resposta imune a antígenos alimentares inofensivos e alérgenos.[2] Mary E. Brunkow, Fred Ramsdell e Shimon Sakaguchi foram agraciados com o Prêmio Nobel de Fisiologia ou Medicina de 2025 "por suas descobertas sobre a tolerância imune periférica".[3]
Células autorreativas estão sujeitas à deleção clonal ou desvio clonal. Ambos os processos de tolerância periférica controlam a presença e produção de células imunes autorreativas.[4] A deleção de células T autorreativas no timo é apenas 60–70% eficiente, e o repertório de células T naive contém uma porção significativa de células T autorreativas de baixa avidez. Essas células podem desencadear uma resposta autoimune, e existem vários mecanismos de tolerância periférica para prevenir sua ativação.[5] Mecanismos antígeno-específicos de tolerância periférica incluem persistência da célula T em quiescência, ignorância do antígeno e inativação direta de células T efetoras por deleção clonal, conversão em células T reguladoras (Tregs) ou indução de anergia.[6][5] Tregs, que também são geradas durante o desenvolvimento de células T no timo, suprimem ainda mais as funções efetoras de linfócitos convencionais na periferia.[7] Células dendríticas (DCs) participam da seleção negativa de células T autorreativas no timo, mas também medeiam a tolerância imune periférica através de vários mecanismos.[8]
A dependência de um antígeno específico na tolerância central ou periférica é determinada por sua abundância no organismo.[9] Células B têm uma probabilidade menor de expressarem marcadores de superfície celular que representem a ameaça de causar um ataque autoimune.[10] A tolerância periférica das células B é amplamente mediada pela dependência das células B na ajuda de células T; no entanto, a tolerância periférica de células B é muito menos estudada.
Células mediadoras da tolerância periférica
Células T reguladoras
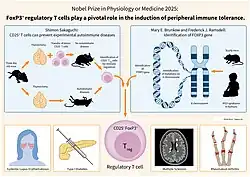
Tregs são as mediadoras centrais da supressão imune, e desempenham um papel fundamental na manutenção da tolerância periférica. O regulador mestre do fenótipo e função das Treg é o Foxp3. Tregs naturais (nTregs) são geradas no timo durante a seleção negativa. O TCR das nTregs mostra alta afinidade por peptídeos próprios. Tregs induzidas (iTreg) se desenvolvem a partir de células T auxiliares naive convencionais após o reconhecimento do antígeno na presença de TGF-β e IL-2. iTregs são enriquecidas no intestino para estabelecer tolerância à microbiota comensal e antígenos alimentares inofensivos.[11] Independentemente de sua origem, uma vez presentes, as Tregs usam vários mecanismos diferentes para suprimir reações autoimunes. Estes incluem depleção de IL-2 do ambiente, secreção de citocinas anti-inflamatórias IL-10, TGF-β e IL-35[12], e indução de apoptose de células efetoras. CTLA-4 é uma molécula de superfície presente nas Tregs que pode prevenir a coestimulação mediada por CD28 de células T após o reconhecimento do antígeno pelo TCR.[7]
DCs tolerogênicas
Células dendríticas (DCs) são uma população celular importante responsável pela iniciação da resposta imune adaptativa. Elas apresentam pequenos peptídeos no MHCII, que são reconhecidos por TCR específicos. Após o encontro com um antígeno com padrões de reconhecimento de perigo ou padrão molecular associado a patógenos, as DCs iniciam a secreção de citocinas pró-inflamatórias, expressam moléculas coestimulatórias CD80 e CD86 e migram para os linfonodos para ativar células T naive.[1] No entanto, DCs imaturas (iDCs) são capazes de induzir tolerância tanto de CD4 quanto de CD8. O potencial imunogênico das iDCs é fraco, devido à baixa expressão de moléculas coestimulatórias e um nível modesto de MHCII. iDCs realizam endocitose e fagocitose de antígenos estranhos e células apoptóticas, o que ocorre fisiologicamente em tecidos periféricos. iDCs carregadas com antígeno migram para os linfonodos, secretam IL-10, TGF-β e apresentam antígeno às células T naive sem coestimulação. Se a célula T reconhece o antígeno, ela é transformada em estado anérgico, depletada ou convertida em Treg.[13] iDCs são indutoras de Treg mais potentes do que DCs residentes no linfonodo.[8] BTLA é uma molécula crucial para a conversão de Treg mediada por DCs.[14] DCs tolerogênicas expressam FasL e TRAIL para induzir diretamente apoptose de células T responsivas. Elas também produzem indoleamina 2,3-dioxigenase (IDO) para prevenir a proliferação de células T. Ácido retinoico é secretado para apoiar a diferenciação de iTreg também.[15] No entanto, após a maturação (por exemplo, durante a infecção), as DCs perdem amplamente suas capacidades tolerogênicas.[13]
LNSCs
Além das células dendríticas, populações celulares adicionais foram identificadas como capazes de induzir tolerância de células T antígeno-específica. Estas são principalmente membros das células estromais de linfonodo (LNSCs). LNSCs são geralmente divididas em várias subpopulações com base na expressão dos marcadores de superfície gp38 (PDPN) e CD31.[16] Entre essas, apenas células reticulares fibrobásticas e células endoteliais linfáticas (LECs) mostraram desempenhar um papel na tolerância periférica. Ambas as populações são capazes de induzir tolerância de células T CD8 pela apresentação de antígenos endógenos em moléculas de MHCI.[17][18] LNSCs não possuem expressão do regulador autoimune, e a produção de autoantígenos depende do fator de transcrição Deaf1. LECs expressam PD-L1 para engajar PD-1 em células T CD8 para restringir a autorreatividade.[19] LNSCs podem direcionar a tolerância de células T CD4 pela apresentação de complexos peptídeo-MHCII, que adquiriram das DCs.[20] Por outro lado, LECs podem servir como reservatório de autoantígenos e podem transportar autoantígenos para DCs para direcionar a apresentação de autopeptídeos-MHCII para células T CD4. Em linfonodos mesentéricos (mLN), LNSCs podem induzir Tregs diretamente pela secreção de TGF-β ou indiretamente pela impressão de DCs residentes em mLN.[19]
Mecanismos intrínsecos de tolerância periférica de células T
Embora a maioria dos clones de células T autorreativas sejam deletados no timo pelos mecanismos de tolerância central, células T autorreativas de baixa afinidade continuamente escapam para a periferia imune.[9] Portanto, existem mecanismos adicionais para prevenir respostas de células T autorreativas e desenfreadas.
Quiescência
Quando as células T naive saem do timo, elas estão em estado de quiescência. Isso significa que estão no estágio não proliferativo, G0 do ciclo celular e têm baixas atividades metabólicas, transcricionais e traducionais, mas ainda retêm a capacidade de entrar no ciclo celular.[21] A quiescência pode prevenir a ativação de células T naive após sinalização tônica, o que significa que as células T podem ser constitutivamente ativadas quando não estão na presença de um ligante.[22] Após a exposição ao antígeno e coestimulação, as células T naive iniciam o processo chamado saída da quiescência, que resulta em proliferação e diferenciação efetora.[23]
Células naive devem entrar e sair de um estado de quiescência no momento adequado em seu ciclo de vida. Se as células T saem da quiescência prematuramente, há uma falta de tolerância a células potencialmente autorreativas. As células T dependem de reguladores negativos para mantê-las em estado de quiescência até que estejam prontas para sair; a regulação negativa de reguladores negativos aumenta a ativação de células T. Ativação prematura e excessiva de células T pode levar a respostas prejudiciais subsequentes e possivelmente desencadear uma resposta autoimune.[24]
À medida que as células saem de um estado de quiescência, elas regularão positivamente enzimas que são responsáveis pela produção de vias essenciais (ácidos nucleicos, proteínas, carboidratos, etc.).[24] Neste estágio, a célula T entrará no ciclo celular e continuará metabolicamente ativa.
Ignorância
Quando células T autorreativas escapam da deleção tímica, elas podem entrar em estado de ignorância.[25] Células T autorreativas podem falhar em iniciar resposta imune após o reconhecimento de autoantígeno. Essas células T não são classificadas como membros disfuncionais da resposta imune; ao contrário, são células naive sem experiência antigênica que permanecerão em circulação.[26] Essas células retêm a capacidade de serem ativadas se na presença dos estímulos corretos.
A ignorância pode ser vista em situações onde não há concentração alta o suficiente de antígeno para desencadear ativação. O mecanismo intrínseco de ignorância é quando a afinidade do TCR ao antígeno é muito baixa para provocar ativação de células T. Há também um mecanismo extrínseco. Antígenos, que estão presentes em números geralmente baixos, não podem estimular células T suficientemente.[1] Adicionalmente, existem barreiras anatômicas que proíbem a ativação dessas células T. Esses mecanismos especializados que garantem ignorância pelo sistema imune se desenvolveram nos chamados órgãos com privilégio imunológico.[6]
Células T podem superar a ignorância através de um sinal suficiente de moléculas sinalizadoras (citocinas, infecção, estímulos inflamatórios, etc.) e induzir uma resposta autoimune.[26] No contexto inflamatório, células T podem sobrepor a ignorância e induzir doença autoimune.[5]
Anergia
Anergia é um estado de não responsividade funcional induzido após o reconhecimento de autoantígeno.[27] Células T podem tornar-se não responsivas a antígenos apresentados se a célula T engaja uma molécula de MHC em uma célula apresentadora de antígeno (sinal 1) sem o engajamento de moléculas coestimulatórias (sinal 2). Moléculas coestimulatórias são reguladas positivamente por citocinas (sinal 3) no contexto de inflamação aguda. Sem citocinas pró-inflamatórias, moléculas coestimulatórias não serão expressas na superfície da célula apresentadora de antígeno, e assim a anergia resultará se houver uma interação MHC-TCR entre a célula T e a APC.[6] A estimulação do TCR leva à translocação do NFAT para o núcleo. Na ausência de coestimulação, não há sinalização de MAPK nas células T e a translocação do fator de transcrição AP-1 para o núcleo é prejudicada. Esse desequilíbrio de fatores de transcrição nas células T resulta na expressão de vários genes envolvidos na formação de um estado anérgico.[28] Células T anérgicas mostram programação epigenética duradoura que silencia a produção de citocinas efetoras. A anergia é reversível e as células T podem recuperar sua responsividade funcional na ausência do antígeno.[5]
Deleção periférica
Antes da liberação na periferia, células T são submetidas à deleção tímica se provarem ter a capacidade de reagir com o próprio. A deleção periférica é o descarte de células T potencialmente autorreativas que escaparam da deleção tímica.[29]
Após a resposta de células T ao antígeno deficiente em coestimulação, uma população menor de células T desenvolve anergia e uma grande proporção de células T é rapidamente perdida por apoptose. Essa morte celular pode ser mediada pelo membro pró-apoptótico intrínseco da família BIM. O equilíbrio entre BIM pró-apoptótico e o mediador antiapoptótico BCL-2 determina o destino final da célula T tolerizada.[5] Existem também mecanismos extrínsecos de deleção mediados pela atividade citotóxica da interação Fas/FasL ou TRAIL/TRAILR.[15] A morte celular pode ser mediada por métodos intrínsecos ou extrínsecos como mencionado. Na maioria dos casos, há uma regulação positiva de marcadores de morte ou a presença de proteínas Bcl-2, que são proteínas essenciais na facilitação da morte celular programada.[29]
Órgãos imunoprivilegiados
Órgãos imunoprivilegiados evoluíram mecanismos nos quais células de tecidos especializados e células imunes podem montar uma resposta apropriada sem perturbar o tecido especializado.[30] Distúrbios imunopatogênicos não estão presentes em uma variedade de órgãos especializados como os olhos, órgãos reprodutivos e o sistema nervoso central. Essas áreas são protegidas por vários mecanismos: expressão de Fas-ligante liga-se ao Fas em linfócitos induzindo apoptose, citocinas anti-inflamatórias (incluindo TGF-beta e interleucina 10) e barreira sangue-tecido com junções de oclusão entre células endoteliais.
Tolerância dividida
Tolerância dividida descreve como alguns antígenos podem desencadear uma resposta imune em um aspecto do sistema imune e o mesmo antígeno não poderia desencadear uma resposta em outro conjunto de células imunes. Como muitas vias da imunidade são interdependentes, elas não precisam todas ser tolerizadas. Por exemplo, células T tolerizadas não ativarão células B autorreativas. Sem essa ajuda das células T CD4, as células B não serão ativadas.[1]
Referências
- ↑ a b c d Janeway, Charles (1 de janeiro de 2001). Immunobiology Five. [S.l.]: Garland Pub. ISBN 978-0-8153-3642-6
- ↑ Soyer, O. U.; Akdis, M.; Ring, J.; Behrendt, H.; Crameri, R.; Lauener, R.; Akdis, C. A. (2013). «Mechanisms of peripheral tolerance to allergens». Allergy. 68 (2): 161–170. ISSN 1398-9995. PMID 23253293. doi:10.1111/all.12085

- ↑ «Nobel Prize in Physiology or Medicine 2025». NobelPrize.org (em inglês). Consultado em 6 de outubro de 2025
- ↑ Xing, Yan; Hogquist, Kristin A. (junho de 2012). «T-Cell Tolerance: Central and Peripheral». Cold Spring Harbor Perspectives in Biology. 4 (6). ISSN 1943-0264. PMC 3367546
 . PMID 22661634. doi:10.1101/cshperspect.a006957
. PMID 22661634. doi:10.1101/cshperspect.a006957
- ↑ a b c d e ElTanbouly, Mohamed A.; Noelle, Randolph J. (abril de 2021). «Rethinking peripheral T cell tolerance: checkpoints across a T cell's journey». Nature Reviews Immunology. 21 (4): 257–267. ISSN 1474-1741. PMID 33077935. doi:10.1038/s41577-020-00454-2
- ↑ a b c Mueller, Daniel L (2010). «Mechanisms maintaining peripheral tolerance». Nature Immunology. 11 (1): 21–27. PMID 20016506. doi:10.1038/ni.1817
- ↑ a b Cretney, Erika; Kallies, Axel; Nutt, Stephen L. (2013). «Differentiation and function of Foxp3+ effector regulatory T cells». Trends in Immunology. 34 (2): 74–80. PMID 23219401. doi:10.1016/j.it.2012.11.002
- ↑ a b Hasegawa, Hitoshi; Matsumoto, Takuya (2018). «Mechanisms of Tolerance Induction by Dendritic Cells In Vivo». Frontiers in Immunology. 9. ISSN 1664-3224. PMC 5834484
 . PMID 29535726. doi:10.3389/fimmu.2018.00350
. PMID 29535726. doi:10.3389/fimmu.2018.00350
- ↑ a b Malhotra, Deepali; Linehan, Jonathan L; Dileepan, Thamotharampillai; Lee, You Jeong; Purtha, Whitney E; Lu, Jennifer V; Nelson, Ryan W; Fife, Brian T; Orr, Harry T; Anderson, Mark S; Hogquist, Kristin A; Jenkins, Marc K (2016). «Tolerance is established in polyclonal CD4+ T cells by distinct mechanisms, according to self-peptide expression patterns». Nature Immunology. 17 (2): 187–195. PMC 4718891
 . PMID 26726812. doi:10.1038/ni.3327
. PMID 26726812. doi:10.1038/ni.3327
- ↑ Getahun, Andrew (maio de 2022). «The role of inhibitory signaling in peripheral B cell tolerance». Immunological Reviews. 307 (1): 27–42. ISSN 0105-2896. PMC 8986582
 . PMID 35128676. doi:10.1111/imr.13070
. PMID 35128676. doi:10.1111/imr.13070
- ↑ Kanamori, Mitsuhiro; Nakatsukasa, Hiroko; Okada, Masahiro; Lu, Qianjin; Yoshimura, Akihiko (1 de novembro de 2016). «Induced Regulatory T Cells: Their Development, Stability, and Applications». Trends in Immunology. 37 (11): 803–811. ISSN 1471-4906. PMID 27623114. doi:10.1016/j.it.2016.08.012
- ↑ Dominguez-Villar, Margarita; Hafler, David A. (julho de 2018). «Regulatory T cells in autoimmune disease». Nature Immunology. 19 (7): 665–673. ISSN 1529-2916. PMC 7882196
 . PMID 29925983. doi:10.1038/s41590-018-0120-4
. PMID 29925983. doi:10.1038/s41590-018-0120-4
- ↑ a b Steinman, Ralph M.; Hawiger, Daniel; Nussenzweig, Michel C. (1 de abril de 2003). «Tolerogenic dendritic cells». Annual Review of Immunology. 21 (1): 685–711. ISSN 0732-0582. PMID 12615891. doi:10.1146/annurev.immunol.21.120601.141040

- ↑ Jones, Andrew; Bourque, Jessica; Kuehm, Lindsey; Opejin, Adeleye; Teague, Ryan M.; Gross, Cindy; Hawiger, Daniel (2016). «Immunomodulatory Functions of BTLA and HVEM Govern Induction of Extrathymic Regulatory T Cells and Tolerance by Dendritic Cells». Immunity. 45 (5): 1066–1077. PMC 5112132
 . PMID 27793593. doi:10.1016/j.immuni.2016.10.008
. PMID 27793593. doi:10.1016/j.immuni.2016.10.008
- ↑ a b Domogalla, Matthias P.; Rostan, Patricia V.; Raker, Verena K.; Steinbrink, Kerstin (2017). «Tolerance through Education: How Tolerogenic Dendritic Cells Shape Immunity». Frontiers in Immunology. 8. ISSN 1664-3224. PMC 5770648
 . PMID 29375543. doi:10.3389/fimmu.2017.01764
. PMID 29375543. doi:10.3389/fimmu.2017.01764
- ↑ Koning, Jasper J.; Mebius, Reina E. (2012). «Interdependence of stromal and immune cells for lymph node function». Trends in Immunology. 33 (6): 264–270. PMID 22153930. doi:10.1016/j.it.2011.10.006
- ↑ Fletcher, Anne L.; Lukacs-Kornek, Veronika; Reynoso, Erika D.; Pinner, Sophie E.; Bellemare-Pelletier, Angelique; Curry, Mark S.; Collier, Ai-Ris; Boyd, Richard L.; Turley, Shannon J. (12 de abril de 2010). «Lymph node fibroblastic reticular cells directly present peripheral tissue antigen under steady-state and inflammatory conditions». Journal of Experimental Medicine. 207 (4): 689–697. ISSN 0022-1007. PMC 2856033
 . PMID 20308362. doi:10.1084/jem.20092642
. PMID 20308362. doi:10.1084/jem.20092642
- ↑ Cohen, Jarish N.; Guidi, Cynthia J.; Tewalt, Eric F.; Qiao, Hui; Rouhani, Sherin J.; Ruddell, Alanna; Farr, Andrew G.; Tung, Kenneth S.; Engelhard, Victor H. (12 de abril de 2010). «Lymph node–resident lymphatic endothelial cells mediate peripheral tolerance via Aire-independent direct antigen presentation». Journal of Experimental Medicine. 207 (4): 681–688. ISSN 0022-1007. PMC 2856027
 . PMID 20308365. doi:10.1084/jem.20092465
. PMID 20308365. doi:10.1084/jem.20092465
- ↑ a b Krishnamurty, Akshay T.; Turley, Shannon J. (abril de 2020). «Lymph node stromal cells: cartographers of the immune system». Nature Immunology. 21 (4): 369–380. ISSN 1529-2916. PMID 32205888. doi:10.1038/s41590-020-0635-3
- ↑ Dubrot, Juan; Duraes, Fernanda V.; Potin, Lambert; Capotosti, Francesca; Brighouse, Dale; Suter, Tobias; LeibundGut-Landmann, Salomé; Garbi, Natalio; Reith, Walter (2 de junho de 2014). «Lymph node stromal cells acquire peptide–MHCII complexes from dendritic cells and induce antigen-specific CD4+ T cell tolerance». Journal of Experimental Medicine. 211 (6): 1153–1166. ISSN 0022-1007. PMC 4042642
 . PMID 24842370. doi:10.1084/jem.20132000
. PMID 24842370. doi:10.1084/jem.20132000
- ↑ Urbán, Noelia; Cheung, Tom H. (1 de fevereiro de 2021). «Stem cell quiescence: the challenging path to activation». Development. 148 (3): dev165084. ISSN 0950-1991. PMC 7888710
 . PMID 33558315. doi:10.1242/dev.165084
. PMID 33558315. doi:10.1242/dev.165084
- ↑ Ajina, Adam; Maher, John (1 de setembro de 2018). «Strategies to Address Chimeric Antigen Receptor Tonic Signaling». Molecular Cancer Therapeutics. 17 (9): 1795–1815. ISSN 1535-7163. PMC 6130819
 . PMID 30181329. doi:10.1158/1535-7163.mct-17-1097
. PMID 30181329. doi:10.1158/1535-7163.mct-17-1097
- ↑ Chapman, Nicole M.; Boothby, Mark R.; Chi, Hongbo (janeiro de 2020). «Metabolic coordination of T cell quiescence and activation». Nature Reviews Immunology. 20 (1): 55–70. ISSN 1474-1741. PMID 31406325. doi:10.1038/s41577-019-0203-y
- ↑ a b Marescal, Océane; Cheeseman, Iain M. (novembro de 2020). «Cellular Mechanisms and Regulation of Quiescence». Developmental Cell. 55 (3): 259–271. PMC 7665062
 . PMID 33171109. doi:10.1016/j.devcel.2020.09.029. hdl:1721.1/138195.2
. PMID 33171109. doi:10.1016/j.devcel.2020.09.029. hdl:1721.1/138195.2
- ↑ Parish, Ian A; Heath, William R (fevereiro de 2008). «Too dangerous to ignore: self-tolerance and the control of ignorant autoreactive T cells». Immunology & Cell Biology. 86 (2): 146–152. ISSN 0818-9641. PMID 18227854. doi:10.1038/sj.icb.7100161
- ↑ a b Schietinger, Andrea; Greenberg, Philip D. (fevereiro de 2014). «Tolerance and exhaustion: defining mechanisms of T cell dysfunction». Trends in Immunology. 35 (2): 51–60. PMC 3946600
 . PMID 24210163. doi:10.1016/j.it.2013.10.001
. PMID 24210163. doi:10.1016/j.it.2013.10.001
- ↑ Kalekar, Lokesh A.; Mueller, Daniel L. (1 de abril de 2017). «Relationship between CD4 Tregs and anergy in vivo». Journal of Immunology. 198 (7): 2527–2533. ISSN 0022-1767. PMC 5363282
 . PMID 28320913. doi:10.4049/jimmunol.1602031
. PMID 28320913. doi:10.4049/jimmunol.1602031
- ↑ Macián, Fernando; Garcı́a-Cózar, Francisco; Im, Sin-Hyeog; Horton, Heidi F.; Michael C.; Rao, Anjana (14 de junho de 2002). «Transcriptional Mechanisms Underlying Lymphocyte Tolerance». Cell. 109 (6): 719–731. ISSN 0092-8674. PMID 12086671. doi:10.1016/S0092-8674(02)00767-5

- ↑ a b Herndon, John M.; Stuart, Patrick M.; Ferguson, Thomas A. (1 de abril de 2005). «Peripheral Deletion of Antigen-Specific T Cells Leads to Long-Term Tolerance Mediated by CD8+ Cytotoxic Cells». The Journal of Immunology. 174 (7): 4098–4104. ISSN 0022-1767. PMID 15778368. doi:10.4049/jimmunol.174.7.4098
- ↑ Streilein, J. Wayne; Takeuchi, Masaharu; Taylor, Andrew W. (fevereiro de 1997). «Immune privilege, T-cell tolerance, and tissue-restricted autoimmunity». Human Immunology. 52 (2): 138–143. PMID 9077562. doi:10.1016/S0198-8859(96)00288-1