Tioacetona
Tioacetona
| |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||
| Nomes | |||||||||||||||||
| Outros nomes |
| ||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| Página de dados suplementares | |||||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||||
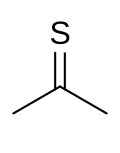
Tioacetona é um composto organossulfurado da família das tiocetonas, de fórmula química (CH3)2C=S. Apresenta-se como um líquido laranja-avermelhado ou castanho, instável acima de −20 °C; nessa faixa, polimeriza-se rapidamente ou converte-se no seu trímero cíclico, a tritioacetona (2,2,4,4,6,6-hexametil-1,3,5-tritiano). É célebre pelo cheiro extremamente forte e repulsivo, considerado o pior já conhecido pela humanidade.[1]
Histórico
A tioacetona foi obtida pela primeira vez em 1889 por Baumann e Fromm como impureza da tritioacetona.[2]
Relatos clássicos do impacto olfativo incluem:
- Freiburg im Breisgau, 1889 – uma tentativa de destilação causou náuseas e desmaios num raio de ≈ 200 m, levando à evacuação parcial da área.[3]
- Esso Research (Reino Unido), 1967 – “quantidades vestigiais tornaram o laboratório e 200m ao redor inabitáveis”.[4]
Estrutura e propriedades
A estrutura é análoga à da acetona (C3H6O), substituindo-se o oxigênio por enxofre (ligação C=S).
| Propriedade | Valor |
|---|---|
| Massa molar | 74,15 g·mol−1 |
| Ponto de fusão | −55 °C |
| Ponto de ebulição | 70 °C (decomp.) |
| Densidade (−20 °C) | 0,94 g·cm−3 |
- Instabilidade – polimeriza-se mesmo a temperaturas sub-zero, formando politioacetona (polímero linear) e tritioacetona (trímero cíclico, p.f. ≈ 24 °C).
- Solubilidade – insolúvel em água; solúvel em solventes orgânicos pouco polares.
Preparação
O método mais comum envolve o craqueamento da tritioacetona [(CH3)2C=S]3 a 500–600 °C:
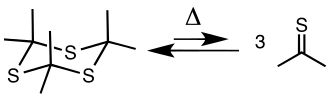
A tritioacetona pode ser obtida por:
- pirólise de sulfeto de alil-isopropila; ou
- reação de acetona com gás sulfídrico (H2S) na presença de um ácido de Lewis.[5]
Polimerização
Mesmo a −78 °C, a tioacetona pode polimerizar, sobretudo na presença de luz ou radicais livres. O polímero apresenta:
- massa molar média: 2 000–14 000 g·mol−1;
- ponto de fusão: 70–125 °C;
- bandas de IV em 2 950, 2 900, 1 440, 1 360–1 375, 1 085 e 643 cm−1.[6]
Odor
Baumann e Fromm descreveram o odor da tioacetona da seguinte forma:
«[…]Nossos esforços nesse sentido fracassaram devido ao fato de que esta substância tem um odor terrível, que se propaga em um tempo surpreendentemente curto e contamina áreas inteiras da cidade. […] Segundo nossas percepções, a intensidade do odor desta substância supera tudo o que se sabe sobre substâncias de cheiro forte a este respeito
— – Baumann, E. y Fromm, E., página 2593
Por não ter aplicação industrial, é manuseada apenas sob atmosfera inerte e temperaturas inferiores a −20 °C, com equipamento de proteção individual completo.
Ver também
- Tiocetona
- Tritioacetona
- Malodorante
Referências
- ↑ Lowe, Derek (11 de junho de 2009). «Things I Won't Work With: Thioacetone». Science (em inglês). Consultado em 20 de julho de 2024
- ↑ Baumann, E.; Fromm, O. (1889). «Über Thioderivate der Ketone». Berichte der Deutschen Chemischen Gesellschaft (em alemão). 22: 1035–1045. doi:10.1002/cber.188902201224
- ↑ «Everything is awesome? Unravelling the world's worst smells». Chemical Communications (em inglês). 2017. pp. 8571–8587. doi:10.1039/C6CC04803J
- ↑ Edwards, D. A.; Filby, R. G. (1967). «Odoriferous organic compounds». Chemistry & Industry (em inglês): 893–894
- ↑ Bailey, W. J.; Chu, H. (1965). «Synthesis of polythioacetone». ACS Polymer Preprints (em inglês). 6: 145–155
- ↑ Sharkey, W. H. (1975). «Polymerization through the carbon–sulfur double bond». Advances in Polymer Science (em inglês). 17. [S.l.: s.n.] pp. 73–103. doi:10.1007/3-540-07111-3_2