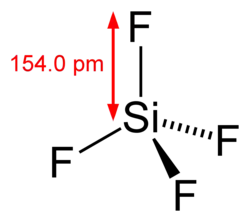
Tetrafluoreto de silício
Silicon tetrafluoride
| |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nomes | |||||||||||||||||
| Nome IUPAC | Tetrafluorosilane Silicon tetrafluoride | ||||||||||||||||
| Outros nomes | Silicon fluoride Fluoro acid air | ||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| Página de dados suplementares | |||||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||||
Tetrafluoreto de silício ou tetrafluorsilano é o composto químico de fórmula SiF4.Essa molécula tetraédrica é notável por ter uma fase líquida "estreita" (seu ponto de ebulição é somente 4°C acima de seu ponto de fusão).Foi sintetizado pela primeira vez por John Davi em 1812.[1]
Síntese
SiF4 é um produto secundário da síntese fertilizantes à base de fosfatos, resultando do ataque do HF em silicatos.Em laboratório, o composto pode ser sintetizado aquecendo-se BaSiF6 (hexafluorosilicato de bário) acima de 300Cº, o SiF4 é volatilizado, deixando um resíduo sólido de BaF2.O BaSiF6 requerido para a reação é obtido pelo tratamento de uma solução aquosa de ácido hexafluorossilícico com cloreto de bário.[2]O análogo GeF4 é preparado similarmente, excepto de que sua temperatura de "quebra" é de 700Cº.[3]
Usos
Esse composto volátil tem usos limitados em microeletrônica e síntese orgânica.[4]
Ocorrência
Plumas vulcânicas tem quantidades significativas de tetrafluoreto de silício, a produção pode chegar á várias toneladas diárias.[5]Parte do tetrafluoreto de silício é hidrolisado para gerar ácido hexafluorossilícico.
Referências
- ↑ John Davy (1812). «An Account of Some Experiments on Different Combinations of Fluoric Acid». Philosophical Transactions of the Royal Society of London. 102: 352–369. ISSN 0261-0523. JSTOR 107324. doi:10.1098/rstl.1812.0020
- ↑ Hoffman, C. J.; Gutowsky, H. S. “Silicon Tetrafluoride” Inorganic Syntheses McGraw-Hill: New York, Volume 4, pages 145-6, 1953.
- ↑ Hoffman, C. J.; Gutowsky, H. S. "Germanium Tetrafluoride” Inorganic Syntheses McGraw-Hill: New York, Volume 4, pages 147-8, 1953.
- ↑ Shimizu, M. "Silicon(IV) Fluoride" Encyclopedia of Reagents for Organic Synthesis, 2001 John Wiley & Sons. DOI: 10.1002/047084289X.rs011
- ↑ T. Mori, M. Sato, Y. Shimoike, K. Notsu (2002). «High SiF4/HF ratio detected in Satsuma-Iwojima volcano's plume by remote FT-IR observation» (PDF). Earth Planets Space. 54: 249–256
| Parte ou a totalidade desta página foi traduzida a partir de «en:Silicon tetrafluoride» da Wikipédia noutra língua em 2011-12-14. |