Sulfeto de potássio
Sulfeto de potássio
| |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||
| Nomes | |||||||||||||||||||
| Nome IUPAC | Potassium sulfide | ||||||||||||||||||
| Outros nomes | Dipotassium monosulfide, Dipotassium sulfide, Potassium monosulfide | ||||||||||||||||||
| |||||||||||||||||||
| |||||||||||||||||||
| |||||||||||||||||||
| |||||||||||||||||||
| |||||||||||||||||||
| Página de dados suplementares | |||||||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||||||
Sulfeto ou sulfureto de potássio é o composto inorgânico de fórmula química K2S. Este sólido incolor quando puro é raramente encontrado, porque reage rapidamente com água, produzindo bissulfeto (KSH) e hidróxido de potássio (KOH).
Estrutura
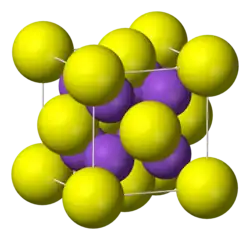
O K2S adota a "estrutura antifluorita", o que significa que os pequenos íons K+ ocupam os sítios tetraédricos fluoreto (F−) na fluorita CaF2, e o íon maior de sulfeto (S2−) ocupa os sítios para Ca2+, octa-coordenados. O Li2S, o Na2S, e o Rb2S cristalizam-se similarmene.[1]
Síntese e reações
Pode ser produzido por aquecimento de K2SO4 com carbono (coque):
- K2SO4 + 4 C → K2S + 4 CO
Em laboratório, uma variedade de métodos existem.[2] K2S forma-se da reação entre enxofre e potássio. No laboratório, esta síntese é usualmente conduzida pela combinação de uma solução de potássio em amônia anidra com o enxofre elementar.
Outro método de obter-se K2S em laboratório envolve a reação de permanganato de potássio e enxofre elementar:
- 2 KMnO4 + S → K2S + 2 MnO2 + 2 O2
Sulfeto é altamente básico, consequentemente K2S hidrolisa completa e irreversivelmente em água de acordo com a seguinte equação:
- K2S + H2O → KOH + KSH
Para muitos propósitos, esta reação é inconsequente dado que a mistura de SH− e OH− comporta-se como uma fonte de S2−. Outros sulfetos de metais alcalinos comportam-se similarmente.[1]