Sulfato de berílio
Sulfato de berílio
| |||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||
 | |||||||||||||||||||||||
| |||||||||||||||||||||||
| |||||||||||||||||||||||
| |||||||||||||||||||||||
| |||||||||||||||||||||||
| Página de dados suplementares | |||||||||||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||||||||||
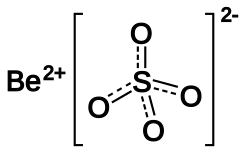
Sulfato de berílio (BeSO4) é um sólido branco cristalino. Foi isolado pela primeira vez em 1815 por Jons Jakob Berzelius.[1][2]
O composto pode ser preparado pelo tratamento de uma solução aquosa de qualquer sal de berílio com ácido sulfúrico e posterior evaporação e cristalização. O sal hidratado se converte na forma anidra pelo aquecimento a 400 °C.[3]
Uma mistura de sulfato de berílio e rádio foi utilizada como fonte de nêutrons na descoberta da fissão nuclear.
Perigo Químico
O sulfato de berílio decompõe-se acima de 550°C, produzindo fumos tóxicos de óxidos de enxofre e óxidos de berílio.[2]
Referências
- ↑ Lathrop Parsons, Charles (1909). The Chemistry and Literature of Beryllium (em inglês). Londres: [s.n.] pp. 29–33
- ↑ a b «ICSC 1351 - SULFATO DE BERÍLIO». chemicalsafety.ilo.org. Consultado em 1 de julho de 2025
- ↑ Patnaik, Pradyot (2002). Handbook of Inorganic Chemicals. [S.l.]: McGraw-Hill. ISBN 0-07-049439-8