Sulfato de antimônio(III)
Sulfato de antimônio(III)
| |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||
| Nomes | |||||||||||||
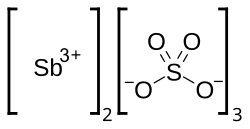
| Nome IUPAC | Sulfato de antimônio(III) | ||||||||||||
| |||||||||||||
| |||||||||||||
| |||||||||||||
| Página de dados suplementares | |||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||
Sulfato de antimônio, Sb2(SO4)3, é um sal higroscópico formado pela reação do antimônio com ácido sulfúrico. O composto é utilizado em dopagem de semicondutores, produção de explosivos e fogos de artifício. [1]
Propriedades Químicas
Sulfato de antimônio é produzido pela reação do ácido sulfúrico com antimônio, entretanto não se forma nitrato de antimônio quando dissolvido em ácido nítrico. Isso se deve à natureza oxidante do ácido nítrico, que forma, com a reação, uma mistura de óxidos de antimônio.[2]
Sulfato de antimônio é deliquescente e solúvel em meio ácido. Pode ser preparado por dissolução de antimônio, trióxido de antimônio, trissulfeto de antimônio ou cloreto de antimonila em ácido sulfúrico concentrado e a quente.[1][2]
- 2 Sb (s) + 6 H2SO4 → Sb2(SO4)3 + 3SO2 + 6 H2O
Precauções
Sulfato de antimônio (III) causa irritação em contato com a pele e mucosas e deve ser manuseado com cuidado. [3]
Referências
- ↑ a b c Herbst, Karl Albert et al. (1985) Antimony and antimony compounds in Ullmann's Encyclopedia of Industral Chemistry 5th ed., vol. A3, p. 70 ISBN 3-527-20103-3
- ↑ a b Nicholas C. Norman. Chemistry of arsenic, antimony, and bismuth. [S.l.]: Springer. pp. 193–. ISBN 978-0-7514-0389-3
- ↑ Antimony(III) Sulfate Material Safety Data Sheet Arquivado em 26 de abril de 2012, no Wayback Machine.. Prochemonline.