Succinato desidrogenase
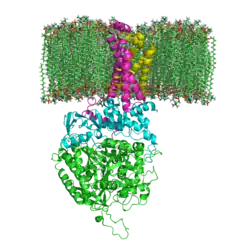
A succinato desidrogenase, succinato-coenzima Q redutase ou complexo II é uma flavoproteína ligada à membrana interna mitocondrial que intervém no ciclo de Krebs e na cadeia respiratória e que contém FAD (dinucleótido de flavina e adenina) unido covalentemente. É a única enzima que participa tanto no ciclo do ácido cítrico como na cadeia de transporte de eletrões.[1] Possui um peso molecular de cerca de 100 kDa, e contém uma molécula de FAD, oito átomos de ferro e oito átomos de enxofre lábeis frente aos ácidos. A enzima possui duas subunidades, cujos pesos moleculares são 30 kDa e 70 kDa respectivamente. A subunidade maior da succinato desidrogenase contém FAD, quatro átomos de ferro e quatro átomos de enxofre ácido-lábeis. A subunidade menor é uma ferro-sulfuro-proteína que contém quatro átomos de ferro e quatro de enxofre ácido-lábeis.
A molécula de FAD da enzima, é o aceitador de electrões da reacção. De maneira general a função bioquímica do FAD é oxidar os alcanos a alcenos, enquanto que o NAD+ oxida os alcóis a aldeídos ou cetonas. Isto é devido a que a oxidação de um alcano (como o succinato) a um alceno (como o fumarato) é suficiente exergónica como para reduzir o FAD a FADH2, mas não para reduzir o NAD+ a NADH. É pouco usual achar uma união covalente entre o FAD e uma proteína; na maioria dos casos, o FAD encontra-se unido à sua enzima associada de forma não covalente (união débil e transitória). Pelo que neste caso o FAD actua como grupo prostético e não como uma coenzima móvel, como o faz normalmente.
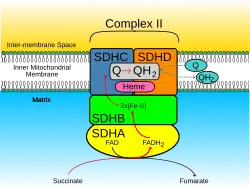
O FADH2 da succinato desidrogenasa, ao não poder desprender-se da enzima, deve oxidar-se novamente in situ. O FADH2 cede seus dois hidrogénios à ubiquinona (coenzima Q) que se reduz a ubiquinol (QH2) e abandona a enzima, difundindo na bicamada lipídica até alcançar o seguinte complexo enzimático da cadeia respiratória.
A succinato desidrogenase actua separando os átomos de hidrogénio que se acham na posição trans dos átomos de carbono metilénicos do succinato.
Esta enzima possui algumas características de uma enzima alostérica: é activada pelo succinato, o fosfato, o ATP e o coenzima Q reduzido , e é inibido pelo malonato, um análogo estrutural do succinato.
Na etapa 8 do ciclo do ácido cítrico, a SQR catalisa a oxidação do succinato a fumarato, enquanto reduz a ubiquinona a ubiquinol. Isto ocorre na membrana interna mitocondrial quando as duas reações estão acopladas.
Estrutura
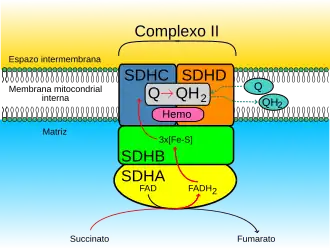
Subunidades
Os monómeros do SQR de mamífeross, mitocôndrias e muitas bactériass são compostos por quatro subunidades proteicas: duas hidrofílicas e duas hidrofóbicas. As duas primeiras subunidades, uma flavoproteína (SdhA) e uma proteína ferro-enxofre (SdhB), são hidrófilas.
A SdhA contém um cofactor (grupo prostético de dinucleótido de flavina e adenina (FAD) ligado covalentemente e o sítio de ligação para o succinato. Além disso, a SdhB contém três clusters ferro-enxofre: [2Fe-2S], [4Fe-4S] e [3Fe-4S]. As outras duas subunidades são subunidades de ancoragem de membrana hidrofóbicas denominadas SdhC e SdhD. As mitocôndrias humanas contêm duas isoformas diferentes de SdhA (subunidades Fp tipo I e tipo II); estas isoformas também se encontram nos vermes Ascaris suum e Caenorhabditis elegans.[2] As subunidades formam um complexo de citocromo b ligado à membrana com seis hélices transmembranares contendo um grupo heme B e um sítio de ligação para a ubiquinona. Encontram-se também nas subunidades SdhC e SdhD duas moléculas de fosfolípidos, uma de cardioolipina e uma de fosfatidiletanolamina, que ocupam o espaço hidrofóbico abaixo do heme B. A envolver SdhC e SdhD está a bicamada lipídica/membrana fosfolipídica, sendo o espaço intermembranar visível na parte superior da primeira e da segunda imagens do artigo.[3]
Sítio de ligação da ubiquinona
O sítio de ligação da ubiquinona está localizado numa lacuna formada por SdhB, SdhC e SdhD. A ubiquinona é estabilizada pelas cadeias laterais da histidina 207 da subunidade B, da serina 27 e da arginina 31 da subunidade C e da tirosina 83 da subunidade D. O anel quinona é envolvido pela isoleucina 28 da subunidade C e pela prolina 160 da subunidade C. B. Estes resíduos, juntamente com o Ile209, o Trp163 e o Trp164 da subunidade B e Ser27 da subunidade C, formam o ambiente hidrofóbico da bolsa de ligação da quinona.[4]
Sítio de ligação do succinato
O SdhA fornece o sítio de ligação para a oxidação do succinato. As cadeias laterais da treonina Thr254, His354 e Arg399 da subunidade A estabilizam a molécula enquanto o FAD oxida e transporta os electrões para o primeiro "cluster" ferro-enxofre, o 2Fe-2S.[5]
Centros redox
O centro de ligação do succinato e o centro de ligação da ubiquinona estão ligados por uma cadeia de centros redox que inclui os clusters FAD e ferro-enxofre. Esta cadeia estende-se pelo monómero ao longo de aproximadamente 40 Å. Todas as distâncias entre as fronteiras dos centros são inferiores ao limite de 14 Å sugerido para a transferência fisiológica de electrões.[3]
Mecanismo
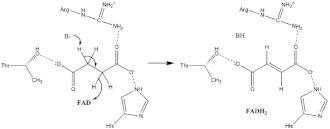
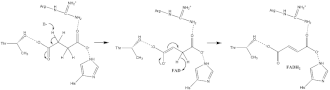
Oxidação do succinato
Pouco se sabe sobre o mecanismo exato da oxidação do succinato. No entanto, a estrutura cristalina obtida a partir do complexo mostra que o FAD, Glu255, Arg286 e His242 da subunidade A são bons candidatos para a reação inicial de desprotonação. Existem dois mecanismos de eliminação possíveis, designados por E2 ou E1cb. Na eliminação E2, o mecanismo é coordenado. O resíduo básico ou cofator desprotona o carbono alfa, e o FAD aceita o hidreto do carbono beta, oxidando o succinato ligado, que se transforma em fumarato. No mecanismo E1cb, forma-se um intermediário enolato antes do FAD aceitar o hidreto. São necessárias mais pesquisas para determinar qual o mecanismo de eliminação que afeta o succinato na succinato desidrogenase. O fumarato oxidado, agora fracamente ligado ao sítio activo, está livre para abandonar a proteína e passar para a matriz mitocondrial.
Tunelamento de electrões
Após os eletrões serem derivados da oxidação do succinato pelo FAD, são tunelados ao longo dos centros ferro-enxofre até atingirem o cluster final [3Fe-4S]. Estes eletrões são depois transferidos para uma molécula de ubiquinona no sítio ativo. O sistema de tunelamento de eletrões ferro-enxofre é apresentado na última imagem.
Redução da ubiquinona
[[Ficheiro:Succinate Dehydrogenase 1YQ3 Electron Carriers Labeled.png|miniatura|280px |Transportadores de eletrões do complexo SQR. FADH₂, centros ferro-enxofre, heme B e ubiquinona.
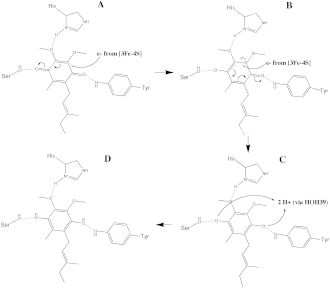
O oxigénio carbonílico O1 da ubiquinona está orientado no sítio ativo através de interações de ligação de hidrogénio com a Tyr83 da subunidade D. A presença de eletrões no cluster ferro-enxofre [3Fe-4S] induz o movimento da ubiquinona para uma segunda orientação. Isto facilita uma segunda interação de ligação de hidrogénio entre o grupo carbonilo O4 da ubiquinona e a Ser27 da subunidade C. Após a primeira etapa de redução de um único eletrão, forma-se um radical semiquinona. O segundo eletrão chega do cluster [3Fe-4S] e provoca a redução completa da ubiquinona a ubiquinol. Este mecanismo de redução da ubiquinona é apresentado na imagem correspondente.
Grupo prostético heme
Embora a funcionalidade do heme na succinato desidrogenase ainda necessite de ser mais investigada, alguns estudos concluíram que o primeiro eletrão que passa do cluster [3Fe-4S] para a ubiquinona pode ser tunelado de um lado para o outro entre o heme e o intermediário ubiquinona. Desta forma, o cofator heme atua como um sumidouro de eletrões. O seu papel é impedir a interação do intermediário com o oxigénio molecular, o que produziria espécies reativas de oxigénio.
Foi proposto que existe um mecanismo de controlo que pode impedir que os eletrões tunelem diretamente do cluster [3Fe-4S] para o heme. Um potencial candidato é o resíduo His207, que se localiza entre o cluster e o heme. O His207 da subunidade B está em estreita proximidade com o cluster [3Fe-4S], a ubiquinona ligada e o heme; e poderia modular o fluxo de eletrões entre estes centros redox.[6]
Transferência de protões
A redução completa da quinona na SQR requer dois eletrões e dois protões. Foi proposto que uma molécula de água (HOH39) chega ao sítio ativo e é coordenada pela His207 da subunidade B, Arg31 da subunidade C e Aspartato82 da subunidade D. A semiquinona é protonada pelos protões da HOH39, completando a redução da ubiquinona a ubiquinol. A His207 e a Asp82 provavelmente facilitam este processo. Outros estudos sugerem que a Tyr83 da subunidade D está coordenada a uma histidina próxima e ao oxigénio carbonílico O1 da ubiquinona. O resíduo de histidina diminui o pKa da tirosina, facilitando a doação do seu protão ao intermediário ubiquinona reduzido. == Inibidores ==
Existem duas classes de inibidores do Complexo II: os que se ligam ao sítio de ligação do succinato e os que se ligam ao sítio de ligação da ubiquinona. Os inibidores do tipo ubiquinona incluem o ácido carboxílico e a feniltrifluoroacetona. Os inibidores análogos do succinato incluem, por exemplo, o composto sintético malonato e os intermediários do ciclo do ácido cítrico malato e oxalacetato. O oxalacetato é um dos inibidores mais potentes do Complexo II. Não se compreende completamente como é que um intermediário comum do ciclo do ácido cítrico pode inibir o Complexo II, mas pode desempenhar um papel protetor na minimização da produção de superóxido mediada pela transferência inversa de eletrões pelo Complexo I.[7]
Os inibidores do tipo ubiquinona têm sido utilizados como fungicidas na agricultura desde a década de 1960. A carboxina era utilizada principalmente para controlar doenças das plantas causadas por fungos basidiomicetos. Mais recentemente, foram desenvolvidos outros compostos com um espectro de ação mais alargado contra uma variedade de agentes patogénicos de plantas, como o boscalid, o penthiopyrad e o fluopiram.[8] Alguns fungos importantes como as pragas agrícolas não são sensíveis aos inibidores da ubiquinona de nova geração.[9]
Doenças
O papel fundamental da succinato-coenzima Q redutase na cadeia de transporte de eletrões das mitocôndrias torna-a vital para a maioria dos organismos multicelulares, e a deleção desta enzima do genoma demonstrou ser letal para os ratinhos na fase embrionária.
- As mutações no gene SdhA podem causar síndrome de Leigh, encefalopatia mitocondrial e atrofia óptica.
- Mutações no gene SdhB podem causar tumorigénese nas células cromafins, resultando em paraganglioma hereditário e feocromocitoma hereditário. Os tumores são geralmente malignos. Podem também reduzir a esperança de vida e aumentar a produção de iões superóxido.
- As mutações no gene SdhC podem resultar numa diminuição da esperança de vida, aumento da produção de iões superóxido e causar paraganglioma e feocromocitoma hereditários. Nestes casos, os tumores tendem a ser benignos. Estas mutações são incomuns.
- As mutações no gene SdhD podem também causar paraganglioma e feocromocitoma hereditários. Os tumores tendem a ser benignos e ocorrem geralmente na cabeça e no pescoço. Estas mutações podem também diminuir a esperança de vida e aumentar a produção de iões superóxido.
A succinato desidrogenase em mamíferos não atua apenas na geração de energia mitocondrial, mas também desempenha um papel na deteção de oxigénio e na supressão tumoral; sendo, por isso, objeto de pesquisas em curso.
Referências
- ↑ Oyedotun KS, Lemire BD (2004). «The quaternary structure of the Saccharomyces cerevisiae succinate dehydrogenase. Homology modeling, cofactor docking, and molecular dynamics simulation studies». J. Biol. Chem. 279 (10): 9424–31. PMID 14672929. doi:10.1074/jbc.M311876200
- ↑ Tomitsuka E, Hirawake H, Goto Y, Taiwaki M, Harada S, Kita K (2003). «Direct evidence for two distinct forms of the flavoprotein subunit of human mitochondrial complex II (succinate-ubiquinone reductase)». J. Biochem. 134 (2): 191–5. PMID 12966066. doi:10.1093/jb/mvg144
- ↑ a b Yankovskaya V, Horsefield R, Törnroth S; et al. (2003). «Architecture of succinate dehydrogenase and reactive oxygen species generation». Science. 299 (5607): 700–4. PMID 12560550. doi:10.1126/science.1079605
- ↑ Horsefield R, Yankovskaya V, Sexton G; et al. (2006). «Structural and computational analysis of the quinone-binding site of complex II (succinate-ubiquinone oxidoreductase): a mechanism of electron transfer and proton conduction during ubiquinone reduction». J. Biol. Chem. 281 (11): 7309–16. PMID 16407191. doi:10.1074/jbc.M508173200
- ↑ Kenney WC (1975). «The reaction of N-ethylmaleimide at the active site of succinate dehydrogenase». J. Biol. Chem. 250 (8): 3089–94. PMID 235539
- ↑ Tran QM, Rothery RA, Maklashina E, Cecchini G, Weiner JH (2006). «The quinone binding site in Escherichia coli succinate dehydrogenase is required for electron transfer to the heme b». J. Biol. Chem. 281 (43): 32310–7. PMID 16950775. doi:10.1074/jbc.M607476200
- ↑ Muller FL, Liu Y, Abdul-Ghani MA; et al. (2008). «High rates of superoxide production in skeletal-muscle mitochondria respiring on both complex I- and complex II-linked substrates». Biochem. J. 409 (2): 491–9. PMID 17916065. doi:10.1042/BJ20071162
- ↑ Avenot, H. F.; Michailides, T. J. (2010). "Progress in understanding molecular mechanisms and evolution of resistance to succinate dehydrogenase inhibiting (SDHI) fungicides in phytopathogenic fungi". Crop Protection 29 (7): 643. doi:10.1016/j.cropro.2010.02.019.
- ↑ Dubos, T.; Pasquali, M.; Pogoda, F.; Casanova, A. L.; Hoffmann, L.; Beyer, M. (2013). "Differences between the succinate dehydrogenase sequences of isopyrazam sensitive Zymoseptoria tritici and insensitive Fusarium graminearum strains". Pesticide Biochemistry and Physiology 105: 28. [ http://www.sciencedirect.com/science/article/pii/S0048357512001769 doi 10.1016/j.pestbp.2012.11.004].