SDS-PAGE
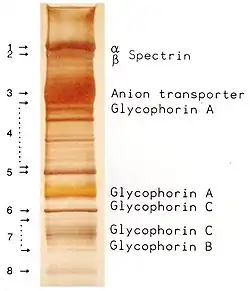
A SDS-PAGE (do inglês sodium dodecyl sulfate–polyacrylamide gel electrophoresis ou eletroforese em gel de poliacrilamida com dodecil sulfato de sódio) é uma das variantes da eletroforese em gel de poliacrilamida, um método analítico usado em bioquímica para a separação de moléculas carregadas em misturas pela sua massa molecular num campo elétrico. Utiliza o dodecil sulfato de sódio (SDS) para ajudar a identificar e isolar moléculas de proteínas. A SDS-PAGE é um sistema eletroforético descontínuo desenvolvido por Ulrich K. Laemmli, que se utiliza habitualmente como método para separar proteínas de massas moleculares entre 5 e 250 KDa.[1] A publicação que a descreve é o artigo mais frequentemente citado de um único autor e o segundo mais citado globalmente.[2]
Propriedades
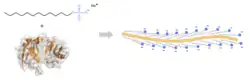

A SDS-PAGE é um método eletroforético com o qual se podem separar proteínas pela sua massa. O meio (ou matriz) no qual se realiza é um gel descontínuo baseado na poliacrilamida. Além disso, utiliza-se o surfactante SDS (dodecil sulfato de sódio). A cada grama de proteína ligam-se cerca de 1,4 gramas de SDS,[3][4][5] o que corresponde a uma molécula de SDS por cada dois aminoácidos da proteína. O SDS atua como um surfactante, que cobre as proteínas dando-lhes uma proporção muito similar de carga-massa. As cargas intrínsecas que as proteínas tinham são desprezíveis em comparação com as que o SDS lhes confere, e as cargas positivas são também reduzidas no intervalo de pH básico de um gel separador. Com a aplicação de um campo elétrico constante, as proteínas migram em direção ao ânodo, cada uma com uma diferente mobilidade, dependendo da sua massa. Este procedimento simples permite a separação precisa das proteínas pela massa sem que as cargas intrínsecas originais da proteína influenciem.
O SDS tende a formar micelas esféricas em soluções aquosas acima de certa concentração chamada concentração micelar crítica (CMC). Acima de uma concentração micelar crítica de 7 a 10 milimolar em soluções aquosas, o SDS aparece como moléculas separadas (monómero) e como micelas, mas abaixo da CMC o SDS existe apenas como monómero em soluções aquosas. Na CMC, uma micela é composta por cerca de 62 moléculas de SDS.[6] No entanto, apenas os monómeros de SDS se ligam a proteínas e fazem-no através de interações hidrofóbicas, enquanto as micelas de SDS são aniónicas na parte exterior e não se adsorvem a nenhuma proteína.[3] O SDS é de natureza anfipática, o que permite que se desdobre tanto os segmentos polares como os não polares da estrutura das proteínas.[7] A concentrações de SDS superiores a 0,1 milimolar, começa o desdobramento das proteínas,[3] e acima de 1 mM, a maioria das proteínas são desnaturadas.[3] Devido ao forte efeito desnaturante do SDS e à subsequente dissociação dos complexos proteicos, as estruturas quaternárias geralmente não podem ser determinadas usando SDS. São exceções, por exemplo, as proteínas que foram previamente estabilizadas por ligações cruzadas covalentes e os complexos proteicos resistentes ao SDS, que são estáveis mesmo na presença de SDS (esto último apenas à temperatura ambiente). Para desnaturar os complexos resistentes ao SDS é necessária uma alta energia de ativação, que se consegue aquecendo. A resistência ao SDS é baseada na metaestabilidade do dobramento das proteínas. Embora a proteína nativa completamente dobrada resistente ao SDS não tenha suficiente estabilidade na presença de SDS, o equilíbrio químico da desnaturação à temperatura ambiente ocorre lentamente. Os complexos de proteínas estáveis caracterizam-se não só pela resistência ao SDS, mas também pela estabilidade contra as proteases e um aumento da semi-vida biológica.[8]
Alternativamente, a eletroforese em gel de poliacrilamida pode ser realizada também com os surfactantes catiónicos CTAB numa CTAB-PAGE,[9][10][11] ou o 16-BAC numa BAC-PAGE.[12]
Referências
- ↑ Laemmli, U. K. (1970). «Cleavage of Structural Proteins during the Assembly of the Head of Bacteriophage T4». Nature. 227 (5259): 680–685. ISSN 0028-0836. doi:10.1038/227680a0
- ↑ «Interview with Ulrich Lämmli in German». Neue Zürcher Zeitung: NZZ Folio, No. 11. 2005. Consultado em 4 de março de 2012
- ↑ a b c d Reynolds JA, Charles Tanford (1970). «Binding of dodecyl sulfate to proteins at high binding ratios. Possible implications for the state of proteins in biological membranes.». Proc Natl Acad Sci U S A. 66 (3): 1002–7. PMC 283150
 . PMID 5269225. doi:10.1073/pnas.66.3.1002 Erro no estilo Vancouver: wikilink (ajuda)
. PMID 5269225. doi:10.1073/pnas.66.3.1002 Erro no estilo Vancouver: wikilink (ajuda)
- ↑ Smith, B. J. (1984). «SDS Polyacrylamide Gel Electrophoresis of Proteins». 1: 41–56. doi:10.1385/0-89603-062-8:41
- ↑ Staikos, Georgios; Dondos, Anastasios (2009). «Study of the sodium dodecyl sulphate–protein complexes: evidence of their wormlike conformation by treating them as random coil polymers». Colloid and Polymer Science. 287 (8): 1001–1004. ISSN 0303-402X. doi:10.1007/s00396-009-2059-3
- ↑ Turro, Nicholas J.; Yekta, Ahmad (1978). «Luminescent probes for detergent solutions. A simple procedure for determination of the mean aggregation number of micelles». Journal of the American Chemical Society. 100 (18): 5951–5952. ISSN 0002-7863. doi:10.1021/ja00486a062
- ↑ 1958-, Berg, Jeremy M. (Jeremy Mark),. Biochemistry. Tymoczko, John L., 1948-, Gatto, Gregory J., Jr. (Gregory Joseph), Stryer, Lubert. Eighth ed. New York: [s.n.] ISBN 9781464126109. OCLC 913469736
- ↑ Manning M, Colón W (2004). «Structural basis of protein kinetic stability: resistance to sodium dodecyl sulfate suggests a central role for rigidity and a bias toward beta-sheet structure.». Biochemistry. 43 (35): 11248–54. PMID 15366934. doi:10.1021/bi0491898
- ↑ Buxbaum, Engelbert (2003). «Cationic electrophoresis and electrotransfer of membrane glycoproteins». Analytical Biochemistry. 314 (1): 70–76. ISSN 0003-2697. doi:10.1016/S0003-2697(02)00639-5
- ↑ Akin, Dianne T.; Shapira, Raymond; Kinkade, Joseph M. (1985). «The determination of molecular weights of biologically active proteins by cetyltrimethylammonium bromide-polyacrylamide gel electrophoresis». Analytical Biochemistry. 145 (1): 170–176. ISSN 0003-2697. doi:10.1016/0003-2697(85)90343-4
- ↑ Simpson, R. J. (2010). «CTAB-PAGE». Cold Spring Harbor Protocols. 2010 (4): pdb.prot5412–pdb.prot5412. ISSN 1559-6095. doi:10.1101/pdb.prot5412
- ↑ Hartinger, Joachim; Stenius, Katinka; Högemann, Dagmar; Jahn, Reinhard (1996). «16-BAC/SDS–PAGE: A Two-Dimensional Gel Electrophoresis System Suitable for the Separation of Integral Membrane Proteins». Analytical Biochemistry. 240 (1): 126–133. ISSN 0003-2697. doi:10.1006/abio.1996.0339
Ligações externas
- Protocolo para SDS-PAGE com BisTris em OpenWetWare.org