Perclorato de magnésio
Perclorato de magnésio
| |||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||
| |||||||||||||||||||||
| |||||||||||||||||||||
| |||||||||||||||||||||
| |||||||||||||||||||||
| Página de dados suplementares | |||||||||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||||||||
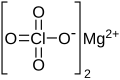
O perclorato de magnésio é um composto inorgânico de fórmula química . Trata-se de um sólido branco, altamente higroscópico e um forte agente oxidante.[1] É comercializado principalmente como agente dessecante sob o nome comercial anidrona (em inglês, Anhydrone), sendo tradicionalmente empregado na secagem de gases em análises laboratoriais.
O composto existe tanto na forma anidra quanto em diversos hidratos, sendo o hexahidratado, , o mais comum em condições ambiente.
Propriedades
O composto apresenta solubilidade muito elevada em água e possui ponto eutético bastante baixo, permitindo que soluções concentradas permaneçam líquidas até cerca de –64 °C[2]. Sua decomposição ocorre na temperatura de 250 ⁰C.[3]
O ânion perclorato () possui geometria tetraédrica e tamanho semelhante ao íon sulfato (), motivo pelo qual os percloratos de metais alcalino-terrosos geralmente exibem estruturas cristalinas semelhantes às dos sulfatos. Apesar dessa semelhança estrutural, os percloratos são quimicamente distintos e caracterizam-se pelo forte poder oxidante.[4]
Devido a esse caráter oxidante, o perclorato de magnésio não deve entrar em contato com materiais orgânicos secos, pois choques mecânicos, atrito ou aquecimento podem ocasionar combustão ou explosão[4].
Preparação
Os percloratos hidratados dos metais alcalino-terrosos podem ser obtidos a partir dos óxidos, carbonatos, cloretos ou nitratos correspondentes. Esses materiais são dissolvidos em quantidade ligeiramente superior ao necessário de ácido perclórico a 70%. No caso dos óxidos, emprega-se um pequeno excesso do sólido, que posteriormente é filtrado. A solução é então concentrada por evaporação até que ocorram a cristalização do perclorato hidratado; os cristais formados são separados por centrifugação e secos em dessecador. Para o magnésio, isso leva tipicamente à formação do hexahidrato .[5]
A forma anidra pode ser preparada por aquecimento do perclorato hidratado em estufa a vácuo, a cerca de 250 °C, sob pressões entre 1 e 10 mmHg, o que remove a água de cristalização sem causar decomposição apreciável.[5]
Outra rota clássica para o perclorato anidro consiste na reação em estado sólido entre um carbonato alcalino-terroso e perclorato de amônio. Os reagentes são previamente moídos em moinho de bolas e aquecidos por volta de 250 °C, também sob vácuo. A transformação ocorre segundo:
Esse processo gera o perclorato metálico anidro com liberação simultânea de dióxido de carbono, água e amônia.[5]
Quando se deseja produzir o sal a partir de hidróxido, o perclorato de magnésio pode ser obtido por neutralização direta do ácido perclórico pelo hidróxido de magnésio:
Aplicações
A principal aplicação do perclorato de magnésio é como agente dessecante, especialmente na secagem de amostras gasosas. Apesar de sua elevada eficiência, seu uso como dessecante geral em laboratório não é recomendado atualmente, devido aos riscos inerentes aos percloratos, que podem reagir violentamente com compostos orgânicos e materiais combustíveis.[6][7]
Percloratos — incluindo o de magnésio — foram identificados em solos de Marte por missões espaciais. A presença desses sais é relevante para estudos sobre a química do planeta, pois soluções salinas contendo percloratos apresentam forte depressão do ponto de congelamento. Isso possibilita a existência de filmes de água líquida ou salmouras em condições ambientais marcianas que, de outra forma, seriam muito frias para permitir água no estado líquido.[8]
Ver também
Referências
- ↑ «Ficha de Informação de Produto Químico (FISPQ) - Perclorato de magnésio»
- ↑ Sizemore, H.G.; Mellon, M.T.; Rempel, A.W.; McKay, C.P.; Heldmann, J.L.; Stoker, C.R.; Perry, M.R. (fevereiro de 2026). «Liquid Vein networks as habitats in ice-cemented ground on Earth and Mars: Effects of soil geometry and salts». Icarus (em inglês). 116828 páginas. doi:10.1016/j.icarus.2025.116828. Consultado em 18 de novembro de 2025
- ↑ CRC Handbook Of Chemistry And Physics 97th Edition ( 2016) (em inglês) 97ª ed. ed. [S.l.]: Taylor and Francis Group. 2016. p. 4-72. Consultado em 18 de novembro de 2025
- ↑ a b Lee, J. D. (1999). Química Inorgânica Não Tão Concisa. São Paulo: Blucher. p. 171. ISBN 978-85-212-0176-2
- ↑ a b c Brauer, Georg (1963). Handbook of Preparative Inorganic Chemistry. New York: Academic Press. p. 320
- ↑ H. H. Willard, G. F. Smith (1922). «The Preparation and Properties of Magnesium Perchlorate and its Use as a Drying Agent». Journal of the American Chemical Society. 44 (10): 2255–2259. doi:10.1021/ja01431a022
- ↑ L. Wu, H. He (1994). «Preparation of perlite-based magnesium perchlorate desiccant with colour indicator». The Chemical Educator. 41 (5): 633–637. PMID 18965975. doi:10.1016/0039-9140(94)80041-3
- ↑ Hand, Eric (6 de agosto de 2008). «Perchlorate found on Mars». Nature (em inglês). ISSN 0028-0836. doi:10.1038/news.2008.1016 Parâmetro desconhecido
|article-number=ignorado (ajuda); Verifique o valor de|url-access=subscription(ajuda)
