Paration
Parathion
| |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||
| Nomes | |||||||||||||
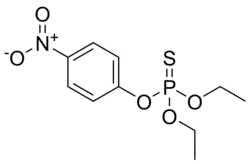
| Nome IUPAC | O,O-diethyl-O-4-nitro-phenylthiophosphate | ||||||||||||
| Outros nomes | E605 | ||||||||||||
| |||||||||||||
| |||||||||||||
| |||||||||||||
| |||||||||||||
| Página de dados suplementares | |||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||
Paration (português brasileiro) ou paratião (português europeu) é um pesticida agrícola, pertecente ao grupo dos organofosforados, sendo um potente inseticida e acaricida.[2] É um líquido marrom, que afunda em contato com a água.[3] Quando absorvido, sofre biotransformação, formando um metabólito ativo de nome paraoxon. Este é um inibidor da acetilcolinesterase, e causa os sintomas do envenenamento por organofosforados. O paratião é metabolizado a maloxão[1].
É uma das substâncias que mais causaram envenenamentos e mortes "acidentais" dentre os organofosforados.[4]
Síntese industrial
O paratião sintetiza-se a partir do ácido dietil ditiofosfórico (C
2H
5O)
2PS
2H por coloração para gerar cloreto de dietiltiofosorilo ((C
2H
5O)
2P(S)Cl), e depois o cloreto é tratado com 4-nitrofenolato de sódio (ou sal de sódio do 4-nitrofenol).[5]
- 2 (C
2H
5O)
2P(S)SH + 3 Cl
2 → 2 (C
2H
5O)
2P(S)Cl + S
2Cl
2 + 2 HCl - (C
2H
5O)
2P(S)Cl + NaOC
6H
4NO
2 → (C
2H
5O)
2P(S)OC
6H
4NO
2 + NaCl
Referências
- ↑ a b Considerações gerais sobre os Organofosforados…
- ↑ Química Nova. «INFLUÊNCIA DO MEIO REACIONAL NO COMPORTAMENTO FOTOQUÍMICO DO INSETICIDA PARATION ETÍLICO». Consultado em 21 de janeiro de 2010
- ↑ «Ficha de Informação de Produto Químico - Paration». Consultado em 20 de Fevereiro de 2008. Arquivado do original em 15 de Janeiro de 2006
- ↑ Goodman & Gilman. As bases farmacológicas da terapêutica. [tradução da 10. ed. original, Carla de Melo Vorsatz. et al] Rio de Janeiro: McGraw-Hill, 2005.
- ↑ Fee, D. C.; Gard, D. R.; Yang, C. (2005). «Phosphorus Compounds». Kirk-Othmer Encyclopedia of Chemical Technology. Nova York: John Wiley & Sons. ISBN 978-0471238966. doi:10.1002/0471238961.16081519060505.a01.pub2