PEGilação
_alternate.svg.png)
A PEGilação é o processo que consiste na união ou amalgamação covalente ou não covalente de cadeias de polímeros de polietilenoglicol (PEG, em farmácia chamado macrogol) a moléculas e macroestruturas, como fármacos, proteínas terapêuticas ou lipossomas, que então se diz que estão PEGiladas.[1][2][3][4] A PEGilação afeta as interações derivadas ou agregadas resultantes, que normalmente tornam mais lenta a coalescência e degradação destes produtos, bem como a sua eliminação do organismo in vivo.[5][6]
A PEGilação é conseguida rotineiramente por incubação de um derivado reativo do PEG com a molécula alvo. A união covalente do PEG a um fármaco ou proteína terapêutica pode "mascarar" o agente perante o sistema imunitário do hospedeiro (reduzindo a imunogenicidade e antigenicidade), e aumenta o seu tamanho hidrodinâmico (tamanho em solução), o que prolonga o seu tempo circulatório ao reduzir a sua eliminação renal. A PEGilação pode também proporcionar hidrossolubilidade a fármacos e proteínas que eram hidrófobos. A tecnologia da PEGilação, que demonstrou as suas vantagens farmacológicas e aceitabilidade, converteu-se na base de uma indústria em crescimento que movimenta milhares de milhões de dólares.[7]
Metodologia
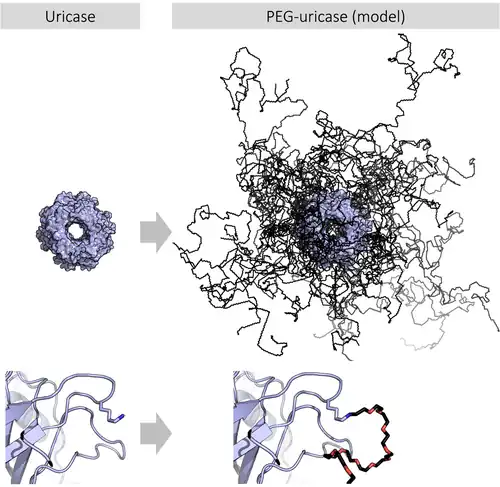
A PEGilação é o processo de unir as cadeias do polímero de PEG a moléculas, tipicamente péptidos, proteínas e fragmentos de anticorpos, o que pode melhorar a segurança e a eficiência de muitas terapias.[9][10] Produz alterações em propriedades físico-químicas como mudanças na conformação, união eletrostática, hidrofobia etc. Estes mudanças físicas e químicas aumentam a retenção sistémica do agente terapêutico. Além disso, podem influenciar a afinidade de união do resíduo terapêutico aos recetores da célula e podem alterar os padrões de absorção e distribuição.
Como a PEGilação aumenta o peso molecular de uma molécula, pode conferir várias vantagens farmacológicas significativas em relação à forma não modificada, como melhorar a solubilidade de um fármaco, reduzir a frequência das doses, o que pode reduzir a toxicidade sem diminuir a eficácia, ampliar a vida em circulação, aumentar a estabilidade do fármaco e aumentar a proteção contra a degradação proteolítica; as formas PEGiladas podem também ser patenteadas.[11]
Fármacos PEGilados
Em 1970, foi relatada a união de um polímero inerte e hidrófilo primariamente para aumentar a vida no sangue e o controlo da imunogenicidade de proteínas.[12] O polietilenoglicol foi o polímero escolhido.[13][14] Em 1981, Davis e Abuchowski fundaram a Enzon, Inc., que colocou no mercado três fármacos PEGilados. Abuchowski fundou posteriormente e foi o diretor executivo da Prolong Pharmaceuticals.[15]
O valor clínico da PEGilação está agora bem estabelecido. O ADAGEN (pegademase bovina) fabricado pela Enzon Pharmaceuticals, Inc., EUA foi a primeira proteína PEGilada aprovada pela FDA americana em março de 1990 a ser lançada no mercado. É usado para tratar uma forma grave de síndrome de imunodeficiência combinada grave (SCID), como alternativa ao transplante de medula óssea e à substituição de enzimas por terapia génica. Desde a introdução do ADAGEN, um grande número de proteínas e péptidos PEGilados foi introduzido como medicamentos, e muitos outros estão em ensaios clínicos ou em diversas fases de desenvolvimento. As vendas dos dois produtos mais bem-sucedidos, Pegasys e Neulasta, ultrapassaram os 5 mil milhões de dólares em 2011.[16][17] Todos os fármacos PEGilados comercialmente disponíveis contêm metoxipoli(etilenoglicol) ou mPEG. Os fármacos PEGilados no mercado (em ordem cronológica inversa do ano de aprovação pela FDA) são:[18]
- Um lípido PEGilado é usado como excipiente tanto na vacina da Moderna como na vacina da Pfizer-BioNTech contra a COVID-19. Ambas são vacinas de RNA que consistem num RNA mensageiro (mRNA), encapsulado numa bolha de moléculas lipídicas. É utilizada tecnologia de lípidos patenteada em cada uma. Em ambas as vacinas, as bolhas estão cobertas com uma molécula estabilizadora de polietilenoglicol. Houve uma pequena percentagem de casos de reações alérgicas ao PEG.[19][20][21] A molécula PEGilada da vacina da Moderna chama-se DMG-PEG 2000.
- Pegvaliase (Biomarin) – Fenilalanina amoníaco-liase recombinante PEGilada para o tratamento da fenilcetonúria, aprovada pela FDA nos EUA em maio de 2018.[22][23]
- Adynovate – Fator VIII anti-hemofílico PEGilado para o tratamento de pacientes com hemofilia A. (Baxalta, 2015)[24]
- Irinotecano lipossomal (Onivyde) – Irinotecano cloridrato tri-hidratado lipossomal PEGilado para o tratamento do cancro pancreático metastático em adultos que estão a ser tratados com gemcitabina. (Ipsen, 2015)
- Plegridy – Interferão Beta-1a PEGilado para o tratamento de pacientes com formas recorrentes de esclerose múltipla. (Biogen, 2014)
- Naloxegol (Movantik) – Naloxol PEGilado para o tratamento de obstipação induzida por opioides em pacientes adultos com dor crónica não cancerosa (a metadona não PEGilada pode causar reações intestinais adversas). (AstraZeneca, 2014)
- Peginesatide (Omontys) – Medicamento que se toma uma vez por mês para tratar a anemia associada à doença renal crónica em pacientes adultos submetidos a diálise (Affymax/Takeda Pharmaceuticals, 2012)
- Pegloticase (Krystexxa) – Uricase PEGilada para o tratamento da gota (Savient, 2010)
- Certolizumab pegol (Cimzia) – Anticorpo monoclonal para o tratamento de artrite reumatóide de moderada a grave e da doença de Crohn, um distúrbio inflamatório intestinal (Nektar/UCB Pharma, 2008)
- Metoxi polietilenoglicol-epoetina beta (Mircera) – Forma PEGilada da eritropoetina para combater a anemia associada à doença renal crónica (Roche, 2007)
- Pegaptanib (Macugen) – Usado para tratar a degeneração macular neovascular relacionada com a idade (Pfizer, 2004)
- Pegfilgrastim (Neulasta) – Fator estimulante de colónias de granulócitos humano metionil recombinante PEGilado para neutropenia grave induzida pela quimioterapia contra o cancro (Amgen, 2002)
- Pegvisomant (Somavert) – Uma muteína antagonista do recetor da PEG-hormona do crescimento humana para o tratamento da acromegalia (Pfizer, 2002)
- Peginterferon alfa-2a (Pegasys) – Interferão alfa PEGilado para uso no tratamento da Hepatite C crónica e hepatite B (Hoffmann-La Roche, 2002)
- Peginterferão alfa-2b (PegIntron) – Interferão alfa PEGilado para uso no tratamento da Hepatite C crónica e hepatite B (Schering-Plough/Enzon, 2000)
- Doxorrubicina HCl lipossomal (Doxil/Caelyx) – Lipossoma PEGilado contendo doxorrubicina para o tratamento do cancro (Alza, 1995)
- Pegaspargase (Oncaspar) – L-asparaginase PEGilada para o tratamento da Leucemia linfoblástica aguda em pacientes que são hipersensíveis à forma não modificada nativa da L-asparaginase (Enzon, 1994). Este fármaco foi recentemente aprovado para uso em casos especiais.
- Pegademase bovina (Adagen) – PEG-adenosina desaminase para o tratamento da Imunodeficiência combinada grave (SCID) (Enzon, 1990)
Litígios de Patentes
O sistema de entrega de fármacos em nanopartículas (LNP) lipídicas PEGiladas das vacinas de mRNA conhecidas como mRNA-1273 foi objeto de um litígio de patentes atual com a Arbutus Biopharma, da qual a Moderna obteve anteriormente licença da tecnologia LNP.[25][26] Em 4 de setembro de 2020, a Nature Biotechnology noticiou que a Moderna perdeu uma parte crucial no caso judicial em curso sobre propriedade intelectual.[27]
Uso em Investigação
A PEGilação tem usos práticos em biotecnologia para a entrega de proteínas,[28] transfeção de células, e edição do genoma em células não humanas.[29]
Procedimento
O primeiro passo da PEGilação é a adequada funcionalização do polímero de PEG numa ou em ambas as extremidades. Os PEGs que são ativados em cada extremidade com o mesmo resíduo reativo denominam-se "homobifuncionais", enquanto se os grupos funcionais presentes forem diferentes, o derivado de PEG é denominado "heterobifuncional" ou "heterofuncional". Os derivados quimicamente ativos ou ativados do polímero de PEG são preparados para que o PEG se ligue à molécula desejada.[30]
O processo global de PEGilação usado até agora para a conjugação de proteínas pode ser classificado em dois grandes tipos: um processo em lotes de fase em solução e um processo em lotes alimentado em coluna.[31] O processo em lotes que geralmente se adota envolve a mistura dos reagentes juntamente com uma solução tampão apropriada, preferencialmente a uma temperatura entre 4 e 6 °C, seguida da separação e purificação do produto desejado usando uma técnica apropriada baseada nas suas propriedades físico-químicas, como a cromatografia de exclusão por tamanho (SEC), cromatografia de troca iónica (IEX), cromatografia de interações hidrofóbicas (HIC) e sistemas de duas fases aquosos ou de membrana (ATPS).[32][33]
A escolha do grupo funcional apropriado para o derivado de PEG baseia-se no tipo de grupo reativo disponível na molécula que será acoplada ao PEG. Para as proteínas, os aminoácidos reativos típicos são os seguintes: lisina, cisteína, histidina, arginina, ácido aspártico, ácido glutâmico, serina, treonina e tirosina. O grupo amino N-terminal e o carboxilo C-terminal podem também ser usados como sítios específicos de sítio por conjugação com polímeros funcionais aldeído.[34]
As técnicas usadas para formar derivados do PEG de primeira geração geralmente envolvem a reação do polímero de PEG com um grupo que é reativo com os grupos hidroxilo, tipicamente anidridos, cloretos de acilo, cloroformatos e carbonatos. Na química de PEGilação de segunda geração, estão disponíveis para a conjugação grupos funcionais mais eficientes, como aldeídos, ésteres, amidas, etc.
As aplicações da PEGilação tornaram-se cada vez mais avançadas e sofisticadas, e aumentou a necessidade de PEGs heterobifuncionais para a conjugação. Estes PEGs heterobifuncionais são muito úteis para ligar duas entidades, onde se necessita de um espaçador hidrófilo, flexível e biocompatível. Os grupos terminais preferidos para os PEGs heterobifuncionais são a maleimida, vinil sulfonas, piridil dissulfureto, aminas, ácidos carboxílicos e ésteres de NHS.[35][36][37]
Os agentes de PEGilação de terceira geração, nos quais o polímero foi ramificado, estão disponíveis nas formas de Y ou de pente e apresentam uma viscosidade reduzida e não causam acumulação em órgãos.[38] Recentemente, também foram desenvolvidas estratégias enzimáticas para a PEGilação, ampliando assim as ferramentas de conjugação.[39][40] Os conjugados PEG-proteína obtidos por métodos enzimáticos já estão em uso clínico, por exemplo: Lipegfilgrastim, Rebinyn ou Esperoct.
Limitações
A imprevisibilidade nos tempos de eliminação do organismo dos compostos PEGilados pode causar a acumulação de compostos de elevado peso molecular no fígado originando corpos de inclusão com consequências toxicológicas desconhecidas.[41] Além disso, a alteração no comprimento da cadeia pode causar tempos de eliminação inesperados in vivo.[42] Adicionalmente, as condições experimentais da reação de PEGilação (isto é, pH, temperatura, tempo de reação, custo global do processo e razão molar entre o derivado do PEG e o péptido) também têm um impacto na estabilidade dos produtos finais PEGilados.[43]
Para superar as limitações mencionadas, vários investigadores ofereceram diversas estratégias, como mudanças de tamanho (Mw), de número, de localização e do tipo de ligação da molécula de PEG.[44][45] A conjugação de polissacarídeos biodegradáveis, que é uma alternativa promissora à PEGilação, é outra forma de resolver a questão da biodegradação do PEG.[46]
Referências
- ↑ Jokerst, Jesse V; Lobovkina, Tatsiana; Zare, Richard N; Gambhir, Sanjiv S (junho de 2011). «Nanoparticle PEGylation for imaging and therapy». Nanomedicine. 6 (4): 715–728. PMC 3217316
 . PMID 21718180. doi:10.2217/nnm.11.19
. PMID 21718180. doi:10.2217/nnm.11.19
- ↑ Knop, Katrin; Hoogenboom, Richard; Fischer, Dagmar; Schubert, Ulrich S. (23 de agosto de 2010). «Poly(ethylene glycol) in Drug Delivery: Pros and Cons as Well as Potential Alternatives». Angewandte Chemie International Edition. 49 (36): 6288–6308. PMID 20648499. doi:10.1002/anie.200902672
- ↑ Veronese, Francesco M; Mero, Anna (2008). «The Impact of PEGylation on Biological Therapies». BioDrugs. 22 (5): 315–329. PMID 18778113. doi:10.2165/00063030-200822050-00004
- ↑ Veronese, Francesco M.; Pasut, Gianfranco (novembro de 2005). «PEGylation, successful approach to drug delivery». Drug Discovery Today. 10 (21): 1451–1458. PMID 16243265. doi:10.1016/S1359-6446(05)03575-0
- ↑ Blume G, Cevc, G (13 de abril de 1990). «Liposomes for the sustained drug release in vivo». Biochimica et Biophysica Acta (BBA) - Biomembranes. 1029 (1): 91–97. PMID 2223816. doi:10.1016/0005-2736(90)90440-y
- ↑ Klibanov AL, Maruyama K, Torchilin VP, Huang L (30 de xullo de 1990). «Amphipathic polyethyleneglycols effectively prolong the circulation time of liposomes». FEBS Lett. 268 (1): 235–237. PMID 2384160. doi:10.1016/0014-5793(90)81016-h Verifique data em:
|data=(ajuda) - ↑ Damodaran V. B. ; Fee C. J. (2010). «Protein PEGylation: An overview of chemistry and process considerations». European Pharmaceutical Review. 15 (1): 18–26
- ↑ Sherman, MR; Saifer, MG; Perez-Ruiz, F (3 de janeiro de 2008). «PEG-uricase in the management of treatment-resistant gout and hyperuricemia.». Advanced Drug Delivery Reviews. 60 (1): 59–68. PMID 17826865. doi:10.1016/j.addr.2007.06.011
- ↑ Veronese, FM; Harris, JM (junho de 2002). «Introduction and overview of peptide and protein pegylation». Advanced Drug Delivery Reviews. 54 (4): 453–456. PMID 12052707. doi:10.1016/s0169-409x(02)00020-0
- ↑ Porfiryeva, N. N.; Moustafine, R. I.; Khutoryanskiy, V. V. (xaneiro de 2020). «PEGylated Systems in Pharmaceutics» (PDF). Polymer Science, Series C. 62 (1): 62–74. doi:10.1134/S181123822001004X Verifique data em:
|data=(ajuda) - ↑ Milla, P; Dosio, F (13 de janeiro de 2012). «PEGylation of proteins and liposomes: a powerful and flexible strategy to improve the drug delivery.». Current Drug Metabolism. 13 (1): 105–119. PMID 21892917. doi:10.2174/138920012798356934. hdl:2318/86788
- ↑ Davis, Frank F. (junho de 2002). «The origin of pegnology». Advanced Drug Delivery Reviews. 54 (4): 457–458. PMID 12052708. doi:10.1016/s0169-409x(02)00021-2
- ↑ Abuchowski, A; Van Es, T; Palczuk, N. C.; Davis, F. F. (1977). «Alteration of immunological properties of bovine serum albumin by covalent attachment of polyethylene glycol». The Journal of Biological Chemistry. 252 (11): 3578–81. PMID 405385. doi:10.1016/S0021-9258(17)40291-2
- ↑ Abuchowski, A; McCoy, J. R.; Palczuk, N. C.; Van Es, T; Davis, F. F. (1977). «Effect of covalent attachment of polyethylene glycol on immunogenicity and circulating life of bovine liver catalase». The Journal of Biological Chemistry. 252 (11): 3582–6. PMID 16907. doi:10.1016/S0021-9258(17)40292-4
- ↑ «Dr. Abraham Abuchowski, Ph.D. – Home». prolongpharma.com. Consultado em 15 de janeiro de 2020. Cópia arquivada em 15 de janeiro de 2020 Parâmetro desconhecido
|url-morta=ignorado (ajuda) - ↑ Klauser, Alexander (Head), Roche Group Media Relations, "Roche in 2011: Strong results and positive outlook," www.roche.com/med-cor-2012-02-01-e.pdf, Feb 1, 2012, p.7
- ↑ "Amgen 2011 Annual Report and Financial Summary," [1] 2011 AnnualReport.pdf, Feb 23 2012, p. 71
- ↑ Zalipsky, Samuel; Pasut, Gianfranco (2020). «Evolution of polymer conjugation to proteins». Polymer-Protein Conjugates. [S.l.: s.n.] pp. 3–22. ISBN 9780444640819. doi:10.1016/b978-0-444-64081-9.00001-2
- ↑ Cabanillas, Beatriz; Akdis, Cezmi; Novak, Natalija (2020). «Allergic reactions to the first COVID‐19 vaccine: A potential role of Polyethylene glycol?». Allergy. 76 (6): 1617–1618. PMID 33320974. doi:10.1111/all.14711
- ↑ Weiland, Noah; LaFraniere, Sharon; Baker, Mike; Thomas, Katie (17 de dezembro de 2020). «2 Alaska Health Workers Got Emergency Treatment After Receiving Pfizer's Vaccine». New York Times
- ↑ Firger, Jessica; Caldwell, Travis (19 de dezembro de 2020). «Third Alaskan health care worker has allergic reaction to Covid-19 vaccine». Cable News Network
- ↑ Powers, Marie (29 de maio de 2018). «Biomarin aces final exam: Palynziq gains FDA approval to treat PKU in adults». BioWorld (em inglês)
- ↑ Levy, Harvey L.; Sarkissian, Christineh N.; Stevens, Raymond C.; Scriver, Charles R. (junho de 2018). «Phenylalanine ammonia lyase (PAL): From discovery to enzyme substitution therapy for phenylketonuria». Molecular Genetics and Metabolism. 124 (4): 223–229. PMID 29941359. doi:10.1016/j.ymgme.2018.06.002
- ↑ «FDA approves modified antihemophilic factor for hemophilia A». www.fda.gov. Cópia arquivada em 16 de novembro de 2015
- ↑ Auth, Dorothy R.; Powell, Michael B. (14 de setembro de 2020). «Patent Issues Highlight Risks of Moderna's COVID-19 Vaccine». New York Law Journal. Consultado em 1 de dezembro de 2020
- ↑ Vardi, Nathan (29 de junho de 2020). «Moderna's Mysterious Coronavirus Vaccine Delivery System». Forbes. Consultado em 1 de dezembro de 2020
- ↑ «Moderna loses key patent challenge». Nature Biotechnology. 38 (9). 1009 páginas. Setembro de 2020. PMID 32887970. doi:10.1038/s41587-020-0674-1
- ↑ Pasut, Gianfranco; Zalipsky, Samuel (2020). Polymer-Protein Conjugates: From Pegylation and Beyond. [S.l.]: Elsevier. ISBN 978-0-444-64082-6. OCLC 1127111107
- ↑ Balazs, Daniel A.; Godbey, WT (15 de dezembro de 2011). «Liposomes for Use in Gene Delivery». Journal of Drug Delivery. 2011: 326497. PMC 3066571
 . PMID 21490748. doi:10.1155/2011/326497
. PMID 21490748. doi:10.1155/2011/326497
- ↑ Pasut, Gianfranco; Veronese, Francesco M. (julho de 2012). «State of the art in PEGylation: The great versatility achieved after forty years of research». Journal of Controlled Release. 161 (2): 461–472. PMID 22094104. doi:10.1016/j.jconrel.2011.10.037
- ↑ Fee, Conan J.; Van Alstine, James M. (2006). «PEG-proteins: Reaction engineering and separation issues». Chemical Engineering Science. 61 (3): 924. doi:10.1016/j.ces.2005.04.040
- ↑ Veronese, Francesco M., ed. (2009). «Protein conjugates purification and characterization». PEGylated protein drugs basic science and clinical applications Online-Ausg. ed. Basel: Birkhäuser. pp. 113–125. ISBN 978-3-7643-8679-5
- ↑ Fee, Conan J. (2003). «Size-exclusion reaction chromatography (SERC): A new technique for protein PEGylation». Biotechnology and Bioengineering. 82 (2): 200–6. PMID 12584761. doi:10.1002/bit.10561. hdl:10092/351
- ↑ Fee, Conan J.; Damodaran, Vinod B. (2012). «Production of PEGylated Proteins». Biopharmaceutical Production Technology. [S.l.: s.n.] 199 páginas. ISBN 9783527653096. doi:10.1002/9783527653096.ch7
- ↑ «Polypeptide therapeutics and uses thereof». Wipo (PCT). WO (138413A1). 2016
- ↑ «Methods and pharmaceutical compositions for treating candida auris in blood». Wipo (PCT). WO (126695A2). 2019
- ↑ «Arginase formulations and methods». Wipo (PCT). WO (8495A2). 2011
- ↑ Ryan, Sinéad M; Mantovani, Giuseppe; Wang, Xuexuan; Haddleton, David M; Brayden, David J (2008). «Advances in PEGylation of important biotech molecules: Delivery aspects». Expert Opinion on Drug Delivery. 5 (4): 371–83. PMID 18426380. doi:10.1517/17425247.5.4.371
- ↑ Maso, Katia; Grigoletto, Antonella; Gianfranco (2018). «Transglutaminase and Sialyltransferase Enzymatic Approaches for Polymer Conjugation to Proteins». Therapeutic Proteins and Peptides. Col: Advances in Protein Chemistry and Structural Biology. 112. [S.l.: s.n.] pp. 123–142. ISBN 9780128143407. PMID 29680235. doi:10.1016/bs.apcsb.2018.01.003
- ↑ da Silva Freitas, Débora; Mero, Anna; Pasut, Gianfranco (20 de março de 2013). «Chemical and Enzymatic Site Specific PEGylation of hGH». Bioconjugate Chemistry. 24 (3): 456–463. PMID 23432141. doi:10.1021/bc300594y. hdl:11577/2574695
- ↑ Kawai, F. (1 de janeiro de 2002). «Microbial degradation of polyethers». Applied Microbiology and Biotechnology. 58 (1): 30–38. PMID 11831473. doi:10.1007/s00253-001-0850-2
- ↑ Veronese, Francesco M (março de 2001). «Peptide and protein PEGylation». Biomaterials. 22 (5): 405–417. PMID 11214751. doi:10.1016/s0142-9612(00)00193-9
- ↑ González-Valdez, José; Rito-Palomares, Marco; Benavides, Jorge (junho de 2012). «Advances and trends in the design, analysis, and characterization of polymer–protein conjugates for 'PEGylaided' bioprocesses». Analytical and Bioanalytical Chemistry. 403 (8): 2225–2235. PMID 22367287. doi:10.1007/s00216-012-5845-6
- ↑ Zhang, Genghui; Han, Baozhong; Lin, Xiaoyan; Wu, Xin; Yan, Husheng (dezembro de 2008). «Modification of Antimicrobial Peptide with Low Molar Mass Poly(ethylene glycol)». The Journal of Biochemistry. 144 (6): 781–788. PMID 18845567. doi:10.1093/jb/mvn134
- ↑ Obuobi, Sybil; Wang, Ying; Khara, Jasmeet Singh; Riegger, Andreas; Kuan, Seah Ling; Ee, Pui Lai Rachel (outubro de 2018). «Antimicrobial and Anti-Biofilm Activities of Surface Engineered Polycationic Albumin Nanoparticles with Reduced Hemolytic Activity». Macromolecular Bioscience. 18 (10). 1800196 páginas. PMID 30066983. doi:10.1002/mabi.201800196
- ↑ Zhou, Yang; Petrova, Stella P.; Edgar, Kevin J. (15 de novembro de 2021). «Chemical synthesis of polysaccharide–protein and polysaccharide–peptide conjugates: A review». Carbohydrate Polymers (em inglês). 274. 118662 páginas. ISSN 0144-8617. PMID 34702481. doi:10.1016/j.carbpol.2021.118662