Oxamida
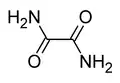
Oxamide
| |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||
| Nomes | |||||||||||||||
| Nome IUPAC | Ethanediamide | ||||||||||||||
| Outros nomes | Oxamide Oxalamide Oxamimidic acid Diaminoglyoxal Oxalic acid diamide 1-Carbamoyl-formimidic acid | ||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| Página de dados suplementares | |||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||
Oxamida é a diamida do ácido oxálico, um composto orgânico. É um sólido branco e cristalino, solúvel em etanol, ligeiramente solúvel em água e insolúvel em éter dietílico. É a diamida derivada do ácido oxálico.
Produção e aplicações
Oxamidas são produzidos de Cianeto de hidrogênio, oxidado do cianogênio e depois hidrolisado.[1]
A maior aplicação é como substituto da ureia em fertilizantes, sendo muitas vezes preferido por liberar a amônia mais lentamente, o que é preferível em alguns processos agrícolas. Também utilizado como estabilizante em preparações de nitrocelulose.
Reações
Acima de 350°C se decompõe em cianogênio e água [2]
Referências
- ↑ Wilhelm Riemenschneider, Minoru Tanifuji "Oxalic Acid" in Ullmann's Encyclopedia of Industrial Chemistry, 2002, Wiley-VCH, Weinheim. doi:10.1002/14356007.a18_247 10.1002/14356007.a18_247.
- ↑ Nguyen T.L., Fowler F.W., Lauher J.W., "Commensurate and incommensurate hydrogen bonds. An exercise in crystal engineering." Journal of the American Chemical Society, 123(44), pp. 11057-64, 2001. doi:10.1021/ja016635v