Nitrato de cádmio
Nitrato de cádmio
| |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||
| Nomes | |||||||||||||
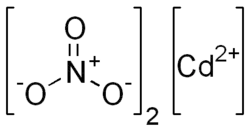
| Nome IUPAC | Nitrato de cádmio | ||||||||||||
| |||||||||||||
| |||||||||||||
| |||||||||||||
| |||||||||||||
| Página de dados suplementares | |||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||
Nitrato de cádmio ou nitrato de cádmio tetrahidratado, é um composto químico de fórmula molecular Cd(NO3)2. 4(H2O).
Características
É um sal inorgânico, sólido inodoro não radioativo, de coloração branca. Não é inflamável, mas pode causar fogo se em contato com certos materiais: como madeira, materiais combustíveis,etc. Quando exposto ao fogo aumentará a intensidade e pode formar óxidos tóxicos de nitrogênio e cádmio.
Síntese
nitrato de cádmio pode ser preparado dissolvendo cádmio metálico, ou seu óxido,hidróxido ou carbonato em ácido nítrico,o nitrato de cádmio é então cristalizado evaporando a a água da solução.
- CdO + 2HNO3 → Cd(NO3)2 + H2O
- CdCO3 + 2 HNO3 → Cd(NO3)2 + CO2 + H2O
- Cd + 4 HNO3 → 2 NO2 + 2 H2O + Cd(NO3)2
reações
À elevadas temperaturas nitrato de cádmio se dissocia em óxido de cádmio, e em óxidos de nitrogênio.Quando sulfeto de hidrogênio é borbulhado em uma solução ácida de nitrato de cádmio,sulfeto de cádmio é formado
Usos
É usado como tintura para vidros e porcelana, como reagente de laboratório, e outros.
Propriedades Físico-Químicas
- Peso molecular 308,47
- Ponto de ebulição (°C)?
- Ponto de fusão (°C) 59,4
- Temperatura crítica (°C)?
- Pressão crítica (atm)?
- Densidade relativa do líquido (ou sólido) 2,45 A 20 °C (SÓLIDO)
