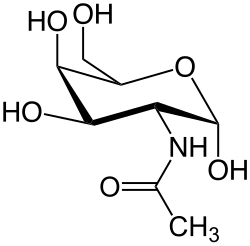
N-Acetilgalactosamina
N-Acetylgalactosamine
| |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||
| Nomes | |||||||||||
| Nome IUPAC | 2-(Acetylamino)-2-deoxy-D-galactose | ||||||||||
| Outros nomes | GalNAc; 2-Acetamido-2-deoxy-D-galactose; N-Acetylchondrosamine; 2-Acetamido-2-deoxy-D-galactopyranose; N-Acetyl-D-galactosamine | ||||||||||
| |||||||||||
| |||||||||||
| |||||||||||
| |||||||||||
| Página de dados suplementares | |||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||
A N-acetilgalactosamina é um aminoaçúcar derivado da galactose, caracterizado pela presença de um grupo acetil ligado ao nitrogênio do carbono 2. Essa modificação química confere à molécula propriedades únicas que a tornam fundamental na composição de glicoproteínas e glicoconjugados, desempenhando papéis cruciais em processos biológicos como reconhecimento celular, sinalização e proteção das superfícies epiteliais. Amplamente distribuída em organismos animais, a N-acetilgalactosamina é essencial para a manutenção da integridade e comunicação celular.[2]
Estrutura
A estrutura química da N-acetilgalactosamina consiste em uma hexosamina, um açúcar de seis carbonos que deriva da galactose pela substituição do grupo hidroxila no carbono 2 por um grupo amino acetilado. Essa modificação altera a polaridade e a reatividade da molécula, conferindo-lhe maior estabilidade química e capacidade de interagir especificamente com proteínas e outras biomoléculas. Em solução aquosa, a molécula pode existir em formas cíclicas e lineares, sendo a forma de anel furanose a predominante, na qual quatro carbonos e um oxigênio formam um ciclo estável.[3]
O grupo acetil ligado ao nitrogênio do carbono 2 distingue a N-acetilgalactosamina de outros aminoaçúcares, como a N-acetilglucosamina, e é fundamental para sua incorporação em glicoconjugados. A conformação espacial da molécula, definida pela posição dos grupos hidroxila e do grupo acetil, influencia sua afinidade por receptores celulares e enzimas, determinando sua função biológica e interações moleculares.[4]
A N-acetilgalactosamina está presente em glicoproteínas, principalmente nas mucinas, onde atua como componente estrutural que contribui para a formação de barreiras protetoras em superfícies mucosas. Essas glicoproteínas revestem órgãos e tecidos, desempenhando funções como lubrificação, proteção contra patógenos e modulação da resposta imune, além de facilitarem o reconhecimento celular e a mediação das interações entre células e a matriz extracelular.[5]
Funções
Além de sua função estrutural, a N-acetilgalactosamina participa de processos de sinalização celular, servindo como molécula de reconhecimento para receptores específicos na superfície celular. Esses receptores mediam eventos como endocitose, adesão celular e respostas imunológicas, sendo a base para estratégias biomédicas de entrega seletiva de fármacos, especialmente direcionados a células do fígado, como os hepatócitos.[6]
A N-acetilgalactosamina também desempenha papel importante em processos patológicos e imunológicos, pois sua presença em glicoconjugados pode influenciar a interação entre células normais e células do sistema imune, além de ser reconhecida por certos patógenos para aderência e invasão. Essa característica tem sido explorada em estudos para o desenvolvimento de vacinas e terapias contra infecções, bem como em pesquisas sobre doenças inflamatórias e câncer, onde alterações na expressão e na estrutura da N-acetilgalactosamina em glicoproteínas podem afetar a progressão e o prognóstico da doença.[7]
Referências
- ↑ a b Datenblatt N-Acetilgalactosamina bei Acros, abgerufen am 26. Februar 2010..
- ↑ Jones, A.; et al. Carbohydrate Chemistry in Biology. Oxford University Press, 2010.
- ↑ Smith, B. Structural Biochemistry of Amino Sugars. Springer, 2012.
- ↑ Brown, C. Glycoconjugates and Cellular Recognition. Elsevier, 2015.
- ↑ Taylor, D.; Wilson, E. Mucins and Their Role in Health. Academic Press, 2018.
- ↑ Wilson, F. Targeted Drug Delivery Systems. Wiley, 2020.
- ↑ Garcia, M.; et al. Immunological Roles of Glycans. Nature Reviews Immunology, 2021.