Miristil éter sulfato de sódio
Miristil éter sulfato de sódio
| |||||||
|---|---|---|---|---|---|---|---|
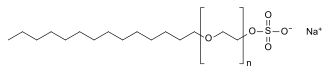 | |||||||
| Nomes | |||||||
| Outros nomes | sal de sódio de miristil éter sulfato PEG-(1-4); miristil éter sulfato POE(2); miristil éter sulfato de sódio dietileno glicol; mireth éter sulfato de sódio | ||||||
| |||||||
| |||||||
| |||||||
| Página de dados suplementares | |||||||
| Estrutura e propriedades | n, εr, etc. | ||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||
Miristil éter sulfato de sódio é uma mistura de compostos orgânicos com propriedades tanto detergentes como surfactantes. É encontrado em muitos produtos de higiene pessoal tal como sabões, xampus, cremes dentais. É um agente formador de espuma barato e efetivo. Típico de muitos detergentes, miristil éter sulfato de sódio consiste de diversos compostos intimamente relacionados. Algumas vezes o número de unidades de éter de etilenoglicol é especificado no nome como miriltil éter-n ou myreth-n sulfato, por exemplo miristil éter-2 sulfato.
Produção
Miristil éter sulfato de sódio é muito similar ao Lauriléter sulfato de sódio; a única diferença é doisa átomos de carbono a mais na porção álcool graxo da "cauda" hidrofóbica. É fabricado por etoxilação com álcool miristílico. Subsequentemente, o grupo terminal OH é convertido ao sulfato por tratamento com ácido clorossulfúrico.[1]
Referências
- ↑ Eduard Smulders, Wolfgang von Rybinski, Eric Sung, Wilfried Rähse, Josef Steber, Frederike Wiebel, Anette Nordskog “Laundry Detergents” in Ullmann's Encyclopedia of Industrial Chemistry 2007, Wiley-VCH, Weinheim. doi:10.1002/14356007.a08_315.pub2 10.1002/14356007.a08_315.pub2.