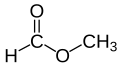
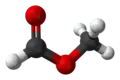
Metanoato de metila
Metanoato de metilo
| |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||
| Nomes | |||||||||||||||||
| Nome IUPAC | Formiato de metila | ||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| Página de dados suplementares | |||||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||||
Metanoato de metilo é o éster produzido pela reação do ácido metanoico com o metanol.
Produção
Em laboratório, o metanoato de metilo pode ser produzido pela reação de condensação do metanol e o ácido fórmico como a seguir:
Na indústria, no entanto, é normalmente obtido pela combinação do metanol e o monóxido de carbono (carbonilação) na presença de um base forte como o metóxido de sódio:[2]
Este processo, praticado por empresas como a BASF produz 96% de seletividade em relação ao metanoato de metilo, embora possa sofrer de sensitividade catalítica à água eventualmente presente no monóxido de carbono, comummente obtido por gás de síntese. Monóxido de carbono muito seco é, portanto, um requerimento essencial para esta processo.[3]