Latrunculina
As latrunculinas são uma família de produtos naturais e toxinas produzidas por certas esponjas, dos géneros Latrunculia e Negombata, do primeiro dos quais deriva o seu nome. Liga-se a monómeros de actina perto da fenda de ligação a nucleótidos com uma estequiometria de 1:1 e impede que a actina se polimerize. Administrada in vivo em experiências, este efeito resulta na distorção dos filamentos de actina do citoesqueleto, e permite a visualização das alterações correspondentes nos processos celulares. Esta propriedade é semelhante à da citocalasina, mas possui um intervalo de concentração eficaz mais estreito.[1] A latrunculina foi muito útil para a descoberta da regulação da distribuição da caderina e possui possíveis aplicações médicas.[2] A latrunculina A, um tipo de toxina, torna reversíveis alterações morfológicas nas células de mamíferos ao alterar a rede de actina.[3]
Latrunculina A:
| Fórmula molecular: | C22H31NO5S[4] |
|---|---|
| Peso molecular: | 421,552 g/mol[4] |
Alvos e funções
A gelsolina - latrunculina A causa o bloqueio das extremidades dos filamentos de actina, uma vez que se liga às extremidades "farpadas" (+), o que acelera a nucleação. Esta proteína regulada pelo cálcio também desempenha um papel na montagem e desmontagem dos cílios.[4]
Latrunculina B:
| Fórmula molecular: | C20H29NO5S[4] |
| Peso molecular: | 395,514 g/mol |
Alvos e funções
A actina - latrunculina B arma a estrutura das fibras de actina.
A proteína espira homóloga 2 é necessária para a divisão celular, transporte de vesículas no filamento de actina e é essencial para a formação do estrangulamento da célula durante a divisão celular[4].
História
A latrunculina é uma toxina produzida por esponjas. A esponja vermelha Latrunculia magnifica é uma esponxa abundante nos golfos de Aqaba e de Suez[5] no mar Vermelho, onde vive a profundidades de 6–30 metros.[6] A toxina foi descoberta por volta de 1970. Observou-se que as esponjas vermelhas Latrunculia magnifica nunca sofriam danos nem eram comidas pelos peixes, enquanto outras esponjas eram. Além disso, quando se esmagavam estas esponjas no mar, libertavam um líquido avermelhado. Os peixes que se encontravam perto fugiam imediatamente da zona onde se vertia o líquido. Estas foram as primeiras indicações de que estas esponjas produziam uma toxina. Posteriormente, esta hipótese confirmou-se ao esmagar a esponja num aquário com peixes, tendo estes mostrado uma perda de equilíbrio e hemorragias graves, morrendo em apenas 4–6 minutos.[6] Observaram-se efeitos semelhantes quando injetada em ratos. A latrunculina constitui 0,35 % do peso seco da esponja.[5] Existem duas formas principais da toxina, chamadas A e B. A latrunculina A está presente apenas nas esponjas do golfo de Suez, enquanto a latrunculina B é própria das esponjas do golfo de Aqaba.[5]
Estrutura
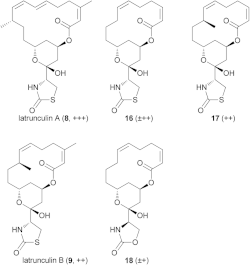
Existem vários isómeros da latrunculina: A, B, C, D, G, H, M, S e T. As estruturas mais comuns e importantes são as das latrunclinas A e B. As suas fórmulas são, respetivamente, C22H31NO5S e C20H29NO5S. O anel de macrolactona da parte superior que contém ligações duplas é uma característica estrutural das moléculas de latrunculina. A cadeia lateral contém uma aciltiazolidinona. Além destas formas que aparecem na natureza, os cientistas produziram formas sintéticas com diferentes intensidades de toxicidade. Na figura mostram-se algumas destas formas e a sua capacidade relativa de alterar a atividade dos microfilamentos. As formas semissintéticas que continham derivados N-alquilados eram inativas.[7]
Mecanismo de ação
As latrunculinas A e B afetam a polimerização da actina. A latrunculina liga-se aos monómeros de actina perto da fenda para a ligação a nucleótidos com uma estequiometria de 1:1 e impede a polimerização da actina.[1] Deste modo, os nucleótidos não podem dissociar-se da fenda para a ligação aos nucleótidos.[8] A evidência experimental mostra que a latrunculina A é biologicamente ativa no solvente DMSO, mas não em soluções aquosas, como demonstrado em culturas celulares e no tecido cerebral,[9] provavelmente devido à permeação celular.
Quando a formação de filamentos de actina é alterada devido à latrunculina, as toxinas Shiga da bactéria Escherichia coli têm maior probabilidade de se infiltrarem na monocamada do epitélio intestinal, o que pode aumentar o risco de doenças do trato gastrointestinal.[10]
Parece que os monómeros de actina têm maior afinidade para se ligarem à latrunculina A do que à latrunculina B.[11] Por outras palavras, a latrunculina A é uma toxina mais potente. A latrunculina B é inativada mais rapidamente do que a A.[12]
A prevenção da polimerização dos filamentos de actina causa alterações reversíveis na morfologia das células de mamíferos.[13] A latrunculina interfere com a estrutura do citoesqueleto em ratos.[14]
Após a exposição de fibroblastos L929 de rato à latrunculina B, estas células crescem mais, e as células renais PtK2 de Potorous (um marsupial) expostas produziam extensões ramificadas longas.[15] Estas extensões parecem ser acumulações de monómeros de actina.
Metabolismo
As células de leveduras na ausência das proteínas osh3 ou osh5 mostram hipersensibilidade à latrunculina B.[16] As proteínas osh são homólogas das enzimas geradas pelo gene OSBP dos mamíferos, o que indica que estas devem desempenhar uma função na toxicocinética das latrunculinas. As leveduras mutantes que são resistentes à latrunculina mostram uma mutação, D157E, que afeta a formação de uma ponte de hidrogénio com a latrunculina.[8] Outros mutantes de leveduras modificam o sítio de ligação, o que as torna resistentes à latrunculina.
Não foram realizadas investigações para compreender como funciona a biotransformação da latrunculina em células eucarióticas. No entanto, os investigadores sugerem que é a forma inalterada da latrunculina que causa efeitos tóxicos.[3]
Toxicidade
Como a latrunculina inibe a polimerização da actina e a capacidade contrátil da actomiosina, a exposição à latrunculina pode causar relaxamento celular, expansão dos tecidos de drenagem e diminuição da resistência ao fluxo de saída, por exemplo na rede trabecular.
Plantas
A latrunculina B causa marcadas reduções dependentes da dose na frequência de germinação do pólen e na velocidade de crescimento do tubo polínico.[17] Adicionar latrunculina B a soluções de actina F do pólen resulta na diminuição rápida na quantidade total de polímero, com um aumento da extensão da despolimerização com a concentração da toxina. A concentração da latrunculina B necessária para a inibição a metade do máximo da germinação do pólen é de 40 a 50 nM. Em contraste, a extensão do tubo polínico é muito mais sensível, necessitando apenas de 5 a 7 nM de LATB para a inibição a metade do máximo. A distorção da germinação e do crescimento do tubo polínico pela latrunculina B é parcialmente reversível a baixa concentração (<30 nM).[17]
Animais
Ao espremer a esponja Latrunculia magnifica num aquário com peixes, estes quase imediatamente experimentam agitação, seguida de hemorragia, perda de equilíbrio e morte em 4–6 minutos.[18] A latrunculina A foi utilizada como inibidor da reação acrossómica em experiências de laboratório com cobaias.[19]
Humanos
A latrunculina A induz a redução da contractilidade da actomiosina. Isto está associado à expansão porosa da rede trabecular sem evidências de que se reduza a expressão das proteínas da matriz extracelular estruturais ou a viabilidade celular.[20] A doses elevadas, a latrunculina pode induzir danos celulares agudos e morte celular programada ao ativar-se a via da caspase-3/7.[18]
Doses letais
Toxicidade
A toxicidade de uma substância é medida através de indicadores específicos que determinam a dosagem necessária para causar efeitos adversos ou o óbito em espécimes de teste.
- TDLo (Menor dose tóxica publicada): Indica a menor dosagem documentada que introduziu efeitos tóxicos em humanos ou animais.
- LD₅₀ (Dose letal média): Indica a dose necessária para matar 50% da população testada.
| Indicador | Espécie | Dose / Exposição |
|---|---|---|
| TDLo (Oral) | Humanos | 1,14 ml/kg (650 mg/kg) |
| LD₅₀ (Oral) | Ratazana | 7,06 mg/kg |
| LD₅₀ (Oral) | Rato | 3,45 g/kg (10,5 ml/kg) |
| LD₅₀ (Oral) | Coelho | 6,30 mg/kg |
| LC₅₀ (Inalação) | Ratazana | 5.900 mg/m³ (6h) / 20.000 ppm (10h) |
| LCLo (Inalação) | Rato | 29.300 ppm (7h) |
| TCLo (Inalação) | Humanos | 2.500 mg/m³ (20m) / 1.800 ppm (30m) |
| Irritação ocular | Coelho | 500 mg (24h) |
| Irritação cutânea | Coelho | 20 mg (24h) |
Aplicações
Na natureza, as latrunculinas são utilizadas pelas próprias esponjas como mecanismos de defesa, e com esse mesmo propósito são sequestradas por nudibrânquios.[21] As latrunculinas são utilizadas em investigação básica e possuem possíveis aplicações médicas, uma vez que as latrunculinas e os seus derivados mostram atividades antiangiogénicas, antiproliferativas, antimicrobianas e antimetastáticas.[2]
Mecanismos de defesa
As esponjas, como muitos outros organismos sésseis, contêm muitos metabolitos secundários com propriedades tóxicas e a maioria deles, incluindo a latrunculina, desempenha um papel na defesa contra predadores, competidores e epibiontes.[22] Para as esponjas, a latrunculina é inócua. Como medida contra a autointoxicação, mantêm a latrunculina dentro de vacúolos rodeados de membrana, que também funcionam como vesículas secretoras e de armazenamento. Estes vacúolos carecem de actina e impedem que a latrunculina entre no citosol, onde danificaria a actina.[22] Após a sua produção nos coanócitos da esponja, a latrunculina é transportada pelos arqueócitos para as áreas vulneráveis da esponja onde se necessita de defesa, como em partes danificadas ou sítios em regeneração.[22]
Sequestro por nudibrânquios
As lesmas do mar do género Chromodoris sequestram como metabolitos defensivos diferentes tóxicos originados nas esponjas de que se alimentam, incluindo a latrunculina. Transferem seletivamente e armazenam latrunculina nos sítios do manto que estão mais expostos a um possível predador.[21] Pensa-se que o sistema digestivo dos nudibrânquios desempenha um importante papel na desintoxicação.[21] Em 2015, a descoberta de que cinco lesmas do mar estreitamente aparentadas do género Chromodoris usam latrunculina como defesa, indica que o tóxico poderá estar a ser utilizado como mimetismo mülleriano.[21]
Referências
- ↑ a b Braet F, De Zanger R, Jans D, Spector I, Wisse E (setembro de 1996). «Microfilament-disrupting agent latrunculin A induces and increased number of fenestrae in rat liver sinusoidal endothelial cells: comparison with cytochalasin B». Hepatology. 24 (3): 627–35. PMID 8781335. doi:10.1002/hep.510240327
- ↑ a b El Sayed KA, Youssef DT, Marchetti D (fevereiro de 2006). «Bioactive natural and semisynthetic latrunculins». Journal of Natural Products. 69 (2): 219–23. Bibcode:2006JNAtP..69..219E. PMID 16499319. doi:10.1021/np050372r
- ↑ a b Coué M, Brenner SL, Spector I, Korn ED (março de 1987). «Inhibition of actin polymerization by latrunculin A». FEBS Letters. 213 (2): 316–8. Bibcode:1987FEBSL.213..316C. PMID 3556584. doi:10.1016/0014-5793(87)81513-2
- ↑ a b c Pubchem. «Latrunculin A». pubchem.ncbi.nlm.nih.gov (em inglês). Consultado em 26 de abril de 2018
- ↑ a b c Groweiss, Amiram; Shmueli, Uri; Kashman, Yoel (1 de outubro de 1983). «Marine toxins of Latrunculia magnifica». The Journal of Organic Chemistry. 48 (20): 3512–3516. doi:10.1021/jo00168a028
- ↑ a b Kashman V, Groweiss A, Shmueli U (janeiro de 1980). «Latrunculin, a new 2-thiazolidinone macrolide from the marine sponge». Tetrahedron Letters. 21 (37): 3629–3632. doi:10.1016/0040-4039(80)80255-3
- ↑ Maier ME (maio de 2015). «Design and synthesis of analogues of natural products». Organic & Biomolecular Chemistry. 13 (19): 5302–43. PMID 25829247. doi:10.1039/C5OB00169B
- ↑ a b Morton WM, Ayscough KR, McLaughlin PJ (junho de 2000). «Latrunculin alters the actin-monomer subunit interface to prevent polymerization». Nature Cell Biology. 2 (6): 376–8. PMID 10854330. doi:10.1038/35014075. hdl:1842/757
- ↑ Tazerart S, Mitchell DE, Miranda-Rottmann S, Araya R (agosto de 2020). «A spike-timing-dependent plasticity rule for dendritic spines». Nature Communications. 11 (1): 4276. Bibcode:2020NatCo..11.4276T. PMC 7449969
 . PMID 32848151. doi:10.1038/s41467-020-17861-7
. PMID 32848151. doi:10.1038/s41467-020-17861-7
- ↑ Maluykova I, Gutsal O, Laiko M, Kane A, Donowitz M, Kovbasnjuk O (junho de 2008). «Latrunculin B facilitates Shiga toxin 1 transcellular transcytosis across T84 intestinal epithelial cells». Biochimica et Biophysica Acta (BBA) - Molecular Basis of Disease. 1782 (6): 370–7. PMC 2509583
 . PMID 18342638. doi:10.1016/j.bbadis.2008.01.010
. PMID 18342638. doi:10.1016/j.bbadis.2008.01.010
- ↑ Wakatsuki T, Schwab B, Thompson NC, Elson EL (março de 2001). «Effects of cytochalasin D and latrunculin B on mechanical properties of cells». Journal of Cell Science. 114 (Pt 5): 1025–36. PMID 11181185. doi:10.1242/jcs.114.5.1025
- ↑ Spector I, Shochet NR, Blasberger D, Kashman Y (1989). «Latrunculins--novel marine macrolides that disrupt microfilament organization and affect cell growth: I. Comparison with cytochalasin D». Cell Motility and the Cytoskeleton. 13 (3): 127–44. PMID 2776221. doi:10.1002/cm.970130302
- ↑ Pendleton A, Koffer A (janeiro de 2001). «Effects of latrunculin reveal requirements for the actin cytoskeleton during secretion from mast cells». Cell Motility and the Cytoskeleton. 48 (1): 37–51. PMID 11124709. doi:10.1002/1097-0169(200101)48:1<37::aid-cm4>3.0.co;2-0
- ↑ Yarmola EG, Somasundaram T, Boring TA, Spector I, Bubb MR (setembro de 2000). «Actin-latrunculin A structure and function. Differential modulation of actin-binding protein function by latrunculin A». The Journal of Biological Chemistry. 275 (36): 28120–7. PMID 10859320. doi:10.1074/jbc.m004253200
- ↑ Gronewold TM, Sasse F, Lünsdorf H, Reichenbach H (janeiro de 1999). «Effects of rhizopodin and latrunculin B on the morphology and on the actin cytoskeleton of mammalian cells». Cell and Tissue Research. 295 (1): 121–9. PMID 9931358. doi:10.1007/s004410051218
- ↑ Fairn GD, McMaster CR (janeiro de 2008). «Emerging roles of the oxysterol-binding protein family in metabolism, transport, and signaling». Cellular and Molecular Life Sciences. 65 (2): 228–36. PMC 11131761
 . PMID 17938859. doi:10.1007/s00018-007-7325-2
. PMID 17938859. doi:10.1007/s00018-007-7325-2
- ↑ a b Gibbon BC, Kovar DR, Staiger CJ (dezembro de 1999). «Latrunculin B has different effects on pollen germination and tube growth». The Plant Cell. 11 (12): 2349–63. Bibcode:1999PlanC..11.2349G. PMC 144132
 . PMID 10590163. doi:10.1105/tpc.11.12.2349
. PMID 10590163. doi:10.1105/tpc.11.12.2349
- ↑ a b Konishi H, Kikuchi S, Ochiai T, Ikoma H, Kubota T, Ichikawa D, Fujiwara H, Okamoto K, Sakakura C, Sonoyama T, Kokuba Y, Sasaki H, Matsui T, Otsuji E (junho de 2009). «Latrunculin a has a strong anticancer effect in a peritoneal dissemination model of human gastric cancer in mice». Anticancer Research. 29 (6): 2091–7. PMID 19528469
- ↑ Roa-Espitia AL, Hernández-Rendón ER, Baltiérrez-Hoyos R, Muñoz-Gotera RJ, Cote-Vélez A, Jiménez I, González-Márquez H, Hernández-González EO (setembro de 2016). «Focal adhesion kinase is required for actin polymerization and remodeling of the cytoskeleton during sperm capacitation». Biology Open. 5 (9): 1189–99. PMC 5051654
 . PMID 27402964. doi:10.1242/bio.017558
. PMID 27402964. doi:10.1242/bio.017558
- ↑ Spector I, Shochet NR, Kashman Y, Groweiss A (fevereiro de 1983). «Latrunculins: novel marine toxins that disrupt microfilament organization in cultured cells». Science. 219 (4584): 493–5. Bibcode:1983Sci...219..493S. PMID 6681676. doi:10.1126/science.6681676
- ↑ a b c d Cheney KL, White A, Mudianta IW, Winters AE, Quezada M, Capon RJ, Mollo E, Garson MJ (20 de janeiro de 2016). «Choose Your Weaponry: Selective Storage of a Single Toxic compound, Latrunculin A, by Closely Related Nudibranch Molluscs». PLOS ONE. 11 (1 (número de artigo: e0145134)). Bibcode:2016PLoSO..1145134C. PMC 4720420
 . PMID 26788920. doi:10.1371/journal.pone.0145134
. PMID 26788920. doi:10.1371/journal.pone.0145134
- ↑ a b c Gillor O, Carmeli S, Rahamim Y, Fishelson Z, Ilan M (maio de 2000). «Immunolocalization of the Toxin Latrunculin B within the Red Sea Sponge Negombata magnifica (Demospongiae, Latrunculiidae)». Marine Biotechnology. 2 (3): 213–23. Bibcode:2000MarBt...2..213G. PMID 10852799. doi:10.1007/s101260000026