Ionona
Iononas
| |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| Nomes | |||||||||||||||
| Nome IUPAC | α: (3E)-4-(2,6,6-Trimetilciclohex-2-en-1-il)but-3-en-2-ona β: (3E)-4-(2,6,6-Trimetilciclohex-1-en-1-il)but-3-en-2-ona γ: (3E)-4-(2,2-Dimetil-6-metileneciclohexil)but-3-en-2-ona | ||||||||||||||
| Outros nomes | Ciclocitrilidenoacetona, irisona | ||||||||||||||
| |||||||||||||||
| |||||||||||||||
| Página de dados suplementares | |||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||
As iononas (do grego ἴον, ion, 'violeta'),[1] são uma série de compostos químicos estreitamente relacionados que formam parte de um grupo chamado cetonas de rosas, entre os quais também estão as damasconas e as damascenonas. As iononas são compostos odoríferos encontrados em diversos óleos essenciais, incluindo o óleo de rosas. A β-ionona contribui significativamente para o aroma das rosas, apesar da sua baixa concentração relativa, e é um importante composto fragrante usado em perfumaria.[2] As iononas derivam da degradação dos carotenoides. Distinguem-se as alfa, beta e gama-iononas, dependendo da posição de uma ligação dupla na parte cíclica da molécula. A combinação de α-ionona e β-ionona é característica do aroma das violetas e utilizada juntamente com outros compostos em perfumaria e na aromatização para recriar o aroma a violetas.[3][4] Os carotenos α-caroteno, β-caroteno e γ-caroteno, e a xantofila β-criptoxantina, podem ser metabolizados a β-ionona e assim têm atividade de vitamina A, porque podem ser convertidos pelos animais herbívoros em retinol e retinal. Os carotenoides que não contêm um radical de β-ionona não podem converter-se em retinol e carecem de atividade de vitamina A.
Biossíntese
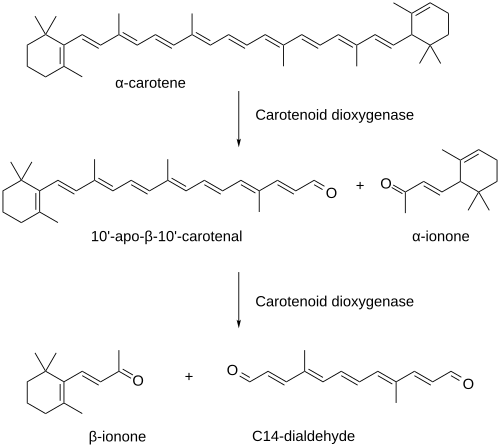
Os carotenoides são os precursores de importantes compostos fragrantes de várias flores. Por exemplo, um estudo de 2010 sobre as iononas de Osmanthus fragrans Lour. var. aurantiacus determinou que o seu óleo essencial continha a maior diversidade de voláteis derivados de carotenoides entre todas as plantas com flor investigadas. Foi identificado um ADNc que codifica uma enzima que corta os carotenoides chamada OfCCD1, a partir de transcritos isolados de flores de O. fragrans Lour. As enzimas recombinantes cortavam os carotenos para produzir α-ionona e β-ionona em ensaios in vitro.[5] O mesmo estudo também descobriu que o conteúdo de carotenoides, as emissões voláteis e o nível de transcritos de OfCCD1 estão sujeitos a mudanças fotorrítmicas e aumentam principalmente durante as horas de luz. Nos momentos em que os níveis de transcritos de OfCCD1 chegam aos seus máximos, o conteúdo de carotenoides permanece baixo ou diminui ligeiramente. A emissão de iononas era também maior durante o dia; no entanto, as emissões diminuíam a menor ritmo do que o faziam os níveis de transcritos. Além disso, o conteúdo de carotenoides aumentava do primeiro ao segundo dia, enquanto que a libertação de voláteis diminuía e os níveis de transcritos de OfCCD1 apresentavam oscilações do estado estável, o que sugere que a disponibilidade do substrato enzimático nos compartimentos celulares é mutável ou intervêm outros fatores regulatórios na formação de norisoprenoides. A formação de iononas realiza-se por um processo mediado pelas carotenoide dioxigenases.[5]
Síntese orgânica
As iononas podem ser sintetizadas a partir de citral e acetona com óxido de cálcio como catalisador heterogéneo básico e servem como exemplo de condensação aldólica seguida de uma reação de redistribuição.[6][7] A adição nucleofílica do carbanion 3 da acetona 1 ao grupo carbonilo do citral 4 é catalisada por bases. O produto da condensação aldólica 5 elimina água por meio do ião enolato 6 para formar pseudoionona 7.
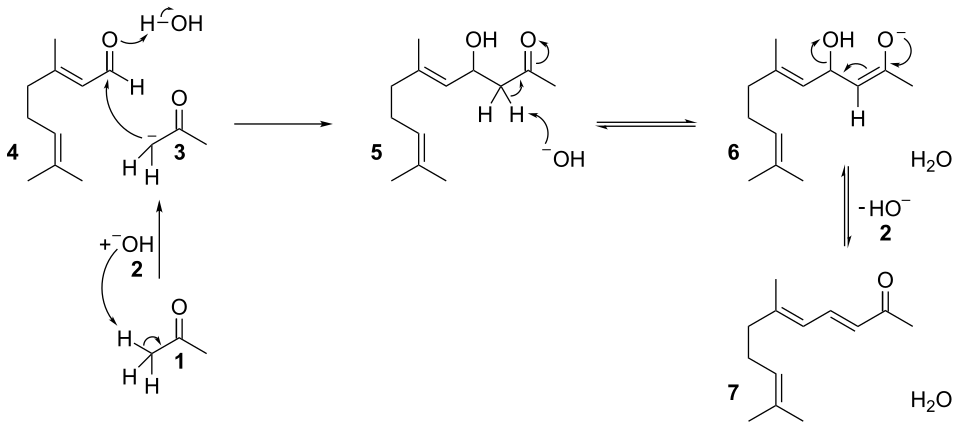
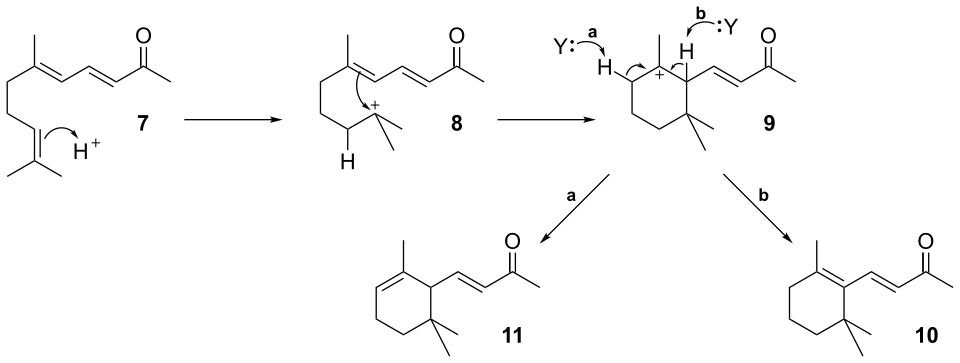
A seguinte reação é realizada por catálise ácida na qual se abre a ligação dupla de 7 para formar o carbocatião 8. De seguida há uma reação de redistribuição do carbocatião com o fecho de um anel dando 9. Finalmente, pode ser extraído um átomo de hidrogénio de 9 por uma molécula aceitadora (Y) para formar 10 (sistema conjugado ampliado) ou bem 11.
Diferenças genéticas na perceção do odor
Um polimorfismo de nucleótido único no receptor OR5A1 (rs6591536[8]) causa diferenças muito significativas na perceção do cheiro da beta-ionona, tanto em sensibilidade como em qualidade subjetiva. Os indivíduos que têm menos de um alelo G são sensíveis à beta-ionona e percebem um agradável aroma floral, enquanto que os que são homozigotos AA são ~100 vezes menos sensíveis e a maiores concentrações percebem em seu lugar um cheiro pungente a azedo/vinagre.[9]
Referências
- ↑ Genaust, Helmut (1976). Etymologisches Wörterbuch der botanischen Pflanzennamen. [S.l.: s.n.] ISBN 978-3-0348-7651-3. doi:10.1007/978-3-0348-7650-6
- ↑ Leffingwell, JC (3 de fevereiro de 2005). «Rose (Rosa damascena)». Aroma from Carotenoids - Rose. Leffingwell & Associates. Consultado em 14 de janeiro de 2014
- ↑ Curtis, T; Williams, DG (2001). Introduction to Perfumery 2nd ed. Fort Washington, Nova Iorque: Micelle Press. ISBN 9781870228244
- ↑ Jensen, B (6 de fevereiro de 2010). «Violet». Essential Oils. Consultado em 14 de janeiro de 2014
- ↑ a b Baldermann, S; Kato, M; Kurosawa, M; Kurobayashi, Y; Fujita, A; Fleischmann, P; Watanabe, N (2010). «Functional characterization of a carotenoid cleavage dioxygenase 1 and its relation to the carotenoid accumulation and volatile emission during the floral development of Osmanthus fragrans Lour». Journal of Experimental Botany. 61 (11): 2967–2977. PMID 20478967. doi:10.1093/jxb/erq123
- ↑ Noda, C; Alt, GP; Werneck, RM; Henriques, C. A.; Monteiro, JLF (1998). «Aldol condensation of citral with acetone on basic solid catalysts». Brazilian Journal Chemical Engineering. 15 (2): 120–125. doi:10.1590/S0104-66321998000200004
- ↑ Russell, A; Kenyon, RL (1943). «Pseudoionone». Organic Syntheses. 23. 78 páginas. doi:10.15227/orgsyn.023.0078
- ↑ «rs6591536». SNPedia
- ↑ Jaeger SR, McRae JF, Bava CM, Beresford MK, Hunter D, Jia Y, Chheang SL, Jin D, Peng M, Gamble JC, Atkinson KR, Axten LG, Paisley AG, Tooman L, Pineau B, Rouse SA, Newcomb RD (2013). «A Mendelian Trait for Olfactory Sensitivity Affects Odor Experience and Food Selection». Current Biology. 23 (16): 1601–1605. PMID 23910657. doi:10.1016/j.cub.2013.07.030