Hexafluoreto de telúrio
Hexafluoreto de telúrio
| |||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||||||
| |||||||||||||||||||||||
| |||||||||||||||||||||||
| |||||||||||||||||||||||
| |||||||||||||||||||||||
| |||||||||||||||||||||||
| Página de dados suplementares | |||||||||||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||||||||||
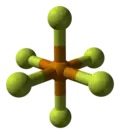
O hexafluoreto de telúrio é um composto químico de telúrio e flúor com a fórmula química TeF6 . É um gás incolor e altamente tóxico, com um cheiro extremamente desagradável.
Preparação
O hexafluoreto de telúrio é mais comumente preparado passando o gás flúor sobre o telúrio a 150 °C. Abaixo desta temperatura, forma-se uma mistura de fluoretos inferiores, incluindo tetrafluoreto de telúrio e decafluoreto de ditelúrio. Também pode ser preparado passando gás flúor sobre TeO3 ou indiretamente reagindo TeO2 com SeF4 para produzir TeF4 e depois aquecendo TeF4 acima de 200 °C para produzir TeF6 e Te.
Propriedades
O hexafluoreto de telúrio é uma molécula octaédrica altamente simétrica. Suas propriedades físicas se assemelham aos análogos de enxofre e selênio. É menos volátil, no entanto, devido ao aumento do peso molecular. A temperaturas abaixo de -38 °C, o hexafluoreto de telúrio condensa em um sólido branco volátil.
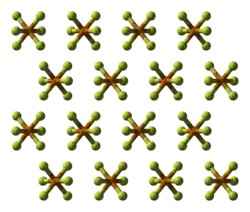

Reatividade
Ao contrário do análogo Hexafluoreto de enxofre, o hexafluoreto de telúrio não é quimicamente inerte. Isso pode ser atribuído ao raio atômico maior, que pode coordenar um máximo de oito átomos em vez de seis como o enxofre e o selênio, o que permite o ataque nucleofílico. TeF6 é hidrolisado em água para ácido telúrico (Te(OH)6) e pode reagir com o Te abaixo de 200 °C.
TeF6 + 6 H2O -> Te(OH)6 + 6 HF
Literatura
- W.C. Cooper; Tellurium, Van Nostrand Reinhold Company, New York, USA, 1971.
- K.W. Bagnall; The Chemistry of Selenium, Tellurium and Polonium, Elsevier Publishing, New York, 1966.
- R.T. Sanderson; Chemical Periodicity, Reinhold, New York, USA, 1960.
- N.N. Greenwood and A. Earnshaw; Chemistry of the Elements, 2nd edition, Butterworth, UK, 1997.
- F. A. Cotton, G. Wilkinson, C.A. Murillo, and M. Bochmann; Advanced Inorganic Chemistry, John Wiley & Sons, 1999.
- G.J. Hathaway, N.H. Proctor; Chemical Hazards of the Workplace, 5th edition, Wiley-Interscience, New Jersey, 2004.