Heptóxido de dicloro
Heptóxido de dicloro
| |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||
| Nomes | |||||||||||||||
| Nome IUPAC | Heptóxido de dicloro | ||||||||||||||
| Outros nomes | Óxido de cloro (VII); Anidrido perclórico; Óxido perclórico; Trióxido (percloriloxi)clorano | ||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| Página de dados suplementares | |||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||
Heptóxido de dicloro é o composto químico com a fórmula Cl2O7. Este óxido de cloro é o anidrido do ácido perclórico. É produzido pela cuidadosa destilação do ácido perclórico na presença do agente desidratante pentóxido de fósforo:[1]
- 2 HClO4 + P4O10 → Cl2O7 + H2P4O11
Ele lentamente hidroliza-se novamente a ácido perclórico, o qual é também perigoso quando anidro.
Cl2O7 é uma molécula endotérmica, o que significa que é intrinsicamente instável.
- Cl2O7 → Cl2 + 3.5 O2 ΔH = 135 kJ/mol
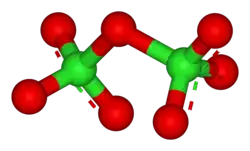
Cl2O7 é ligado com ângulo Cl-O-Cl de 118.6° dando a molécula simetria C2. As distâncias dos Cl-O terminais são 1.709 Å e as distâncias Cl=O são de 1.405 Å.[1] Neste comsposto, o cloro existe em seu mais alto estado de oxidação de 7+, embora a ligação nesta molécula hipervalente seja significativamente covalente.
Segurança
Cl2O7 é um forte oxidante assim como um explosivo que deve ser mantido afastado de chamas ou choques mecânicos.