Hemeritrina
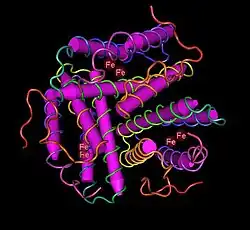
A hemeritrina' (do grego ἀμέρα = sangue, e ερυθρός = vermelho) é uma proteína oligomérica responsável pelo transporte de oxigénio (O2) em certos filos de invertebrados marinhos, especificamente em sipunculídeos, priapulídeos, braquiópodess, e também em anelídeoss do género Magellan. Recentemente, a hemoeritrina foi descoberta em bactérias metanotróficas da espécie Methylococcus capsulatus.[1] A Miohemeritrina é uma proteína monomérica de ligação ao O2 que se encontra nos músculos dos invertebrados marinhos. A hemohemeritrina e a miohemeritrina são essencialmente incolores quando desoxigenadas, mas adquirem uma coloração rosa-violeta no estado oxigenado.
A hemohemeritrina não contém o grupo heme, apesar do seu nome o sugerir. Os nomes dos transportadores de oxigénio nos seres vivos, hemoglobina, hemocianina e hemeritrina, não se referem ao grupo heme das globinas (que somente a hemoglobina possui), mas são derivados da palavra grega para "sangue".
Mecanismo de ligação ao oxigénio (O2)
O mecanismo de ligação ao dioxigénio desta proteína é invulgar. A maioria dos transportadores de O2 funciona formando complexos de dioxigénio, mas a hemeritrina mantém o O2 sob a forma de hidroperóxido. O sítio de ligação do O2 consiste num par de centros de ferro. Os átomos de ferro estão ligados à proteína através das cadeias laterais cadeia lateral carboxilato dos resíduos glutamato e aspartato e por cinco resíduos de histidina. A hemeritrina e a miohemeritrina são frequentemente descritas pelos estados de ligação e oxidação dos seus centros de ferro:
| Fe2+—OH—Fe2+ | desoxi (reducido) |
| Fe2+—OH—Fe3+ | semi-met |
| Fe3+—O—Fe3+—OOH- | oxi (oxidado) |
| Fe3+—OH—Fe3+— (qualquer outro ligando) | met (oxidado) |
A captação de O2 pela hemeritrina é acompanhada pela oxidação de dois eletrões do centro diferferroso para produzir um complexo hidroperóxido (OOH-). A ligação de O2 é geralmente descrita neste diagrama:

Sítio ativo da hemeritrina antes e depois da oxigenação.
A desoxihemeritrina contém dois iões ferrosos de spin alto ligados por um grupo hidroxilo. Um ferro é hexacoordenado e o outro é pentacoordenado. Um grupo hidroxilo serve como ligante de ponte, mas também funciona como dador de protões para o substrato O2. Esta transferência de protões resulta na formação de uma ponte de oxigénio simples (μ-oxo) na oxihemeritrina e na metemeritrina. O O2 liga-se ao centro Fe2+ pentacoordenado no sítio de coordenação vazio. Os eletrões são então transferidos dos iões ferrosos para gerar o centro férrico binuclear (Fe3+,Fe3+) com o peróxido ligado.[2][3]
Estrutura quaternária e cooperatividade
A hemeritrina existe normalmente como um homooctámero ou heterooctámero composto por subunidades α e β de 13-14 kDa, embora algumas espécies possuam hemeritrinas diméricas, triméricas e tetraméricas. Cada subunidade possui uma dobra α de quatro hélices que se liga a um centro binuclear de ferro. Devido ao seu tamanho, a hemeritrina encontra-se geralmente no interior de células ou "corpúsculos" do sangue, não flutuando livremente no fluido.
Ao contrário da hemoglobina, a maioria das hemeritrinas não apresenta ligação cooperativa para o oxigénio, sendo apenas 1/4 tão eficiente como a hemoglobina. No entanto, em alguns braquiópodes, a hemeritrina apresenta uma ligação cooperativa para o O2. Esta ligação cooperativa deve-se às interações entre subunidades: a oxigenação de uma subunidade aumenta a afinidade de uma segunda subunidade pelo oxigénio.
A afinidade da hemeritrina pelo monóxido de carbono (CO) é menor do que pelo O2, o que a distingue da hemoglobina, que tem uma afinidade muito maior pelo CO. A baixa afinidade da hemeritrina pelo CO reflete o papel das ligações de hidrogénio na ligação ao O2, um mecanismo incompatível com os complexos de CO, que normalmente não formam ligações de hidrogénio.
Domínio de ligação de catiões HHE/hemeritrina
| Domínio de ligação do catão HHE da hemoritrina | |
|---|---|
| Indicadores | |
| Pfam | PF01814 |
| InterPro | IPR012312 |
| PROSITE | PDOC00476 |
| SCOP | 2hmq |
O domínio de ligação do catão HHE/hemeritrina aparece como um domínio duplicado nas hemeritrinas, miohemeritrinas e outras proteínas relacionadas. Este domínio liga-se ao ferro nas hemeritrinas, mas pode ligar-se a outros metais em proteínas relacionadas, como o cádmio na hemeritrina do anelídeo Nereis diversicolor. Também se encontra na proteína NorA da bactéria Cupriavidus necator; esta proteína é um regulador da resposta ao óxido nítrico, sugerindo que tem um arranjo diferente para estes ligantes metálicos. Uma proteína da levedura Cryptococcus neoformans que contém este domínio está também envolvida na resposta ao óxido nítrico.[4] Uma proteína da bacteria Staphylococcus aureus que contém este dominio chamada proteína de reparação do cluster de ferro-enxofre ScdA.[5]
Notas
Referências
- ↑ Karlsen, O.A., Ramsevik, L., Bruseth, L.J., Larsen, Ø., Brenner, A., Berven, F.S., Jensen, H.B. and Lillehaug, J.R. (2005). «Characterization of a prokaryotic haemerythrin from the methanotrophic bacterium Methylococcus capsulatus (Bath)». FEBS J. 272 (10): 2428–2440. PMID 15885093. doi:10.1111/j.1742-4658.2005.04663.x
- ↑ D. M. Kurtz, Jr. "Dioxygen-binding Proteins" in Comprehensive Coordination Chemistry II 2003, Volume 8, Pages 229-260. doi:10.1016/B0-08-043748-6/08171-8
- ↑ Friesner, R. A., M.-H. Baik, B. F. Gherman, V. Guallar, M. Wirstam, R. B. Murphy, and S. J. Lippard, 2003, How iron-containing proteins control dioxygen chemistry: a detailed atomic level description via accurate quantum chemical and mixed quantum mechanics/molecular mechanics calculations: Coord. Chem. Rev., v. 238-239, p. 267-290.
- ↑ Chow ED, Liu OW, O'Brien S, Madhani HD (September 2007). «Exploration of whole-genome responses of the human AIDS-associated yeast pathogen Cryptococcus neoformans var grubii: nitric oxide stress and body temperature». Curr. Genet. 52 (3–4): 137–48. PMID 17661046. doi:10.1007/s00294-007-0147-9 Verifique data em:
|data=(ajuda) - ↑ Overton TW, Justino MC, Li Y, Baptista JM, Melo AM, Cole JA; et al. (2008). «Widespread Distribution in Pathogenic Bacteria of Di-Iron Proteins That Repair Oxidative and Nitrosative Damage to Iron-Sulfur Centers». J Bacteriol. 190 (6): 2004–13. PMC 2258886
 . PMID 18203837. doi:10.1128/JB.01733-07
. PMID 18203837. doi:10.1128/JB.01733-07
Ver também
- Hemocianina
- Hemoglobina
- Clorocruorina
- Eritrocruorina